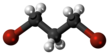1,3-Dibromopropane - 1,3-Dibromopropane
|
|
|||
|
|
|||
| Des noms | |||
|---|---|---|---|
|
Nom IUPAC préféré
1,3-dibromopropane |
|||
| Autres noms | |||
| Identifiants | |||
|
Modèle 3D ( JSmol )
|
|||
| 635662 | |||
| ChemSpider | |||
| Carte d'information de l'ECHA |
100.003.356 |
||
| Numéro CE | |||
| Engrener | 1,3-dibromopropane | ||
|
CID PubChem
|
|||
| Numéro RTECS | |||
| UNII | |||
| Numéro ONU | 1993 | ||
|
Tableau de bord CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriétés | |||
| C 3 H 6 Br 2 | |||
| Masse molaire | 201,889 g·mol -1 | ||
| Apparence | Liquide incolore | ||
| Densité | 1,989 g mL -1 | ||
| Point de fusion | −34,20 °C ; -29,56 °F ; 238,95 K | ||
| Point d'ébullition | 167 °C ; 332 °F; 440 K | ||
|
Constante de la loi de Henry ( k H ) |
11 mol Pa -1 kg -1 | ||
|
Indice de réfraction ( n D )
|
1.524 | ||
| Thermochimie | |||
|
Capacité calorifique ( C )
|
163,7 JK mol -1 | ||
| Dangers | |||
| Pictogrammes SGH |
  
|
||
| Mention d'avertissement SGH | Avertissement | ||
| H226 , H302 , H315 , H411 | |||
| P273 | |||
| point de rupture | 56 °C (133 °F; 329 K) | ||
| Dose ou concentration létale (LD, LC) : | |||
|
DL 50 ( dose médiane )
|
315 mg kg -1 (orale, rat) | ||
| Composés apparentés | |||
|
Alcanes apparentés
|
|||
|
Composés apparentés
|
Mitobronitol | ||
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 °C [77 °F], 100 kPa). |
|||
|
|
|||
| Références de l'infobox | |||
Le 1,3-dibromopropane est un composé organobromé de formule (CH 2 ) 3 Br 2 . C'est un liquide incolore à l'odeur sucrée. Il est utilisé dans la synthèse organique pour former C 3 composés -bridged tels que des réactions de couplage par l' intermédiaire du CN.
Le 1,3-dibromopropane a été utilisé dans la première synthèse du cyclopropane en 1881, connue sous le nom de réaction de Freund .
La synthèse
Le 1,3-dibromopropane peut être préparé via l' addition de radicaux libres entre le bromure d'allyle et le bromure d'hydrogène .
Métabolisme
Le métabolisme du 1,3-dibromopropane a été examiné en 1981. L'examen a été effectué en administrant oralement du 1,3-dibromopropane à des rats et en recueillant les résultats 24 heures après l'administration. Les résultats ont été obtenus à partir de trois sources : l'urine, les matières fécales et l'air expiré. Après analyse des résultats urinaires, les chercheurs ont découvert la formation de métabolite, la N- acétyl- S- (1-bromo-3-propyl)-cystéine et la baisse de la teneur en GSH du foie des rats. Cela a conduit à l'hypothèse que le 1,3-dibromopropane aurait pu réagir avec le GSH après administration et donner naissance au 1-bromo-3- propyl - S- glutathion, qui forme finalement le métabolite urinaire. De plus, en raison de la faible radioactivité observée dans les matières fécales et de la confirmation des taux sanguins de radioactivité maintenus, l'excrétion biliaire de métabolites contenant du soufre et le cycle entérohépatique ont été confirmés.