Motoneurone alpha - Alpha motor neuron
| Neurone moteur alpha | |
|---|---|
 Les neurones moteurs alpha sont dérivés de la plaque basale (lame basale) de l' embryon en développement .
| |
| Identifiants | |
| Identifiant NeuroLex | sao1154704263 |
| E | H2.0.01.0.00008 |
| FMA | 83664 |
| Termes anatomiques de la neuroanatomie | |
Alpha ( α ) des neurones moteurs (également appelés motoneurones alpha ), sont grandes, les multipolaires neurones moteurs inférieurs du tronc cérébral et la moelle épinière . Ils innervent les fibres musculaires extrafusales du muscle squelettique et sont directement responsables d'initier leur contraction . Les motoneurones alpha sont distincts des motoneurones gamma , qui innervent les fibres musculaires intrafusales des fuseaux musculaires .
Alors que leurs corps cellulaires se trouvent dans le système nerveux central (SNC), les motoneurones α sont également considérés comme faisant partie du système nerveux somatique - une branche du système nerveux périphérique (SNP) - car leurs axones s'étendent vers la périphérie pour innerver les muscles squelettiques. .
Un motoneurone alpha et les fibres musculaires qu'il innerve constituent une unité motrice . Un pool de motoneurones contient les corps cellulaires de tous les motoneurones alpha impliqués dans la contraction d'un seul muscle.
Emplacement
Les neurones moteurs alpha (α-MNs) innervant la tête et le cou se trouvent dans le tronc cérébral ; les -MN restants innervent le reste du corps et se trouvent dans la moelle épinière . Il y a plus de -MN dans la moelle épinière que dans le tronc cérébral, car le nombre de -MN est directement proportionnel à la quantité de contrôle de la motricité fine dans ce muscle. Par exemple, les muscles d'un seul doigt ont plus de -MN par fibre, et plus de α-MN au total, que les muscles du quadriceps , ce qui permet un contrôle plus fin de la force appliquée par un doigt.
En général, les -MN d'un côté du tronc cérébral ou de la moelle épinière innervent les muscles de ce même côté du corps. Une exception est le noyau trochléaire dans le tronc cérébral, qui innerve le muscle oblique supérieur de l'œil du côté opposé du visage.
Tronc cérébral
Dans le tronc cérébral, les -MN et d'autres neurones résident dans des grappes de cellules appelées noyaux , dont certaines contiennent les corps cellulaires des neurones appartenant aux nerfs crâniens . Tous les noyaux des nerfs crâniens ne contiennent pas de -MN; ceux qui le font sont des noyaux moteurs , tandis que d'autres sont des noyaux sensoriels . Les noyaux moteurs se trouvent dans tout le tronc cérébral - moelle , pont et mésencéphale - et pour des raisons de développement se trouvent près de la ligne médiane du tronc cérébral.
En règle générale, les noyaux moteurs situés plus haut dans le tronc cérébral (c'est-à-dire plus rostral) innervent les muscles situés plus haut sur le visage. Par exemple, le noyau oculomoteur contient des -MN qui innervent les muscles de l'œil et se trouve dans le mésencéphale, le composant le plus rostral du tronc cérébral. En revanche, le noyau hypoglosse , qui contient des -MN qui innervent la langue, se trouve dans la moelle, la plus caudale (c'est-à-dire vers le bas) des structures du tronc cérébral.
Moelle épinière

Dans la moelle épinière, les -MN sont situés dans la matière grise qui forme la corne ventrale . Ces α-MN fournissent la composante motrice des nerfs spinaux qui innervent les muscles du corps.
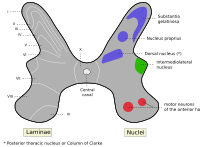
Comme dans le tronc cérébral, les segments supérieurs de la moelle épinière contiennent des -MN qui innervent les muscles plus haut sur le corps. Par exemple, le muscle biceps brachial , un muscle du bras, est innervé par les -MN dans les segments de la moelle épinière C5, C6 et C7, qui se trouvent rostralement dans la moelle épinière. D'autre part, le muscle gastrocnémien , l'un des muscles de la jambe, est innervé par les -MN au sein des segments S1 et S2, qui se trouvent caudalement dans la moelle épinière.
Les motoneurones alpha sont situés dans une région spécifique de la matière grise de la moelle épinière. Cette région est appelée lamina IX dans le système Rexed lamina , qui classe les régions de la matière grise en fonction de leur cytoarchitecture . La lame IX est située principalement dans la face médiale de la corne ventrale, bien qu'il y ait une certaine contribution à la lame IX à partir d'un ensemble de neurones moteurs situés plus latéralement. Comme d'autres régions de la moelle épinière, les cellules de cette lame sont organisées de manière somatotopique , ce qui signifie que la position des neurones dans la moelle épinière est associée aux muscles qu'ils innervent. En particulier, les -MN de la zone médiale de la lame IX ont tendance à innerver les muscles proximaux du corps, tandis que ceux de la zone latérale ont tendance à innerver les muscles plus distaux. Il existe une somatotopie similaire associée aux -MN qui innervent les muscles fléchisseurs et extenseurs : les α-MN qui innervent les fléchisseurs ont tendance à être situés dans la partie dorsale de la lame IX ; ceux qui innervent les extenseurs ont tendance à être situés plus ventralement.
Développement
Les neurones moteurs alpha proviennent de la plaque basale , la partie ventrale du tube neural de l' embryon en développement . Le hérisson sonique (Shh) est sécrété par la notocorde voisine et d'autres structures ventrales (par exemple, la plaque de plancher ), établissant un gradient de Shh hautement concentré dans la plaque basale et de Shh moins concentré dans la plaque alaire . Sous l'influence de Shh et d'autres facteurs, certains neurones de la plaque basale se différencient en -MN.
Comme les autres neurones, les -MN envoient des projections axonales pour atteindre leurs fibres musculaires extrafusales cibles via le guidage axonal , un processus régulé en partie par des facteurs neurotrophiques libérés par les fibres musculaires cibles. Les facteurs neurotrophiques garantissent également que chaque fibre musculaire est innervée par le nombre approprié de -MN. Comme pour la plupart des types de neurones du système nerveux , les -MN sont plus nombreux au début du développement qu'à l'âge adulte. Les fibres musculaires sécrètent une quantité limitée de facteurs neurotrophiques capables de ne soutenir qu'une fraction des -MN qui se projettent initialement vers la fibre musculaire. Les -MN qui ne reçoivent pas suffisamment de facteurs neurotrophiques subiront l' apoptose , une forme de mort cellulaire programmée .
Parce qu'ils innervent de nombreux muscles, certains groupes de -MN reçoivent des concentrations élevées de facteurs neurotrophiques et survivent à cette étape de l'élagage neuronal. C'est le cas des -MNs innervant les membres supérieurs et inférieurs : ces -MNs forment de grandes colonnes cellulaires qui contribuent aux élargissements cervicaux et lombaires de la moelle épinière. En plus de recevoir des facteurs neurotrophiques des muscles, les -MN sécrètent également un certain nombre de facteurs trophiques pour soutenir les fibres musculaires qu'ils innervent. Des niveaux réduits de facteurs trophiques contribuent à l'atrophie musculaire qui suit une lésion α-MN.
Connectivité
Comme les autres neurones, les motoneurones inférieurs ont à la fois des connexions afférentes (entrantes) et efférentes (sortantes). Les motoneurones alpha reçoivent des informations d'un certain nombre de sources, notamment les motoneurones supérieurs , les neurones sensoriels et les interneurones . La sortie principale des -MN est dirigée vers les fibres musculaires extrafusales . Cette connectivité afférente et efférente est nécessaire pour obtenir une activité musculaire coordonnée.
Entrée afférente
| origine UMN | Cible α-MN | Nom du secteur |
|---|---|---|
| Cortex cérébral | Tronc cérébral | Voie corticonucléaire |
| Cortex cérébral | Moelle épinière | Tractus corticospinal |
| Noyau rouge | Moelle épinière | Voie rubrospinale |
| Noyaux vestibulaires | Moelle épinière | Voie vestibulo-spinale |
| tectum du mésencéphale | Moelle épinière | Tractus tectospinal |
| Formation réticulaire | Moelle épinière | Tractus réticulo-spinal |
Neurones moteurs supérieurs (motoneurones) envoyer l' entrée en a-MNs par plusieurs voies, y compris (mais sans s'y limiter) le corticonucléaire , cortico et tracts rubrospinaux . Les faisceaux corticonucléaires et corticospinaux sont couramment rencontrés dans les études de connectivité des motoneurones supérieurs et inférieurs dans le contrôle des mouvements volontaires.
Le tractus corticonucléaire est ainsi nommé car il relie le cortex cérébral aux noyaux des nerfs crâniens . (Le tube corticonucléaire est aussi appelé le tractus cortico , en tant que cible dans le tronc cérébral, qui est medulla -is appelé archaïque la « ampoule ».) Il est par cette voie que les neurones moteurs supérieurs descendent du cortex et synapse sur les a-MNs du tronc cérébral. De même, les UMN du cortex cérébral contrôlent directement les -MN de la moelle épinière via les voies corticospinales latérale et ventrale .
L'apport sensoriel aux -MN est vaste et trouve son origine dans les organes tendineux de Golgi , les fuseaux musculaires , les mécanorécepteurs , les thermorécepteurs et d'autres neurones sensoriels de la périphérie. Ces connexions fournissent la structure des circuits neuronaux qui sous-tendent les réflexes . Il existe plusieurs types de circuits réflexes, dont le plus simple consiste en une seule synapse entre un neurone sensoriel et un -MNs. Le réflexe rotulien est un exemple d'un tel réflexe monosynaptique.
L' apport le plus important aux -MN provient des interneurones locaux , qui sont le type de neurone le plus nombreux dans la moelle épinière . Parmi leurs nombreux rôles, les interneurones se synapsent sur les -MN pour créer des circuits réflexes plus complexes. Un type d'interneurone est la cellule de Renshaw .
Sortie efférente
Les motoneurones alpha envoient des fibres qui se synapsent principalement sur les fibres musculaires extrafusales . D'autres fibres des -MNs se synapsent sur les cellules de Renshaw , c'est-à-dire des interneurones inhibiteurs qui se synapsent sur les -MN et limitent son activité afin de prévenir les dommages musculaires.
Signalisation
Comme les autres neurones, les -MN transmettent des signaux sous forme de potentiels d'action , des changements rapides d'activité électrique qui se propagent du corps cellulaire à l'extrémité de l' axone . Pour augmenter la vitesse de déplacement des potentiels d'action, les axones α-MN ont de grands diamètres et sont fortement myélinisés à la fois par les oligodendrocytes et les cellules de Schwann . Les oligodendrocytes myélinisent la partie de l'axone α-MN qui se trouve dans le système nerveux central (SNC), tandis que les cellules de Schwann myélinisent la partie qui se trouve dans le système nerveux périphérique (SNP). La transition entre le SNC et le SNP se produit au niveau de la pie-mère , la couche la plus interne et la plus délicate du tissu méningé entourant les composants du SNC.
L'axone d'un -MN se connecte à sa fibre musculaire extrafusale via une jonction neuromusculaire , un type spécialisé de synapse chimique qui diffère à la fois par sa structure et sa fonction des synapses chimiques qui relient les neurones les uns aux autres. Les deux types de synapses reposent sur des neurotransmetteurs pour transformer le signal électrique en un signal chimique et inversement. Ils diffèrent notamment par le fait que les synapses entre les neurones utilisent généralement le glutamate ou le GABA comme neurotransmetteurs, tandis que la jonction neuromusculaire utilise exclusivement l' acétylcholine . L'acétylcholine est détectée par les récepteurs nicotiniques de l'acétylcholine sur les fibres musculaires extrafusales, provoquant leur contraction.
Comme les autres motoneurones, les -MN sont nommés d'après les propriétés de leurs axones . Les motoneurones alpha ont des axones Aα , qui sont des fibres de gros calibre fortement myélinisées qui conduisent rapidement des potentiels d'action . En revanche, les neurones moteurs gamma ont des axones Aγ , qui sont des fibres minces et légèrement myélinisées qui conduisent moins rapidement.
Signification clinique
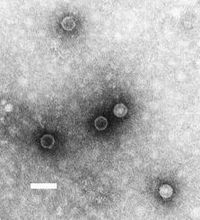
Les lésions des -MN sont le type le plus courant de lésion des motoneurones inférieurs . Les dommages peuvent être causés par un traumatisme , une ischémie et une infection , entre autres. De plus, certaines maladies sont associées à la perte sélective des -MN. Par exemple, la poliomyélite est causée par un virus qui cible et tue spécifiquement les motoneurones de la corne ventrale de la moelle épinière. La sclérose latérale amyotrope est également associée à la perte sélective des motoneurones.
La paralysie est l'un des effets les plus prononcés des dommages causés aux -MN. Étant donné que les -MN fournissent la seule innervation aux fibres musculaires extrafusales , la perte des α-MN rompt efficacement la connexion entre le tronc cérébral et la moelle épinière et les muscles qu'ils innervent. Sans cette connexion, le contrôle musculaire volontaire et involontaire (réflexe) est impossible. Le contrôle volontaire des muscles est perdu car les -MN transmettent les signaux volontaires des motoneurones supérieurs aux fibres musculaires. La perte de contrôle involontaire résulte de l'interruption des circuits réflexes tels que le réflexe tonique d' étirement . Une conséquence de l'interruption réflexe est que le tonus musculaire est réduit, entraînant une parésie flasque . Une autre conséquence est la dépression des réflexes tendineux profonds , provoquant une hyporéflexie .
La faiblesse musculaire et l' atrophie sont également des conséquences inévitables des lésions α-MN. Parce que la taille et la force des muscles sont liées à l'étendue de leur utilisation, les muscles dénervés sont sujets à l'atrophie. Une cause secondaire d'atrophie musculaire est que les muscles dénervés ne sont plus alimentés en facteurs trophiques par les α-MN qui les innervent. Les lésions des motoneurones alpha entraînent également des potentiels EMG anormaux (par exemple, des potentiels de fibrillation ) et des fasciculations , ces dernières étant des contractions musculaires spontanées et involontaires.
Les maladies qui altèrent la signalisation entre les -MN et les fibres musculaires extrafusales, à savoir les maladies de la jonction neuromusculaire, présentent des signes similaires à ceux de la maladie α-MN. Par exemple, la myasthénie grave est une maladie auto-immune qui empêche la signalisation à travers la jonction neuromusculaire , ce qui entraîne une dénervation fonctionnelle du muscle.
Voir également
Les références
- John A. Kiernan (2005). Le système nerveux humain de Barr : Un point de vue anatomique (8e éd.). Hagerstown, Maryland : Lippincott Williams & Wilkins. ISBN 0-7817-5154-3.
- Duane E. Haines (2004). Neuroanatomie : un atlas des structures, des sections et des systèmes (6e éd.). Hagerstown, Maryland : Lippincott Williams & Wilkins. ISBN 0-7817-4677-9.
