Nitrure d'aluminium - Aluminium nitride

|
|
|
|
| Des noms | |
|---|---|
| Autres noms
Nitrure d'aluminium
|
|
| Identifiants | |
|
Modèle 3D ( JSmol )
|
|
| ChEBI | |
| ChemSpider | |
| Carte d'information de l'ECHA |
100.041.931 |
| Numéro CE | |
| 13611 | |
|
CID PubChem
|
|
| Numéro RTECS | |
| UNII | |
|
Tableau de bord CompTox ( EPA )
|
|
|
|
|
|
| Propriétés | |
| Al N | |
| Masse molaire | 40,989 g/mol |
| Apparence | solide blanc à jaune pâle |
| Densité | 3,255 g / cm 3 |
| Point de fusion | 2 500 °C (4 530 °F; 2 770 K) |
| hydrolyse (poudre), insoluble (monocristallin) | |
| Solubilité | insoluble, sujet à l'hydrolyse dans les solutions aqueuses de bases et d'acides |
| Bande interdite | 6,015 eV ( direct ) |
| Mobilité électronique | ~300 cm 2 /(V·s) |
| Conductivité thermique | 321 W/(m·K) |
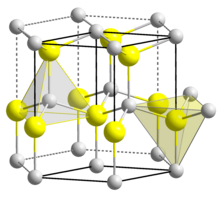
| Structure | |
| Wurtzite | |
| C 6v 4 - P 6 3 mc , n° 186, hP4 | |
|
a = 0,31117 nm, c = 0,49788 nm
|
|
|
Unités de formule ( Z )
|
2 |
| tétraédrique | |
| Thermochimie | |
|
Capacité calorifique ( C )
|
30,1 J/(mol·K) |
|
Entropie molaire standard ( S |
20,2 J/(mol·K) |
|
Std enthalpie de
formation (Δ f H ⦵ 298 ) |
−318,0 kJ/mol |
|
Énergie libre de Gibbs (Δ f G ˚)
|
-287,0 kJ/mol |
| Dangers | |
| Pictogrammes SGH |
  
|
| Mention d'avertissement SGH | Avertissement |
| H315 , H319 , H335 , H373 , H411 | |
| P260 , P261 , P264 , P271 , P280 , P301+330+331 , P302+352 , P303+361+353 , P304+340 , P305+351+338 , P310 , P312 , P321 , P332+313 , P337+313 , P362 , P363 , P403 + 233 , P405 , P501 | |
| NFPA 704 (diamant de feu) | |
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Références de l'infobox | |
Le nitrure d'aluminium ( Al N ) est un nitrure solide d' aluminium . Il a une conductivité thermique élevée allant jusqu'à 321 W/(m·K) et est un isolant électrique. Sa phase wurtzite (w-AlN) a une bande interdite d'environ 6 eV à température ambiante et a une application potentielle en optoélectronique fonctionnant à des fréquences ultraviolettes profondes .
Histoire et propriétés physiques
AlN a été synthétisé pour la première fois en 1877.
AlN, à l'état pur (non dopé) présente une conductivité électrique de 10 -11 -10 -13 Ω -1 ⋅cm -1 , passant à 10 -5 -10 -6 Ω -1 ⋅cm -1 lorsque dopé. Le claquage électrique se produit à un champ de 1,2 à 1,8 × 10 5 V/mm ( rigidité diélectrique ).
Il est prédit que la phase de mélange de zinc cubique d'AlN (zb-AlN) peut présenter une supraconductivité à haute pression.
AlN a une conductivité thermique élevée , le monocristal d'AlN cultivé par MOCVD de haute qualité a une conductivité thermique intrinsèque de 321 W/(m·K), compatible avec un calcul de premier principe. Pour une céramique électriquement isolante , il est de 70 à 210 W/(m·K) pour les matériaux polycristallins, et jusqu'à 285 W/(m·K) pour les monocristaux).
Stabilité et propriétés chimiques
Le nitrure d'aluminium est stable à haute température dans des atmosphères inertes et fond à environ 2200 °C. Dans le vide, AlN se décompose à ~ 1800 °C. Dans l'air, l'oxydation de surface se produit au-dessus de 700 °C, et même à température ambiante, des couches d'oxyde de surface de 5 à 10 nm d'épaisseur ont été détectées. Cette couche d'oxyde protège le matériau jusqu'à 1370 °C. Au-dessus de cette température, une oxydation en masse se produit. Le nitrure d'aluminium est stable dans des atmosphères d'hydrogène et de dioxyde de carbone jusqu'à 980 °C.
Le matériau se dissout lentement dans les acides minéraux par attaque de la limite des grains et dans les alcalis forts par attaque sur les grains de nitrure d'aluminium. Le matériau s'hydrolyse lentement dans l'eau. Le nitrure d'aluminium résiste aux attaques de la plupart des sels fondus, y compris les chlorures et la cryolite .
Le nitrure d'aluminium peut être modelé avec une gravure ionique réactive à base de Cl 2 .
Fabrication
L'AIN est synthétisé par la réduction carbothermique de l'oxyde d'aluminium en présence d'azote ou d'ammoniac gazeux ou par nitruration directe de l'aluminium. L'utilisation d' auxiliaires de frittage , tels que Y 2 O 3 ou CaO, et le pressage à chaud sont nécessaires pour produire un matériau dense de qualité technique.
Applications
Épitaxiale développée film mince en nitrure d'aluminium cristallin est utilisé pour ondes acoustiques de surface de capteurs (BP) déposées sur silicium plaquettes en raison de AlN de piézoélectriques propriétés. Une application est un filtre RF , largement utilisé dans les téléphones mobiles, qui est appelé résonateur acoustique en vrac à couche mince (FBAR). Il s'agit d'un dispositif MEMS qui utilise du nitrure d'aluminium pris en sandwich entre deux couches métalliques.
AlN est également utilisé pour construire des transducteurs à ultrasons piézoélectriques micro-usinés, qui émettent et reçoivent des ultrasons et qui peuvent être utilisés pour la télémétrie dans l'air sur des distances allant jusqu'à un mètre.
Des méthodes de métallisation sont disponibles pour permettre à l'AlN d'être utilisé dans des applications électroniques similaires à celles de l'alumine et de l'oxyde de béryllium . Les nanotubes d'AlN en tant que nanotubes inorganiques quasi-unidimensionnels, qui sont isoélectroniques avec les nanotubes de carbone, ont été suggérés comme capteurs chimiques pour les gaz toxiques.
Actuellement, de nombreuses recherches sont en cours pour développer des diodes électroluminescentes fonctionnant dans l'ultraviolet en utilisant des semi-conducteurs à base de nitrure de gallium et, en utilisant l'alliage d' aluminium et de nitrure de gallium , des longueurs d'onde aussi courtes que 250 nm ont été atteintes. En 2006, une émission de LED AlN inefficace à 210 nm a été signalée.
Parmi les applications d'AlN figurent
- opto-électronique,
- couches diélectriques dans des supports de stockage optiques,
- substrats électroniques, supports de puces où une conductivité thermique élevée est essentielle,
- applications militaires,
- comme creuset pour faire croître des cristaux d' arséniure de gallium ,
- fabrication d' acier et de semi - conducteurs .
Voir également
- Nitrure de bore
- Phosphure d'aluminium
- Nitrure d'indium
- Oxynitrure d'aluminium
- Nitrure d'aluminium titane , TiAlN ou AlTiN
Les références
Sources citées
- Haynes, William M., éd. (2016). CRC Handbook of Chemistry and Physics (97e éd.). CRC Appuyez sur . p. 4.45. ISBN 9781498754293.
|
NH 3 N 2 H 4 |
Il (N 2 ) 11 | ||||||||||||||||
| Li 3 N | Soyez 3 N 2 | NE |
-C 3 N 4 g-C 3 N 4 C x N y |
N 2 | N x O y | NF 3 | Ne | ||||||||||
| Non 3 N | Mg 3 N 2 | AIN | Si 3 N 4 |
PN P 3 N 5 |
S x N y SN S 4 N 4 |
NCl 3 | Ar | ||||||||||
| K 3 N | Ca 3 N 2 | ScN | Étain | VN |
CrN Cr 2 N |
Mn x N y | Fe x N y | CoN | Ni 3 N | CuN | Zn 3 N 2 | GaN | Ge 3 N 4 | Comme | Se | NBr 3 | Kr |
| Rb | Sr 3 N 2 | ON | ZrN | NbN | -Mo 2 N | Tc | Ru | Rhésus | PdN | Ag 3 N | CdN | Auberge | Sn | Sb | Te | NI 3 | Xe |
| Cs | Ba 3 N 2 | Hf 3 N 4 | Bronzer | WN | Ré | Os | Je | pt | Au | Hg 3 N 2 | TlN | Pb | Poubelle | Pô | À | Rn | |
| Fr | Ra 3 N 2 | Rf | DB | Sg | Bh | Hs | Mont | DS | Rg | Cn | Nh | Fl | Mc | Niv | Ts | Og | |
| ↓ | |||||||||||||||||
| La | CeN | PrN | nd | après-midi | SM | UE | GdN | To | Dy | Ho | Euh | Tm | Yb | Lu | |||
| c.a. | E | Pennsylvanie | U 2 N 3 | Np | Pu | Un m | Cm | Noir | Cf. | Es | FM | Maryland | Non | G / D | |||

