Chlorure d'américium(III) - Americium(III) chloride
|
|
| Noms | |
|---|---|
|
Nom IUPAC
Chlorure d'américium(III)
|
|
|
Nom IUPAC systématique
Chlorure d'américium (3+) |
|
| Autres noms
Chlorure d'
américium Trichlorure d'américium |
|
| Identifiants | |
|
Modèle 3D ( JSmol )
|
|
| ChemSpider | |
|
CID PubChem
|
|
|
|
|
|
| Propriétés | |
| Suis Cl 3 | |
| Masse molaire | 349 g·mol -1 |
| Apparence | Cristaux rouge clair opaques |
| Densité | 5,87 g cm -3 |
| Point de fusion | 715 °C (1 319 °F; 988 K) |
| Point d'ébullition | 850 °C (1 560 °F ; 1 120 K) |
| Structure | |
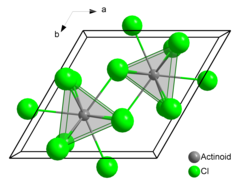
| hexagonale ( type UCl 3 ), hP8 | |
| P6 3 /m, n° 176 | |
| Prismatique trigonale tricapped (neuf coordonnées) |
|
| Composés apparentés | |
|
Autres cations
|
Chlorure d'europium(III) |
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Références de l'infobox | |
Le chlorure d'américium (III) ou trichlorure d'américium est le composé chimique composé d' américium et de chlore de formule AmCl 3 . Il forme des cristaux hexagonaux roses . A l'état solide, chaque atome d'américium a neuf atomes de chlore comme voisins proches, à peu près à la même distance, dans une configuration prismatique trigonale à trois coiffes.
L'hexahydrate a une structure cristalline monocline avec : a = 970,2 pm, b = 656,7 pm et c = 800,9 pm ; = 93° 37'; groupe d'espaces : P 2/ n .
Réactions
Une méthode d' électroraffinage du chlorure d'américium (III) a été étudiée pour séparer des mélanges d' actinides , car l' énergie libre standard de Gibbs de formation du chlorure d'américium (III) est très différente du reste des chlorures d'actinides. Cela peut être utilisé pour éliminer l'américium du plutonium en faisant fondre le mélange brut avec des sels tels que le chlorure de sodium .
Les références
