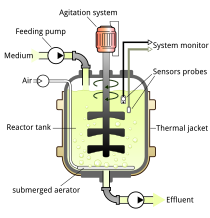
Bioréacteur - Bioreactor
Un bioréacteur fait référence à tout dispositif ou système fabriqué qui prend en charge un environnement biologiquement actif. Dans un cas, un bioréacteur est un récipient dans lequel un processus chimique est effectué qui implique des organismes ou des substances biochimiquement actives dérivées de tels organismes. Ce processus peut être aérobie ou anaérobie . Ces bioréacteurs sont généralement cylindriques, allant de litres à mètres cubes, et sont souvent fabriqués en acier inoxydable . Il peut également faire référence à un dispositif ou un système conçu pour cultiver des cellules ou des tissus dans le cadre de la culture cellulaire . Ces dispositifs sont en cours de développement pour une utilisation en ingénierie tissulaire ou en ingénierie biochimique / bioprocédés .
Sur la base du mode de fonctionnement, un bioréacteur peut être classé comme batch , fed batch ou continu (par exemple un modèle de réacteur à cuve agitée en continu ). Un exemple de bioréacteur continu est le chémostat .
Les organismes poussant dans des bioréacteurs peuvent être immergés dans un milieu liquide ou peuvent être attachés à la surface d'un milieu solide. Les cultures immergées peuvent être suspendues ou immobilisées. Les bioréacteurs en suspension peuvent utiliser une plus grande variété d'organismes, car des surfaces de fixation spéciales ne sont pas nécessaires et peuvent fonctionner à une échelle beaucoup plus grande que les cultures immobilisées. Cependant, dans un procédé fonctionnant en continu, les organismes seront retirés du réacteur avec l'effluent. L'immobilisation est un terme général décrivant une grande variété de méthodes pour la fixation ou le piégeage de cellules ou de particules. Il peut être appliqué à pratiquement tous les types de biocatalyse, y compris les enzymes, les organites cellulaires, les cellules animales et végétales. L'immobilisation est utile pour les processus fonctionnant en continu, car les organismes ne seront pas éliminés avec l'effluent du réacteur, mais est limité en échelle car les microbes ne sont présents que sur les surfaces de la cuve.
Les bioréacteurs à cellules immobilisées à grande échelle sont :
- milieu mobile, également connu sous le nom de réacteur à biofilm à lit mobile (MBBR)
- lit emballé
- lit fibreux
- membrane
Concevoir
La conception de bioréacteurs est une tâche d'ingénierie relativement complexe, qui est étudiée dans la discipline de l' ingénierie biochimique /des bioprocédés . Dans des conditions optimales, les micro-organismes ou les cellules sont capables de remplir leur fonction souhaitée avec une production limitée d'impuretés. Les conditions environnementales à l'intérieur du bioréacteur, telles que la température, les concentrations de nutriments, le pH et les gaz dissous (en particulier l'oxygène pour les fermentations aérobies) affectent la croissance et la productivité des organismes. La température du milieu de fermentation est maintenue par une chemise de refroidissement, des serpentins ou les deux. Les fermentations particulièrement exothermiques peuvent nécessiter l'utilisation d'échangeurs de chaleur externes. Les nutriments peuvent être ajoutés en continu au fermenteur, comme dans un système fed-batch, ou peuvent être chargés dans le réacteur au début de la fermentation. Le pH du milieu est mesuré et ajusté avec de petites quantités d'acide ou de base, selon la fermentation. Pour les fermentations aérobies (et certaines anaérobies), des gaz réactifs (en particulier de l'oxygène) doivent être ajoutés à la fermentation. L'oxygène étant relativement insoluble dans l'eau (la base de presque tous les milieux de fermentation), de l'air (ou de l'oxygène purifié) doit être ajouté en continu. L'action des bulles qui montent aide à mélanger le milieu de fermentation et également « bandes » sur les gaz résiduaires tels que le dioxyde de carbone. En pratique, les bioréacteurs sont souvent pressurisés ; cela augmente la solubilité de l'oxygène dans l'eau. Dans un processus aérobie, le transfert optimal d'oxygène est parfois l'étape limitant la vitesse. L'oxygène est peu soluble dans l'eau - encore moins dans les bouillons de fermentation chauds - et est relativement rare dans l' air (20,95 %). Le transfert d'oxygène est généralement facilité par l'agitation, qui est également nécessaire pour mélanger les nutriments et maintenir la fermentation homogène. Les agitateurs à dispersion de gaz sont utilisés pour briser les bulles d'air et les faire circuler dans le récipient.
L'encrassement peut nuire à l'efficacité globale du bioréacteur, en particulier des échangeurs de chaleur . Pour l'éviter, le bioréacteur doit être facilement nettoyé. Les surfaces intérieures sont généralement en acier inoxydable pour un nettoyage et un assainissement faciles. En règle générale, les bioréacteurs sont nettoyés entre les lots ou sont conçus pour réduire autant que possible l'encrassement lorsqu'ils fonctionnent en continu. Le transfert de chaleur est une partie importante de la conception d'un bioréacteur ; les petits récipients peuvent être refroidis avec une chemise de refroidissement, mais les grands récipients peuvent nécessiter des serpentins ou un échangeur de chaleur externe.
Les types
Photobioréacteur
Un photobioréacteur (PBR) est un bioréacteur qui incorpore un certain type de source lumineuse (qui peut être la lumière naturelle du soleil ou un éclairage artificiel). Pratiquement n'importe quel conteneur translucide pourrait être appelé un PBR, mais le terme est plus couramment utilisé pour définir un système fermé, par opposition à un réservoir de stockage ouvert ou à un étang . Les photobioréacteurs sont utilisés pour cultiver de petits organismes phototrophes tels que les cyanobactéries , les algues ou les mousses . Ces organismes utilisent la lumière par photosynthèse comme source d' énergie et n'ont pas besoin de sucres ou de lipides comme source d'énergie. Par conséquent, le risque de contamination par d'autres organismes comme des bactéries ou des champignons est plus faible dans les photobioréacteurs par rapport aux bioréacteurs pour organismes hétérotrophes .
Traitement des eaux usées
Le traitement conventionnel des eaux usées utilise des bioréacteurs pour entreprendre les principaux processus de purification. Dans certains de ces systèmes, un milieu chimiquement inerte avec une très grande surface spécifique est fourni comme substrat pour la croissance du film biologique. La séparation du film biologique en excès a lieu dans des bassins de décantation ou des cyclones. Dans d'autres systèmes, les aérateurs fournissent de l'oxygène aux eaux usées et au biote pour créer des boues activées dans lesquelles le composant biologique est librement mélangé dans la liqueur en "flocs". Dans ces processus, la demande biochimique en oxygène (DBO) du liquide est suffisamment réduite pour que l'eau contaminée puisse être réutilisée. Les biosolides peuvent être collectés pour un traitement ultérieur, ou séchés et utilisés comme engrais. Une version extrêmement simple d'un bioréacteur d'eaux usées est une fosse septique dans laquelle les eaux usées sont laissées in situ, avec ou sans milieu supplémentaire pour abriter les bactéries. Dans ce cas, la boue biologique elle-même est l'hôte principal de la bactérie.
Bioréacteurs pour tissus spécialisés
De nombreuses cellules et tissus, en particulier ceux de mammifères, doivent avoir une surface ou un autre support structurel pour se développer, et les environnements agités sont souvent destructeurs pour ces types de cellules et ces tissus. Les organismes supérieurs, étant auxotrophes , nécessitent également des milieux de croissance hautement spécialisés. Cela pose un défi lorsque l'objectif est de cultiver de plus grandes quantités de cellules à des fins de production thérapeutique, et une conception très différente est nécessaire par rapport aux bioréacteurs industriels utilisés pour la croissance de systèmes d'expression de protéines tels que la levure et les bactéries.
De nombreux groupes de recherche ont développé de nouveaux bioréacteurs pour la croissance de tissus et de cellules spécialisés sur un échafaudage structurel, dans le but de recréer des structures tissulaires semblables à des organes in vitro . Parmi ceux-ci, citons les bioréacteurs tissulaires capables de développer des tissus cardiaques, des tissus musculaires squelettiques, des ligaments, des modèles de tissus cancéreux et autres. Actuellement, la production à grande échelle de ces bioréacteurs spécialisés à usage industriel reste un défi et constitue un domaine de recherche actif.
Pour plus d'informations sur la culture de tissus artificiels, voir ingénierie tissulaire .
La modélisation
Les modèles mathématiques constituent un outil important dans diverses applications de bioréacteurs, notamment le traitement des eaux usées. Ces modèles sont utiles pour planifier des stratégies de contrôle de processus efficaces et prédire les performances futures de l'usine. De plus, ces modèles sont bénéfiques dans les domaines de l'éducation et de la recherche.
Les bioréacteurs sont généralement utilisés dans les industries concernées par l'alimentation, les boissons et les produits pharmaceutiques. L'émergence du génie biochimique est d'origine récente. Le traitement de matériaux biologiques à l'aide d'agents biologiques tels que des cellules, des enzymes ou des anticorps sont les principaux piliers du génie biochimique. Les applications du génie biochimique couvrent les principaux domaines de la civilisation tels que l'agriculture, l'alimentation et les soins de santé, la récupération des ressources et la chimie fine.
Jusqu'à présent, les industries associées à la biotechnologie ont pris du retard par rapport aux autres industries dans la mise en œuvre de la maîtrise des procédés et des stratégies d'optimisation. Un inconvénient majeur du contrôle des processus biotechnologiques est le problème de la mesure des paramètres physiques et biochimiques clés.
Étapes opérationnelles d'un bioprocédé
Un bioprocédé est composé principalement de trois étapes - traitement en amont, bioréaction et traitement en aval - pour convertir la matière première en produit fini.
La matière première peut être d'origine biologique ou non biologique. Il est d'abord converti en une forme plus appropriée pour le traitement. Cela se fait dans une étape de traitement en amont qui implique l'hydrolyse chimique, la préparation du milieu liquide, la séparation des particules, la purification de l'air et de nombreuses autres opérations préparatoires.
Après l'étape de traitement en amont, la charge résultante est transférée vers une ou plusieurs étapes de bioréaction. Les réacteurs biochimiques ou bioréacteurs forment la base de l'étape de bioréaction. Cette étape consiste principalement en trois opérations, à savoir la production de biomasse , la biosynthèse des métabolites et la biotransformation.
Enfin, le matériau produit dans le bioréacteur doit être davantage traité dans la section en aval pour le convertir en une forme plus utile. Le processus en aval consiste principalement en des opérations de séparation physique qui incluent la séparation solide-liquide, l' adsorption , l' extraction liquide-liquide , la distillation , le séchage, etc.
Caractéristiques
Un bioréacteur typique se compose des éléments suivants :
Agitateur - Utilisé pour le mélange du contenu du réacteur qui maintient les cellules dans des conditions parfaitement homogènes pour un meilleur transport des nutriments et de l'oxygène vers le ou les produits souhaités.
Déflecteur - Utilisé pour briser la formation de vortex dans le navire, ce qui est généralement très indésirable car il modifie le centre de gravité du système et consomme de l'énergie supplémentaire.
Sparger - Dans le processus de culture aérobie, le but du sparger est de fournir suffisamment d'oxygène aux cellules en croissance.
Veste - La veste fournit la zone annulaire pour la circulation d'une température constante de l'eau qui maintient la température du bioréacteur à une valeur constante.
Voir également
- Test ATP
- Génie biochimique
- Biocarburant à partir d'algues
- Production biologique d'hydrogène (algues)
- Bioprocesseur
- Décharge de bioréacteur
- Biotechnologie
- Culture de cellules
- Chémostat
- Digesteur
- Réacteur électro-biochimique (EBR)
- Culture de racines velues
- Histoire de la biotechnologie
- Bioréacteur à fibres creuses
- Enzyme immobilisée
- Biotechnologie industrielle
- Réacteur à biofilm à lit mobile
- Fosse septique
- Bioréacteur à usage unique
- Création de tissus
Les références
- ^ IUPAC , Compendium de terminologie chimique , 2e éd. (le "Livre d'or") (1997). Version corrigée en ligne : (2006–) " bioréacteur ". doi : 10.1351/goldbook.B00662
- ^ http://www.eolss.net/Sample-Chapters/C17/E6-58-04-15.pdf
- ^ Lopez, Asunción; Lázaro, Nuria; Marqués, Ana M. (septembre 1997). « La technique d'interphase : une méthode simple d'immobilisation cellulaire dans des billes de gel ». Journal des méthodes microbiologiques . 30 (3) : 231-234. doi : 10.1016/S0167-7012 (97) 00071-7 .
- ^ Peinado, Rafael A.; Moreno, Juan J.; Villalba, José M.; González-Reyes, José A.; Ortega, José M.; Mauricio, Juan C. (décembre 2006). « Biocapsules de levure : une nouvelle méthode d'immobilisation et leurs applications ». Technologie enzymatique et microbienne . 40 (1) : 79-84. doi : 10.1016/j.enzmictec.2005.10.040 .
- ^ Decker, Eva L.; Reski, Ralf (14 août 2007). « Réalisations actuelles dans la production de produits biopharmaceutiques complexes avec des bioréacteurs à mousse ». Ingénierie des bioprocédés et des biosystèmes . 31 (1) : 3-9. doi : 10.1007/s00449-007-0151-y . PMID 17701058 .
- ^ Bursac, N.; Papadaki, M. ; Cohen, RJ; Schoen, FJ; Eisenberg, SR ; Carrier, R.; Vunjak-Novakovic, G.; Libéré, LE (1er août 1999). « Ingénierie tissulaire musculaire cardiaque : vers un modèle in vitro pour les études électrophysiologiques ». Journal américain de physiologie. Physiologie cardiaque et circulatoire . 277 (2) : H433–H444. doi : 10.1152/ajpheart.1999.277.2.h433 . PMID 10444466 .
- ^ Transporteur, Rebecca L.; Papadaki, Maria ; Rupnick, Maria ; Schoen, Frederick J.; Bursac, Nenad ; Langer, Robert; Libéré, Lisa E. ; Vunjak-Novakovic, Gordana (5 septembre 1999). « Ingénierie tissulaire cardiaque : ensemencement cellulaire, paramètres de culture et caractérisation de la construction tissulaire ». Biotechnologie et bio-ingénierie . 64 (5) : 580-589. doi : 10.1002/(SICI)1097-0290(19990905)64:5<580::AID-BIT8>3.0.CO;2-X .
- ^ Heher, Philipp; Maleiner, Babette ; Prüller, Johanna; Teuschl, Andreas Herbert; Kollmitzer, Josef ; Monforte, Xavier ; Wolbank, Susanne; Redl, Heinz; Rünzler, Dominik ; Fuchs, Christiane (septembre 2015). « Un nouveau bioréacteur pour la génération de constructions de type muscle squelettique 3D hautement alignées grâce à l'orientation de la fibrine via l'application d'une contrainte statique ». Acta Biomaterialia . 24 : 251-265. doi : 10.1016/j.actbio.2015.06.033 . PMID 26141153 .
- ^ Carlsson, Bengt (24 mars 2009). « Une introduction à la modélisation des bioréacteurs » (PDF) .
- ^ Rosser, J.; Thomas, DJ (2018-01-01), Thomas, Daniel J.; Jessop, Zita M. ; Whitaker, Iain S. (eds.), "10 - Processus de bioréacteur pour la maturation de tissus bio-imprimés en 3D" , 3D Bioprinting for Reconstructive Surgery , Woodhead Publishing, pp. 191-215, ISBN 978-0-08-101103-4, récupéré le 2020-12-14
- ^ Jana, AMIYA K. (2011). MODÉLISATION DE PROCESSUS CHIMIQUES ET SIMULATION PAR ORDINATEUR . PHI Apprentissage Pvt. Ltd.
- ^ "Bioréacteur-Bases" .
Lectures complémentaires
- Pauline M Doran, Principes d'ingénierie des bioprocédés, Elsevier, 2e éd., 2013 ISBN 978-0-12-220851-5
- La société de biotechnologie, Medicago Inc. , utilise des plantes pour faire pousser des particules de type virus pour un éventuel vaccin COVID-19