Trioxyde de bore - Boron trioxide
![Structure cristalline de B2O3 [1]](https://upload.wikimedia.org/wikipedia/commons/thumb/d/d9/B2O3powder.JPG/220px-B2O3powder.JPG)
|
|
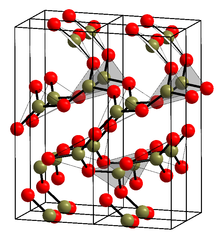
|
|
| Noms | |
|---|---|
| Autres noms
oxyde de bore, trioxyde de dibore, sesquioxyde de bore, oxyde borique, boria
Anhydride d'acide borique |
|
| Identifiants | |
|
Modèle 3D ( JSmol )
|
|
| ChEBI | |
| ChemSpider | |
| Carte Info ECHA |
100.013.751 |
| Numéro CE | |
| 11108 | |
|
PubChem CID
|
|
| Numéro RTECS | |
| UNII | |
|
Tableau de bord CompTox ( EPA )
|
|
|
|
|
|
| Propriétés | |
| B 2 O 3 | |
| Masse molaire | 69,6182 g / mol |
| Apparence | blanc, solide vitreux |
| Densité | 2,460 g / cm 3 , liquide; 2,55 g / cm 3 , trigonal; |
| Point de fusion | 450 ° C (842 ° F; 723 K) (trigonal) 510 ° C (tétraédrique) |
| Point d'ébullition | 1860 ° C (3380 ° F; 2130 K), sublime à 1500 ° C |
| 1,1 g / 100 ml (10 ° C) 3,3 g / 100 ml (20 ° C) 15,7 g / 100 ml (100 ° C) |
|
| Solubilité | partiellement soluble dans le méthanol |
| Acidité (p K a ) | ~ 4 |
| -39,0 · 10 −6 cm 3 / mol | |
| Thermochimie | |
|
Capacité thermique ( C )
|
66,9 J / mol K |
|
Entropie molaire std ( S |
80,8 J / mol K |
| -1254 kJ / mol | |
|
Énergie libre de Gibbs (Δ f G ˚)
|
-832 kJ / mol |
| Dangers | |
| Principaux dangers | Irritant |
| Fiche de données de sécurité | Voir: page de données |
| Pictogrammes SGH |

|
| Mot de signalisation SGH | Danger |
| H360FD | |
| P201 , P202 , P281 , P308 + 313 , P405 , P501 | |
| NFPA 704 (diamant de feu) | |
| point de rupture | incombustible |
| Dose ou concentration létale (DL, LC): | |
|
DL 50 ( dose médiane )
|
3163 mg / kg (oral, souris) |
| NIOSH (limites d'exposition pour la santé aux États-Unis): | |
|
PEL (autorisé)
|
TWA 15 mg / m 3 |
|
REL (recommandé)
|
TWA 10 mg / m 3 |
|
IDLH (danger immédiat)
|
2 000 mg / m 3 |
| Page de données supplémentaires | |
|
Indice de réfraction ( n ), constante diélectrique (ε r ), etc. |
|
|
Données thermodynamiques |
Comportement de phase solide – liquide – gaz |
| UV , IR , RMN , MS | |
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Références Infobox | |
Le trioxyde de bore (ou trioxyde de dibore ) est l'un des oxydes de bore . C'est un solide blanc vitreux de formule B 2 O 3 . Il se trouve presque toujours sous la forme vitreuse (amorphe); cependant, il peut être cristallisé après un recuit étendu (c'est-à-dire sous une chaleur prolongée).
On pense que l'oxyde de bore vitreux (gB 2 O 3 ) est composé de cycles de boroxol qui sont des cycles à six chaînons composés de bore alterné à 3 coordonnées et d'oxygène à 2 coordonnées. En raison de la difficulté de construire des modèles désordonnés à la densité correcte avec de nombreux anneaux de boroxol , ce point de vue était initialement controversé, mais de tels modèles ont été récemment construits et présentent des propriétés en excellent accord avec l'expérience. Il est maintenant reconnu, à partir d' études théoriques et expérimentales, que la fraction d'atomes de bore appartenant à des cycles de boroxol en B vitreux 2 O 3 se situe entre 0,73 et 0,83, avec 0,75 ( 3 / 4 ) correspondant à un rapport 1: 1 entre unités annulaires et non annulaires. Le nombre d'anneaux boroxol se désintègre à l'état liquide avec l'augmentation de la température.
La forme cristalline (α-B 2 O 3 ) (voir structure dans l'infobox) est exclusivement composée de triangles BO 3 . Ce réseau trigonal de type quartz subit une transformation de type coésite en β-B 2 O 3 monoclinique à plusieurs gigapascals (9,5 GPa).
Préparation
Le trioxyde de bore est produit en traitant le borax avec de l'acide sulfurique dans un four de fusion . A des températures supérieures à 750 ° C, la couche d'oxyde de bore fondu se sépare du sulfate de sodium . Il est ensuite décanté, refroidi et obtenu avec une pureté de 96 à 97%.
Une autre méthode consiste à chauffer l'acide borique au-dessus de ~ 300 ° C. L'acide borique se décomposera initialement en vapeur (H 2 O (g) ) et acide métaborique (HBO 2 ) à environ 170 ° C, et un chauffage supplémentaire au-dessus de 300 ° C produira plus de vapeur et de trioxyde de dibore. Les réactions sont:
- H 3 BO 3 → HBO 2 + H 2 O
- 2 HBO 2 → B 2 O 3 + H 2 O
L'acide borique se transforme en B 2 O 3 microcristallin anhydre dans un lit fluidisé chauffé. La vitesse de chauffage soigneusement contrôlée évite le gommage lorsque l'eau évolue. L'oxyde de bore fondu attaque les silicates. Les tubes graphités en interne par décomposition thermique de l'acétylène sont passivés.
La cristallisation de α-B 2 O 3 fondu à pression ambiante est fortement défavorisée cinétiquement (comparer les densités de liquide et de cristal). Les conditions de seuil pour la cristallisation du solide amorphe sont de 10 kbar et ~ 200 ° C. Sa structure cristalline proposée dans les groupes spatiaux énantiomorphes P3 1 (# 144); P3 2 (# 145) (par exemple, y-glycine) a été révisé en groupes d'espace énantiomorphique P3 1 21 (# 152); P3 2 21 (# 154) (par exemple, quartz α).
L'oxyde de bore se formera également lorsque le diborane (B 2 H 6 ) réagira avec l'oxygène de l'air ou des traces d'humidité:
- 2B 2 H 6 (g) + 3O 2 (g) → 2B 2 O 3 (s) + 6H 2 (g)
- B 2 H 6 (g) + 3H 2 O (g) → B 2 O 3 (s) + 6H 2 (g)
Applications
- Agent de flux pour verre et émaux
- Matière de départ pour la synthèse d'autres composés de bore tels que le carbure de bore
- Un additif utilisé dans les fibres de verre ( fibres optiques )
- Composant utilisé dans la production de verre borosilicaté
- La couche de coiffage inerte dans le procédé Czochralski d'encapsulation liquide pour la production de monocristal d' arséniure de gallium
- En tant que catalyseur acide en synthèse organique

