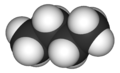
Butane - Butane
|
|
|||
|
|
|||
| Noms | |||
|---|---|---|---|
|
Nom IUPAC préféré
Butane |
|||
|
Nom IUPAC systématique
Tétracarbane (jamais recommandé) |
|||
| Autres noms
hydrure de butyle; Quartane; Réfrigérant 3-11-0
|
|||
| Identifiants | |||
|
Modèle 3D ( JSmol )
|
|||
| 969129 | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| Carte d'information de l'ECHA |
100.003.136 |
||
| Numéro CE | |||
| numéro E | E943a (agents de glaçage, ...) | ||
| 1148 | |||
| KEGG | |||
| Engrener | butane | ||
|
CID PubChem
|
|||
| Numéro RTECS | |||
| UNII | |||
| Numéro ONU | 1011 | ||
|
Tableau de bord CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriétés | |||
| C 4 H 10 | |||
| Masse molaire | 58,124 g·mol -1 | ||
| Apparence | Gaz incolore | ||
| Odeur | De type essence ou gaz naturel | ||
| Densité | 2,48 kg/m 3 (à 15 °C (59 °F)) | ||
| Point de fusion | -140 à -134 °C ; -220 à -209 °F ; 133 à 139 K | ||
| Point d'ébullition | -1 à 1 °C ; 30 à 34 °F; 272 à 274 K | ||
| 61 mg/L (à 20 °C (68 °F)) | |||
| log P | 2.745 | ||
| La pression de vapeur | ~170 kPa à 283 K | ||
|
Constante de la loi de Henry ( k H ) |
11 nmoles Pa -1 kg -1 | ||
| Acide conjugué | butane | ||
| −57,4·10 −6 cm 3 /mol | |||
| Thermochimie | |||
|
Capacité calorifique ( C )
|
98,49 J/(K·mol) | ||
|
Std enthalpie de
formation (Δ f H ⦵ 298 ) |
−126,3–−124,9 kJ/mol | ||
| −2.8781–−2.8769 MJ/mol | |||
| Dangers | |||
| Fiche de données de sécurité | Voir : page de données | ||
| Pictogrammes SGH |
 
|
||
| Mention d'avertissement SGH | Danger | ||
| H220 | |||
| P210 | |||
| NFPA 704 (diamant de feu) | |||
| point de rupture | −60 °C (−76 °F; 213 K) | ||
| 405 °C (761 °F; 678 K) | |||
| Limites d'explosivité | 1,8-8,4% | ||
| NIOSH (limites d'exposition pour la santé aux États-Unis) : | |||
|
PEL (Autorisé)
|
rien | ||
|
REL (recommandé)
|
TWA 800 ppm (1900 mg/m 3 ) | ||
|
IDLH (Danger immédiat)
|
1600 ppm | ||
| Composés apparentés | |||
|
Alcanes apparentés
|
|||
|
Composés apparentés
|
Perfluorobutane | ||
| Page de données supplémentaires | |||
|
Indice de réfraction ( n ), Constante diélectrique (ε r ), etc. |
|||
|
Données thermodynamiques |
Comportement des phases solide-liquide-gaz |
||
| UV , IR , RMN , MS | |||
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 °C [77 °F], 100 kPa). |
|||
|
|
|||
| Références de l'infobox | |||
Butane ( / b ju t eɪ n / ) ou n - butane est un alcane ayant la formule C 4 H 10 . Le butane est un gaz à température ambiante et à pression atmosphérique. Butane est un très inflammable, incolore, facilement liquéfié gaz qui se vaporise rapidement à la température ambiante. Le nom butane vient des racines but- (de l'acide butyrique , du nom du mot grec pour beurre) et -ane . Il a été découvert par le chimiste Edward Frankland en 1849. Il a été trouvé dissous dans du pétrole brut en 1864 par Edmund Ronalds , qui fut le premier à décrire ses propriétés.
Histoire
Le butane a été découvert par le chimiste Edward Frankland en 1849. Il a été trouvé dissous dans du pétrole brut en 1864 par Edmund Ronalds, qui fut le premier à décrire ses propriétés.
Isomères
| Nom commun |
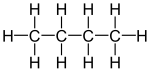
butane normal butane non ramifié n -butane |
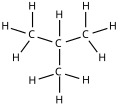
isobutane i -butane |
| Nom IUPAC | butane | méthylpropane |
Diagramme moléculaire |
|
|
Diagramme squelettique |
|

|
La rotation autour de la liaison centrale C−C produit deux conformations différentes ( trans et gauche ) pour le n- butane.
Réactions

Lorsque l'oxygène est abondant, le butane brûle pour former du dioxyde de carbone et de la vapeur d'eau ; lorsque l'oxygène est limité, du carbone ( suie ) ou du monoxyde de carbone peut également se former. Le butane est plus dense que l'air.
Lorsqu'il y a suffisamment d'oxygène :
- 2 C 4 H 10 + 13 O 2 → 8 CO 2 + 10 H 2 O
Lorsque l'oxygène est limité :
- 2 C 4 H 10 + 9 O 2 → 8 CO + 10 H 2 O
En poids, le butane contient environ 49,5 MJ / kg (13,8 kWh /kg ; 22,5 MJ/ lb ; 21 300 Btu /lb) ou en volume liquide 29,7 mégajoules par litre (8,3 kWh/l ; 112 MJ/US gal ; 107 000 Btu/US fille).
La température de flamme adiabatique maximale du butane avec l' air est de 2 243 K (1 970 °C; 3 578 °F).
Le n- butane est la matière première du procédé catalytique de DuPont pour la préparation d' anhydride maléique :
- 2 CH 3 CH 2 CH 2 CH 3 + 7 O 2 → 2 C 2 H 2 (CO) 2 O + 8 H 2 O
Le n- butane, comme tous les hydrocarbures, subit une chloration radicalaire fournissant à la fois des 1-chloro- et 2-chlorobutanes, ainsi que des dérivés plus fortement chlorés. Les vitesses relatives de la chloration s'expliquent en partie par les différentes énergies de dissociation des liaisons , 425 et 411 kJ /mol pour les deux types de liaisons CH.
Les usages
Le butane normal peut être utilisé pour le mélange d' essence , comme gaz combustible, solvant d'extraction de parfum, seul ou en mélange avec du propane , et comme matière première pour la fabrication d' éthylène et de butadiène , un ingrédient clé du caoutchouc synthétique . L'isobutane est principalement utilisé par les raffineries pour améliorer (augmenter) l' indice d'octane de l'essence à moteur.
Lorsqu'il est mélangé avec du propane et d'autres hydrocarbures, il peut être appelé commercialement GPL , pour le gaz de pétrole liquéfié. Il est utilisé comme composant du pétrole, comme matière première pour la production de produits pétrochimiques de base dans le vapocraquage , comme carburant pour les briquets et comme propulseur dans les aérosols tels que les déodorants .
Des formes très pures de butane, en particulier l'isobutane, peuvent être utilisées comme réfrigérants et ont largement remplacé les halométhanes appauvrissant la couche d'ozone , par exemple dans les réfrigérateurs et les congélateurs ménagers. La pression de fonctionnement du système pour le butane est inférieure à celle des halométhanes, tels que le R-12 , de sorte que les systèmes R-12 tels que les systèmes de climatisation automobile, lorsqu'ils sont convertis en butane pur, ne fonctionneront pas de manière optimale et, par conséquent, un mélange d'isobutane et de propane est utilisé pour donner des performances de système de refroidissement comparables au R-12.
Le butane est également utilisé comme combustible plus léger pour un briquet commun ou une torche au butane et est vendu en bouteille comme combustible pour la cuisine, les barbecues et les réchauds de camping. Le marché mondial des bidons de butane est dominé par les fabricants sud-coréens .
En tant que carburant, il est souvent mélangé à de petites quantités de sulfure d'hydrogène et de mercaptans qui donneront au gaz non brûlé une odeur désagréable facilement détectée par le nez humain. De cette façon, les fuites de butane peuvent être facilement identifiées. Alors que le sulfure d'hydrogène et les mercaptans sont toxiques, ils sont présents à des niveaux si bas que l'étouffement et le risque d'incendie par le butane deviennent une préoccupation bien avant la toxicité. La plupart des butanes disponibles dans le commerce contiennent également une certaine quantité d'huile contaminante qui peut être éliminée par filtration mais qui autrement laissera un dépôt au point d'allumage et peut éventuellement bloquer l'écoulement uniforme du gaz. Le butane utilisé dans l'extraction de parfum ne contient pas ces contaminants et les gaz butane peuvent provoquer des explosions de gaz dans des zones mal ventilées si les fuites passent inaperçues et sont enflammées par une étincelle ou une flamme. Le butane dans sa forme la plus pure est également utilisé comme solvant dans l'extraction industrielle de huiles de cannabis.
Effets et problèmes de santé
L'inhalation de butane peut provoquer une euphorie , une somnolence , une perte de conscience , une asphyxie , une arythmie cardiaque , des fluctuations de la pression artérielle et une perte de mémoire temporaire , lorsqu'il est abusé directement à partir d'un récipient fortement pressurisé , et peut entraîner la mort par asphyxie et fibrillation ventriculaire . Il pénètre dans l'approvisionnement en sang et en quelques secondes produit une intoxication. Le butane est la substance volatile la plus consommée au Royaume-Uni et a été à l'origine de 52 % des décès liés aux solvants en 2000. En pulvérisant du butane directement dans la gorge, le jet de liquide peut refroidir rapidement jusqu'à -20 °C (-4 °C). F) par expansion, provoquant un laryngospasme prolongé . Le syndrome de la « mort subite du renifleur », décrit pour la première fois par Bass en 1970, est la cause unique la plus courante de décès lié aux solvants, entraînant 55 % des cas mortels connus.
Voir également
- Isobutane
- Cyclobutane
- Éther diméthylique
- Abus de substances volatiles
- Butane (page de données)
- butanone
- n- butanol
- Gaz de pétrole liquéfié
- Gaz industriel
- Torche au butane
- Explosions de gaz