Hydroxytoluène butylé - Butylated hydroxytoluene
|
|

|
|
| Noms | |
|---|---|
|
Nom IUPAC préféré
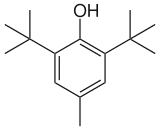
2,6-Di- tert -butyl-4-méthylphénol |
|
| Autres noms | |
| Identifiants | |
|
Modèle 3D ( JSmol )
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| Carte d'information de l'ECHA |
100.004.439 |
| Numéro CE | |
| numéro E | E321 (antioxydants, ...) |
| KEGG | |
|
CID PubChem
|
|
| Numéro RTECS | |
| UNII | |
|
Tableau de bord CompTox ( EPA )
|
|
|
|
|
|
| Propriétés | |
| C 15 H 24 O | |
| Masse molaire | 220,356 g/mol |
| Apparence | Poudre blanche à jaune |
| Odeur | Léger, phénolique |
| Densité | 1,048 g / cm 3 |
| Point de fusion | 70 °C (158 °F; 343 K) |
| Point d'ébullition | 265 °C (509 °F; 538 K) |
| 1,1 mg/L (20 °C) | |
| log P | 5.32 |
| La pression de vapeur | 0,01 mmHg (20 °C) |
| Dangers | |
| Principaux dangers | Inflammable |
| Fiche de données de sécurité | |
| Pictogrammes SGH |

|
| Mention d'avertissement SGH | Avertissement |
| H400 , H410 | |
| P273 , P391 , P501 | |
| NFPA 704 (diamant de feu) | |
| point de rupture | 127 °C (261 °F; 400 K) |
| Dose ou concentration létale (LD, LC) : | |
|
DL 50 ( dose médiane )
|
> 2 000 mg/kg (cutanée, rat) |
| NIOSH (limites d'exposition pour la santé aux États-Unis) : | |
|
PEL (Autorisé)
|
Rien |
|
REL (recommandé)
|
TWA 10 mg/m 3 |
|
IDLH (Danger immédiat)
|
ND |
| Composés apparentés | |
|
Composés apparentés
|
hydroxyanisole butylé |
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Références de l'infobox | |
L'hydroxytoluène butylé ( BHT ), également connu sous le nom de dibutylhydroxytoluène , est un composé organique lipophile , chimiquement dérivé du phénol , utile pour ses propriétés antioxydantes . BHT est largement utilisé pour empêcher les radicaux libres médié par oxydation dans les liquides (par exemple les carburants, les huiles) et d' autres matériaux, et les règlements supervisés par l' USFDA -qui considère BHT à « généralement reconnus comme sûrs » -permettez petites quantités à ajouter à aliments . Malgré cela, et la détermination antérieure par le National Cancer Institute que le BHT était non cancérigène dans un modèle animal, des inquiétudes sociétales concernant sa large utilisation ont été exprimées. Le BHT a également été postulé en tant que médicament antiviral , mais en mars 2020, l'utilisation du BHT en tant que médicament n'est pas étayée par la littérature scientifique et il n'a été approuvé par aucun organisme de réglementation des médicaments pour une utilisation en tant qu'antiviral.
Occurrence naturelle
Le phytoplancton , y compris l'algue verte Botryococcus braunii , ainsi que trois cyanobactéries différentes ( Cylindrospermopsis raciborskii , Microcystis aeruginosa et Oscillatoria sp.) sont capables de produire du BHT en tant que produit naturel . Le litchi fruitier produit également du BHT dans son péricarpe . Plusieurs champignons (exemple Aspergillus conicus ) vivant dans les olives produisent du BHT.
Production
Biosynthèse
Production industrielle
La synthèse chimique du BHT dans l'industrie a impliqué la réaction du p- crésol (4-méthylphénol) avec l' isobutylène (2-méthylpropène), catalysée par l'acide sulfurique :
- CH 3 (C 6 H 4 )OH + 2 CH 2 =C(CH 3 ) 2 → ((CH 3 ) 3 C) 2 CH 3 C 6 H 2 OH
Alternativement, le BHT a été préparé à partir de 2,6-di- tert- butylphénol par hydroxyméthylation ou aminométhylation suivie d' hydrogénolyse .
Réactions
L'espèce se comporte comme un analogue synthétique de la vitamine E , agissant principalement comme un agent de terminaison qui supprime l' auto - oxydation , un processus par lequel les composés organiques insaturés (généralement) sont attaqués par l'oxygène atmosphérique. Le BHT arrête cette réaction autocatalytique en convertissant les radicaux peroxy en hydroperoxydes. Il effectue cette fonction en faisant don d'un atome d'hydrogène :
- RO 2 • + ArOH → ROOH + ArO •
- RO 2 • + ArO• → produits non radicaux
où R est un groupe alkyle ou aryle et où ArOH est BHT ou des antioxydants phénoliques apparentés. Chaque BHT consomme deux radicaux peroxy.
Applications
Le BHT est répertorié par la banque de données sur les substances dangereuses du NIH sous plusieurs catégories dans des catalogues et des bases de données, tels qu'additif alimentaire, ingrédient de produit ménager, additif industriel, produit de soins personnels/ingrédient cosmétique, ingrédient pesticide, ingrédient plastique/caoutchouc et médical/vétérinaire/recherche .
Additif alimentaire
Le BHT est principalement utilisé comme additif alimentaire antioxydant. Aux États-Unis, il est classé comme généralement reconnu comme sûr (GRAS) sur la base d'une étude du National Cancer Institute de 1979 chez le rat et la souris. Il est approuvé pour une utilisation aux États-Unis par la Food and Drug Administration : par exemple, 21 CFR § 137.350(a)(4) autorise le BHT jusqu'à 0,0033% en poids dans le "riz enrichi", tandis que 9 CFR § 381.147](f )(1) autorise jusqu'à 0,01 % dans les volailles "en matière grasse". Il est autorisé dans l'Union européenne sous E321 .
Le BHT est utilisé comme ingrédient de conservation dans certains aliments. Avec cette utilisation, le BHT maintient la fraîcheur ou empêche la détérioration; il peut être utilisé pour diminuer la vitesse à laquelle la texture, la couleur ou la saveur des aliments change.
Certaines entreprises alimentaires ont volontairement éliminé le BHT de leurs produits ou ont annoncé qu'elles allaient l'éliminer progressivement.
Antioxydant
Le BHT est également utilisé comme antioxydant dans des produits tels que les fluides de travail des métaux , les cosmétiques , les produits pharmaceutiques , le caoutchouc , les huiles de transformateur et le fluide d' embaumement . Dans l' industrie pétrolière , où le BHT est connu sous le nom d'additif pour carburant AO-29 , il est utilisé dans les fluides hydrauliques , les huiles pour turbines et engrenages et les carburéacteurs . Le BHT est également utilisé pour empêcher la formation de peroxyde dans les éthers organiques et autres solvants et produits chimiques de laboratoire. Il est ajouté à certains monomères comme inhibiteur de polymérisation pour faciliter leur stockage en toute sécurité. Certains produits additifs contiennent du BHT comme ingrédient principal, tandis que d'autres contiennent le produit chimique simplement comme composant de leur formulation, parfois aux côtés de l'hydroxyanisole butylé (BHA).
Effets sur la santé
Comme de nombreux antioxydants phénoliques étroitement apparentés , le BHT a une faible toxicité aiguë (par exemple, l' analogue desméthyle du BHT, le 2,6-di-tert-butylphénol , a une DL 50 > 9 g/kg). La Food and Drug Administration des États-Unis classe le BHT comme généralement reconnu comme sûr (GRAS) en tant qu'agent de conservation des aliments lorsqu'il est utilisé de manière approuvée. En 1979, le National Cancer Institute a déterminé que le BHT était non cancérigène dans un modèle murin .
Néanmoins, l' Organisation mondiale de la santé a discuté d'un lien possible entre le BHT et le risque de cancer en 1986, et certaines études de recherche primaires dans les années 1970-1990 ont signalé à la fois un risque accru et un risque réduit dans le domaine de l'oncologie. De plus, des préoccupations ont été exprimées concernant le rôle alimentaire du BHT dans l'asthme et les problèmes de comportement chez les enfants. En raison de cette incertitude, le Centre pour la science dans l'intérêt public place BHT dans sa colonne « attention » et recommande de l'éviter.
Sur la base de divers rapports de recherche primaires disparates, il a été suggéré que le BHT ait une activité antivirale, et les rapports se divisent en divers types d'études. Premièrement, il existe des études qui décrivent l'inactivation du virus, où le traitement avec le produit chimique entraîne des particules virales perturbées ou autrement inactivées. L'action du BHT dans ceux-ci s'apparente à l'action de nombreux autres composés organiques, par exemple les composés d'ammonium quaternaire, les composés phénoliques et les détergents, qui perturbent les virus en insérant le produit chimique dans la membrane virale, l'enveloppe ou toute autre structure, qui sont établis méthodes de désinfection virale secondaires aux méthodes d'oxydation chimique et d'irradiation UV. En outre, il existe un rapport sur l'utilisation du BHT, par voie topique contre les lésions d'herpès génital, un rapport sur l'activité inhibitrice in vitro contre la pseudorage (en culture cellulaire) et deux études, dans des contextes vétérinaires, sur l'utilisation du BHT pour tenter de se protéger contre le virus. exposition (pseudorage chez la souris et le porc, et Newcastle chez le poulet). La pertinence d'autres rapports, concernant la grippe chez la souris, n'est pas facile à discerner. Notamment, cette série de rapports de recherche primaires ne soutient pas une conclusion générale de confirmation indépendante des résultats de recherche originaux, et il n'y a pas non plus de revues critiques apparaissant par la suite, dans des sources secondaires, pour les divers systèmes hôte-virus étudiés avec BHT.
Ainsi, à l'heure actuelle, les résultats ne présentent pas de consensus scientifique en faveur de la conclusion du potentiel antiviral général du BHT lorsqu'il est administré à l'homme. De plus, en mars 2020, aucune directive d'aucune des associations internationalement reconnues de spécialistes des maladies infectieuses n'avait préconisé l'utilisation des produits BHT comme thérapie antivirale ou prophylactique.

