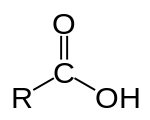
Acide carboxylique - Carboxylic acid
Un acide carboxylique est un acide organique qui contient un groupe carboxyle (C(=O)OH) attaché à un groupe R. La formule générale d'un acide carboxylique est R-COOH ou R-CO 2 H , avec R se référant au groupe alkyle , alcényle , aryle ou autre. Les acides carboxyliques sont largement répandus. Des exemples importants incluent les acides aminés et les acides gras . La déprotonation d'un acide carboxylique donne un anion carboxylate .
Exemples et nomenclature
Les acides carboxyliques sont communément identifiés par leurs noms triviaux . Ils ont souvent le suffixe acide -ique .Les noms recommandés par l' IUPAC existent également ; dans ce système, les acides carboxyliques ont un suffixe acide -oïque . Par exemple, l'acide butyrique (C 3 H 7 CO 2 H) est l'acide butanoïque selon les directives de l'IUPAC. Pour la nomenclature des molécules complexes contenant un acide carboxylique, le carboxyle peut être considéré comme la position 1 de la chaîne mère même s'il existe d'autres substituants , tels que l' acide 3-chloropropanoïque . Alternativement, il peut être nommé substituant « carboxy » ou « acide carboxylique » sur une autre structure parente, telle que le 2-carboxyfurane .
L'anion carboxylate (R-COO - ou RCO 2 - ) d'un acide carboxylique est généralement nommé avec le suffixe -ate , conformément au schéma général de l' acide -ic et -ate pour un acide conjugué et sa base conjuguée, respectivement. Par exemple, la base conjuguée de l'acide acétique est l' acétate .
L'acide carbonique , qui se produit dans la nature dans les systèmes tampons bicarbonates , n'est généralement pas classé parmi les acides carboxyliques, malgré le fait qu'il possède une fraction qui ressemble à un groupe COOH.
| Atomes de carbone |
Nom commun | Nom de l'UICPA | Formule chimique | Emplacement ou usage commun |
|---|---|---|---|---|
| 1 | L'acide formique | Acide méthanoïque | HCOOH | Les piqûres d'insectes |
| 2 | Acide acétique | Acide éthanoique | CH 3 COOH | Le vinaigre |
| 3 | L'acide propionique | Acide propanoïque | CH 3 CH 2 COOH | Conservateur pour céréales stockées, odeur corporelle , lait, beurre, fromage |
| 4 | Acide butyrique | Acide butanoïque | CH 3 (CH 2 ) 2 COOH | Le beurre |
| 5 | Acide valérique | Acide pentanoïque | CH 3 (CH 2 ) 3 COOH | Plante de valériane |
| 6 | Acide caproïque | Acide hexanoïque | CH 3 (CH 2 ) 4 COOH | chèvre gras |
| 7 | Acide énanthique | Acide heptanoïque | CH 3 (CH 2 ) 5 COOH | Fragrance |
| 8 | Acide caprylique | Acide octanoïque | CH 3 (CH 2 ) 6 COOH | Noix de coco |
| 9 | Acide pélargonique | Acide nonanoïque | CH 3 (CH 2 ) 7 COOH | Usine de pélargonium |
| dix | Acide caprique | Acide décanoïque | CH 3 (CH 2 ) 8 COOH | Huile de noix de coco et de palmiste |
| 11 | Acide undécylique | Acide undécanoïque | CH 3 (CH 2 ) 9 COOH | Agent antifongique |
| 12 | L'acide laurique | Acide dodécanoïque | CH 3 (CH 2 ) 10 COOH | Savons à l' huile de coco et pour le lavage des mains |
| 13 | Acide tridécylique | Acide tridécanoïque | CH 3 (CH 2 ) 11 COOH | Métabolite végétal |
| 14 | L'acide myristique | Acide tétradécanoïque | CH 3 (CH 2 ) 12 COOH | Noix de muscade |
| 15 | Acide pentadécylique | Acide pentadécanoïque | CH 3 (CH 2 ) 13 COOH | Matière grasse du lait |
| 16 | L'acide palmitique | Acide hexadécanoïque | CH 3 (CH 2 ) 14 COOH | huile de palme |
| 17 | Acide margarique | Acide heptadécanoïque | CH 3 (CH 2 ) 15 COOH | Phéromone chez divers animaux |
| 18 | Acide stéarique | Acide octadécanoïque | CH 3 (CH 2 ) 16 COOH | Chocolat , cires, savons et huiles |
| 19 | Acide non adécylique | Acide non adécanoïque | CH 3 (CH 2 ) 17 COOH | Graisses, huiles végétales, phéromone |
| 20 | Acide arachidique | Acide icosanoïque | CH 3 (CH 2 ) 18 COOH | Huile d'arachide |
| Classe composée | Membres |
|---|---|
| acides monocarboxyliques insaturés | acide acrylique ( acide 2-propénoïque) – CH 2 =CHCOOH, utilisé dans la synthèse des polymères |
| Les acides gras | acides monocarboxyliques saturés et insaturés à chaîne moyenne à longue, avec un nombre pair de carbones; exemples : acide docosahexaénoïque et acide eicosapentaénoïque (compléments nutritionnels) |
| Acides aminés | les éléments constitutifs des protéines |
| Acides céto | acides d'importance biochimique qui contiennent un groupe cétone ; exemples : acide acétoacétique et acide pyruvique |
| Acides carboxyliques aromatiques | contenant au moins un cycle aromatique ; exemples : acide benzoïque - le sel de sodium de l'acide benzoïque est utilisé comme conservateur alimentaire, acide salicylique - un type bêta-hydroxy présent dans de nombreux produits de soins de la peau, acides phénylalcanoïques - la classe de composés où un groupe phényle est attaché à un acide carboxylique |
| Acides dicarboxyliques | contenant deux groupes carboxyle; exemples : acide adipique le monomère utilisé pour produire le nylon et l' acide aldarique - une famille d'acides de sucre |
| Acides tricarboxyliques | contenant trois groupes carboxyle; exemples : acide citrique – présent dans les agrumes et l' acide isocitrique |
| Alpha hydroxy acides | contenant un groupe hydroxy en première position ; exemples: l' acide glycérique , l' acide glycolique et l' acide lactique (acide 2-hydroxypropanoïque) - présent dans le lait aigre, acide tartrique - dans le vin |
| Bêta hydroxy acides | contenant un groupe hydroxy en deuxième position |
| Acides oméga hydroxylés | contenant un groupe hydroxy au-delà de la première ou de la deuxième position |
| Acides gras divinyléthers | contenant une chaîne carbonée doublement insaturée attachée via une liaison éther à un acide gras, trouvée dans certaines plantes |
Propriétés physiques
Solubilité
Les acides carboxyliques sont polaires . Parce qu'ils sont à la fois des accepteurs de liaisons hydrogène (le carbonyle -C=O) et des donneurs de liaisons hydrogène (l'hydroxyle -OH), ils participent également à la liaison hydrogène . Ensemble, les groupes hydroxyle et carbonyle forment le groupe fonctionnel carboxyle. Les acides carboxyliques existent généralement sous forme de dimères dans les milieux non polaires en raison de leur tendance à « s'auto-associer ». Les acides carboxyliques plus petits (1 à 5 atomes de carbone) sont solubles dans l'eau, tandis que les acides carboxyliques plus gros ont une solubilité limitée en raison de la nature hydrophobe croissante de la chaîne alkyle. Ces acides à chaîne plus longue ont tendance à être solubles dans les solvants moins polaires tels que les éthers et les alcools. L'hydroxyde de sodium aqueux et les acides carboxyliques, même hydrophobes, réagissent pour donner des sels de sodium solubles dans l'eau. Par exemple, l' acide énathique a une faible solubilité dans l'eau (0,2 g/L), mais son sel de sodium est très soluble dans l'eau.
Points d'ébullition
Les acides carboxyliques ont tendance à avoir des points d'ébullition plus élevés que l'eau, en raison de leurs plus grandes surfaces et de leur tendance à former des dimères stabilisés par des liaisons hydrogène . Pour que l'ébullition se produise, soit les liaisons dimères doivent être rompues, soit l'ensemble de l'arrangement dimère doit être vaporisé, ce qui augmente considérablement l' enthalpie des exigences de vaporisation .

Acidité
Les acides carboxyliques sont des acides de Brønsted-Lowry car ce sont des donneurs de protons (H + ). Ils sont le type d' acide organique le plus courant .
Les acides carboxyliques sont généralement des acides faibles , ce qui signifie qu'ils ne se dissocient que partiellement en cations H 3 O + et en anions RCOO − en solution aqueuse neutre . Par exemple, à température ambiante, dans une solution 1 molaire d' acide acétique , seuls 0,4% de l'acide sont dissociés. Substituants attracteurs d' électrons, tel que -CF 3 groupe , donnent des acides plus forts (pKa de l' acide formique est de 3,75 alors que l' acide trifluoracétique, avec un substituant trifluorométhyle , a un pK a de 0,23). Les substituants donneurs d'électrons donnent des acides plus faibles (le pK a de l'acide formique est de 3,75 alors que l'acide acétique, avec un substituant méthyle , a un pK a de 4,76)
| Acide carboxylique | p K a |
|---|---|
| Acide acétique (CH 3 CO 2 H) | 4.76 |
| Acide benzoïque (C 6 H 5 CO 2 H) | 4.2 |
| Acide formique (HCOOH) | 3,75 |
| Acide chloroacétique (CH 2 ClCO 2 H) | 2,86 |
| Acide dichloroacétique (CHCl 2 CO 2 H) | 1,29 |
|
Acide oxalique (HO 2 CCO 2 H)
(première dissociation) |
1,27 |
|
Acide oxalique (HO 2 CCO 2 − )
(deuxième dissociation) |
4.14 |
| Acide trichloracétique (CCl 3 CO 2 H) | 0,65 |
| Acide trifluoroacétique (CF 3 CO 2 H) | 0,23 |
La déprotonation des acides carboxyliques donne des anions carboxylates; ceux-ci sont stabilisés en résonance , car la charge négative est délocalisée sur les deux atomes d'oxygène, augmentant la stabilité de l'anion. Chacune des liaisons carbone-oxygène dans l'anion carboxylate a un caractère partiel de double liaison. La charge positive partielle du carbone du groupe carbonyle est également affaiblie par les - 1 / 2 charges de négatifs sur les 2 atomes d'oxygène.
Odeur
Les acides carboxyliques ont souvent de fortes odeurs acides. Les esters d'acides carboxyliques ont tendance à avoir des odeurs agréables, et beaucoup sont utilisés en parfumerie .
Caractérisation
Les acides carboxyliques sont facilement identifiés comme tels par spectroscopie infrarouge . Ils présentent une forte bande associée à la vibration de la liaison C-O vibration ( ν C = O ) entre 1680 et 1725 cm -1 . Une bande caractéristique ν O–H apparaît sous la forme d'un large pic dans la région de 2500 à 3000 cm -1 . Par spectrométrie RMN 1 H , l' hydrogène hydroxylé apparaît dans la région de 10 à 13 ppm, bien qu'il soit souvent soit élargi, soit non observé en raison d'échanges avec des traces d'eau.
Occurrence et applications
De nombreux acides carboxyliques sont produits industriellement à grande échelle. On les trouve aussi fréquemment dans la nature. Les esters d'acides gras sont les principaux composants des lipides et les polyamides d' acides aminocarboxyliques sont les principaux composants des protéines .
Les acides carboxyliques sont utilisés dans la production de polymères, de produits pharmaceutiques, de solvants et d'additifs alimentaires. Les acides carboxyliques d'importance industrielle comprennent l'acide acétique (composant du vinaigre, précurseur des solvants et des revêtements), les acides acrylique et méthacrylique (précurseurs des polymères, adhésifs), l'acide adipique (polymères), l'acide citrique (un arôme et un conservateur dans les aliments et les boissons), acide éthylènediaminetétraacétique (agent chélatant), acides gras (enrobages), acide maléique (polymères), acide propionique (conservateur alimentaire), acide téréphtalique (polymères). Les sels de carboxylate importants sont les savons.
Synthèse
Routes industrielles
En général, les voies industrielles vers les acides carboxyliques diffèrent de celles utilisées à plus petite échelle car elles nécessitent un équipement spécialisé.
- Carbonylation des alcools illustrée par le procédé Cativa pour la production d'acide acétique. L'acide formique est préparé par une voie de carbonylation différente, en partant également du méthanol.
- Oxydation d' aldéhydes à l'air à l'aide de catalyseurs au cobalt et au manganèse. Les aldéhydes recherchés sont facilement obtenus à partir d'alcènes par hydroformylation .
- Oxydation des hydrocarbures par l'air. Pour les alcanes simples, cette méthode est peu coûteuse mais pas assez sélective pour être utile. Les composés allyliques et benzyliques subissent des oxydations plus sélectives. Les groupes alkyle sur un cycle benzénique sont oxydés en acide carboxylique, quelle que soit sa longueur de chaîne. L' acide benzoïque à partir de toluène , de l' acide téréphtalique à partir de para - xylène , et l' acide phtalique à partir d' ortho - xylène sont les conversions à grande échelle d' illustration. L'acide acrylique est généré à partir du propène .
- Oxydation de l'éthène à l' aide d' un catalyseur d' acide silicotungstique .
- Déshydrogénation d'alcools catalysée par une base.
- Carbonylation couplée à l'ajout d'eau. Cette méthode est efficace et polyvalente pour les alcènes qui génèrent des carbocations secondaires et tertiaires , par exemple l' isobutylène en acide pivalique . Dans la réaction de Koch , l'ajout d'eau et de monoxyde de carbone aux alcènes est catalysé par des acides forts. Les hydrocarboxylations impliquent l'ajout simultané d'eau et de CO . De telles réactions sont parfois appelées « chimie de Reppe ».
- HCCH + CO + H 2 O → CH 2 =CHCO 2 H
- Hydrolyse des triglycérides obtenus à partir d'huiles végétales ou animales. Ces méthodes de synthèse de certains acides carboxyliques à longue chaîne sont liées à la fabrication de savons .
- Fermentation de l'éthanol. Cette méthode est utilisée dans la production de vinaigre .
- La réaction de Kolbe-Schmitt fournit une voie à l'acide salicylique , précurseur de l' aspirine .
Méthodes de laboratoire
Les méthodes de préparation pour les réactions à petite échelle pour la recherche ou pour la production de produits chimiques fins utilisent souvent des réactifs consommables coûteux.
- Oxydation d'alcools primaires ou d' aldéhydes avec des oxydants forts tels que le dichromate de potassium , le réactif de Jones , le permanganate de potassium ou le chlorite de sodium . La méthode est plus adaptée aux conditions de laboratoire que l'utilisation industrielle de l'air, qui est plus "vert" car il donne moins de sous-produits inorganiques tels que les oxydes de chrome ou de manganèse.
- Clivage oxydatif des oléfines par ozonolyse , permanganate de potassium ou dichromate de potassium .
- Hydrolyse des nitriles , des esters ou des amides , généralement avec une catalyse acide ou basique.
- Carbonatation d'un réactif de Grignard et réactifs organolithiens :
- RLi + CO 2 → RCO 2 Li
- RCO 2 Li + HCl → RCO 2 H + LiCl
- Halogénation suivie d'hydrolyse des méthylcétones dans la réaction haloforme
- Clivage catalysé par une base de cétones non énolisables, en particulier d'aryl cétones :
- RC(O)Ar + H 2 O → RCO 2 H + ArH
Réactions moins fréquentes
De nombreuses réactions produisent des acides carboxyliques mais ne sont utilisées que dans des cas spécifiques ou sont principalement d'intérêt académique.
- Dismutation d'un aldéhyde dans la réaction de Cannizzaro
- Le réarrangement des dicétones dans le réarrangement de l'acide benzilique impliquant la génération d'acides benzoïques est la réaction de von Richter à partir de nitrobenzènes et la réaction de Kolbe-Schmitt à partir de phénols .
Réactions
Les réactions les plus largement pratiquées convertissent les acides carboxyliques en esters, amides, sels de carboxylate, chlorures d'acide et alcools. Les acides carboxyliques réagissent avec les bases pour former des sels de carboxylate, dans lesquels l'hydrogène du groupe hydroxyle (-OH) est remplacé par un cation métallique . Par exemple, l'acide acétique présent dans le vinaigre réagit avec le bicarbonate de sodium (bicarbonate de soude) pour former de l'acétate de sodium, du dioxyde de carbone et de l'eau :
- CH 3 COOH + NaHCO 3 → CH 3 COO − Na + + CO 2 + H 2 O
Les acides carboxyliques réagissent également avec les alcools pour donner des esters . Ce procédé est largement utilisé, par exemple dans la production de polyesters . De même, les acides carboxyliques sont convertis en amides , mais cette conversion ne se produit généralement pas par réaction directe de l'acide carboxylique et de l'amine. Au lieu de cela, les esters sont des précurseurs typiques des amides. La conversion des acides aminés en peptides est un processus biochimique important qui nécessite de l' ATP .
Le groupe hydroxyle sur les acides carboxyliques peut être remplacé par un atome de chlore en utilisant du chlorure de thionyle pour donner des chlorures d'acyle . Dans la nature, les acides carboxyliques sont convertis en thioesters .
Réduction
Comme les esters , la plupart des acides carboxyliques peuvent être réduits en alcools par hydrogénation ou en utilisant des agents de transfert d'hydrure ou d'alkyle (car ils déprotoneraient les acides à la place sans transfert) tels que l'hydrure de lithium et d'aluminium ou les réactifs de Grignard ( composés organolithiens ).
Le chlorure de N , N -diméthyl(chlorométhylène)ammonium (ClHC=N + (CH 3 ) 2 Cl − ) est un agent hautement chimiosélectif pour la réduction de l'acide carboxylique. Il active sélectivement l'acide carboxylique pour donner le sel de carboxyméthylèneammonium, qui peut être réduit par un réducteur doux comme l'hydrure de lithium tris( t- butoxy)aluminium pour donner un aldéhyde dans une procédure en un seul pot. Cette procédure est connue pour tolérer des fonctionnalités carbonyle réactives telles que la cétone ainsi que des fragments ester, oléfine, nitrile et halogénure modérément réactifs.
Réactions spécialisées
- Comme pour tous les composés carbonylés, les protons sur le carbone sont labiles en raison de la tautomérisation céto-énol . Ainsi, le carbone est facilement halogéné dans l'halogénation Hell-Volhard-Zelinsky .
- La réaction de Schmidt convertit les acides carboxyliques en amines .
- Les acides carboxyliques sont décarboxylés dans la réaction de Hunsdiecker .
- La réaction de Dakin-West convertit un acide aminé en l'aminocétone correspondante.
- Dans la dégradation Barbier-Wieland , un acide carboxylique sur une chaîne aliphatique ayant un simple pont méthylène en position alpha peut avoir la chaîne raccourcie d'un carbone. La procédure inverse est la synthèse d'Arndt-Eistert , où un acide est converti en halogénure d'acyle, qui est ensuite mis à réagir avec du diazométhane pour donner un méthylène supplémentaire dans la chaîne aliphatique.
- De nombreux acides subissent une décarboxylation oxydative . Les enzymes qui catalysent ces réactions sont appelées carboxylases ( EC 6.4.1) et décarboxylases (EC 4.1.1).
- Les acides carboxyliques sont réduits en aldéhydes via l' ester et le DIBAL , via le chlorure d'acide dans la réduction de Rosenmund et via le thioester dans la réduction de Fukuyama .
- Dans la décarboxylation cétonique, les acides carboxyliques sont convertis en cétones.
- Les réactifs organolithiens (> 2 équiv) réagissent avec les acides carboxyliques pour donner un 1,1-diolate de dilithium, un intermédiaire tétraédrique stable qui se décompose pour donner une cétone lors d'un traitement acide.
- L' électrolyse de Kolbe est une réaction de dimérisation électrolytique et décarboxylative. Il se débarrasse des groupes carboxyle de deux molécules d'acide et relie les fragments restants entre eux.
Radical carboxyle
Le radical carboxyle , •COOH, n'existe que brièvement. La constante de dissociation acide de • COOH a été mesurée par spectroscopie de résonance paramagnétique électronique . Le groupe carboxyle a tendance à se dimériser pour former de l'acide oxalique .
Voir également
- Anhydride d'acide
- Chlorure d'acide
- Amide
- Acide aminé
- Ester
- Liste des acides carboxyliques
- Acide dicarboxylique
- Acide polyhydroxycarboxylique (PHC).
- Pseudoacide
- Thiocarboxy
Les références
Liens externes
- Acides carboxyliques pH et titrage - logiciel gratuit pour les calculs, l'analyse des données, la simulation et la génération de diagrammes de distribution
- SSP.