Shunt cérébral - Cerebral shunt
| Shunt cérébral | |
|---|---|
 Un schéma d'un shunt cérébral typique
| |
| Engrener | D002557 |
Les shunts cérébraux sont couramment utilisés pour traiter l' hydrocéphalie , le gonflement du cerveau dû à une accumulation excessive de liquide céphalo-rachidien (LCR) . Si rien n'est fait, le liquide céphalo-rachidien peut s'accumuler, entraînant une augmentation de la pression intracrânienne (PIC) pouvant entraîner un hématome intracrânien , un œdème cérébral , un écrasement du tissu cérébral ou une hernie . Le shunt cérébral peut être utilisé pour atténuer ou prévenir ces problèmes chez les patients qui souffrent d'hydrocéphalie ou d'autres maladies apparentées.
Les shunts peuvent se présenter sous diverses formes, mais la plupart d'entre eux consistent en un boîtier de valve relié à un cathéter, dont l'extrémité est généralement placée dans la cavité péritonéale . Les principales différences entre les shunts résident généralement dans les matériaux utilisés pour les construire, les types de vannes (le cas échéant) utilisées et si la vanne est programmable ou non.
La description
Types de vannes
| Type de vanne | La description |
|---|---|
| Delta | Conçu pour éviter le drainage excessif. Reste fermé jusqu'à ce que l'ICP atteigne un niveau prédéterminé. Laisse le ventricule shunté plus gros que les ventricules non shuntés . |
| Moyenne pression cylindrique | Peut conduire à un drainage inégal des ventricules. |
| Nulsen et Spitz | Contient deux unités à clapet à bille reliées par un ressort. N'a pas de réglage de pression réglable. Première valve produite en série utilisée pour traiter l'hydrocéphalie en 1956. |
| Spitz Holter | Utilise des fentes en silicone pour éviter les défaillances mécaniques. |
| Anti-siphon | Empêche le drainage excessif en empêchant l' effet de siphon . Le dispositif se ferme lorsque la pression à l'intérieur de la vanne devient négative par rapport à la pression ambiante. Empêche le drainage excessif qui pourrait se produire lorsqu'un patient s'assoit, se lève ou change rapidement de posture. |
| Sigma | La vanne Sigma fonctionne sur un mécanisme de contrôle de débit par opposition au système de contrôle de pression des autres vannes. L'appareil peut réguler les changements de débit du LCR sans être programmé ou modifié chirurgicalement. La première itération a été introduite en 1987. La vanne fonctionnait en trois étapes pour empêcher le drainage excessif et insuffisant. |
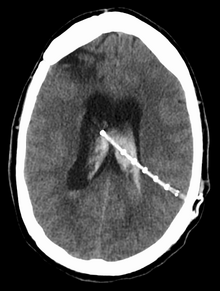
Emplacement du shunt

L'emplacement du shunt est déterminé par le neurochirurgien en fonction du type et de l'emplacement du blocage provoquant l'hydrocéphalie. Tous les ventricules cérébraux sont candidats au shunt. Le cathéter est le plus souvent placé dans l'abdomen, mais d'autres emplacements incluent le cœur et les poumons. Les shunts peuvent souvent être nommés d'après la voie empruntée par le neurochirurgien. L'extrémité distale du cathéter peut être située dans à peu près n'importe quel tissu avec suffisamment de cellules épithéliales pour absorber le LCR entrant. Vous trouverez ci-dessous quelques plans de routage courants pour les shunts cérébraux.
Le point de Frazier
Il est situé sur l'os pariétal, au-dessus de la suture lambdoïde. Plus précisément, 3 à 4 cm latéralement à la ligne médiane et 6 cm au-dessus de l'inion. C'est un site fréquent de canulation ventriculaire dans le cadre de la mise en place d'un shunt ventriculopéritonéal pour le traitement de l'hydrocéphalie. Il a été décrit pour la première fois par CH Frazier en 1928.
Acheminement des shunts
| Route | Emplacement du drain de fluide |
|---|---|
| Shunt ventriculo-péritonéal (shunt VP) | Cavité péritonéale |
| Shunt ventriculo-auriculaire (shunt VA) | oreillette droite du coeur |
| Shunt ventriculo-pleural (shunt VPL) | Cavité pleurale |
| Shunt ventriculo-cisternal (shunt VC) | Cisterna magna |
| Shunt ventriculo-sous-galéal (shunt SG) | Espace sous-galéal |
| Shunt lombo-péritonéal (shunt LP) | Cavité péritonéale |
Un shunt sous-galéal est généralement une mesure temporaire utilisée chez les nourrissons trop petits ou prématurés pour tolérer d'autres types de shunt. Le chirurgien forme une poche sous l'aponévrose épicrânienne (l'espace sous-galéal) et permet au LCR de s'écouler des ventricules, créant un gonflement rempli de liquide sur le cuir chevelu du bébé. Ces shunts sont normalement convertis en VP ou en d'autres types de shunt une fois que l'enfant est assez grand.
Les indications
Vous trouverez ci-dessous une courte liste des complications connues pouvant entraîner une hydrocéphalie nécessitant un shunt.
| Diagnostics | La description | Incidence |
|---|---|---|
| Hydrocéphalie congénitale | Un large éventail d'anomalies génétiques pouvant conduire à une hydrocéphalie à la naissance. | 0,04–0,08% |
| Tumeur | Un certain nombre de tumeurs différentes peuvent entraîner un blocage du LCR si elles sont situées dans certaines zones. Certaines de ces zones comprennent les ventricules latéraux ou tiers, la fosse postérieure et les tumeurs intrarachidiennes. Les tumeurs peuvent être malignes ou bénignes. | Inconnu |
| Hydrocéphalie post-hémorragique | Les saignements dans les ventricules du cerveau, en particulier chez les nourrissons, peuvent entraîner un blocage du drainage du LCR et provoquer une hydrocéphalie. | |
| Spina bifida | Spécifiquement, le myéloméningocèle du spina bifida peut provoquer le développement de l'hydrocéphalie car le cervelet bloquera le flux de LCR dans un développement de la malformation de Chiari II. | .125% |
| Sténose congénitale de l'aqueduc | Une maladie génétique qui peut provoquer des déformations du système nerveux. Le défaut est généralement associé à un retard mental, des pouces enlevés et une paraplégie spastique. | 0,003% |
| Craniosynostose | La craniosynostose survient lorsque les sutures du crâne se ferment trop tôt. Le résultat de la fusion de plusieurs sutures avant que le cerveau ne cesse de croître est une augmentation de la PIC conduisant à une hydrocéphalie. | 0,05% |
| Hydrocéphalie post-méningitique | L'inflammation et les cicatrices causées par la méningite peuvent inhiber l'absorption du LCR. | |
| Syndrome de Dandy-Walker | Les patients présentent généralement une déformation kystique du quatrième ventricule, une hypoplasie du vermis cérébelleux et une fosse postérieure élargie. La condition est une maladie génétiquement héréditaire. | 0,003% |
| Kyste arachnoïdien | Un défaut causé lorsque le LCR forme une collection qui est piégée dans les membranes arachnoïdiennes. Le kyste résultant peut alors bloquer le flux normal de LCR du cerveau entraînant une hydrocéphalie ainsi que d'autres défauts. Les localisations les plus courantes d'un kyste arachnoïdien sont la fosse moyenne et la fosse postérieure. Les symptômes les plus courants sont les nausées et les vertiges. | 0,05% |
| Hypertension intracrânienne idiopathique | Un trouble neurologique rare affectant environ 1 personne sur 100 000, dont la plupart sont des femmes en âge de procréer. L'IIH entraîne une élévation de la pression intracrânienne et peut entraîner une perte permanente de la vision. | |
| Hydrocéphalie à pression normale , également connue sous le nom de syndrome de Hakim-Adams | Un excès de liquide céphalo-rachidien (LCR) se produit dans les ventricules et avec une pression de liquide céphalo-rachidien normale ou légèrement élevée |
Complications
Il existe un certain nombre de complications associées à la mise en place d'un shunt. Bon nombre de ces complications surviennent pendant l'enfance et cessent une fois que le patient a atteint l'âge adulte. Bon nombre des complications observées chez les patients nécessitent une révision immédiate du shunt (le remplacement ou la reprogrammation du shunt déjà existant). Les symptômes courants ressemblent souvent à la nouvelle apparition de l'hydrocéphalie, tels que maux de tête, nausées, vomissements, vision double et altération de la conscience. Cela peut endommager la mémoire à court terme d'un individu. De plus, dans la population pédiatrique, le taux d'échec du shunt 2 ans après l'implantation a été estimé à 50 %.
Infection
L'infection est une complication courante qui affecte normalement les patients pédiatriques, car ils n'ont pas encore développé d'immunité contre un certain nombre de maladies différentes. Normalement, l'incidence de l'infection diminue à mesure que le patient vieillit et que le corps acquiert une immunité contre divers agents infectieux. L'infection du shunt est un problème courant et peut survenir chez jusqu'à 27 % des patients ayant un shunt. L'infection peut entraîner des défauts cognitifs à long terme, des problèmes neurologiques et, dans certains cas, la mort. Les agents microbiens courants pour l'infection par shunt comprennent Staphylococcus epidermidis , Staphylococcus aureus et Candida albicans . D'autres facteurs conduisant à l'infection du shunt comprennent l'insertion du shunt à un jeune âge (< 6 mois) et le type d'hydrocéphalie traitée. Il n'y a pas de forte corrélation entre l'infection et le type de shunt. Les symptômes d'une infection par shunt sont très similaires aux symptômes observés dans l'hydrocéphalie, mais peuvent également inclure de la fièvre et un nombre élevé de globules blancs.
Traitement des infections de shunt
Le traitement d'une infection du shunt du LCR comprend généralement le retrait du shunt et la mise en place d'un réservoir ventriculaire temporaire jusqu'à ce que l'infection soit résolue. Il existe quatre méthodes principales de traitement des infections du shunt ventriculopéritonéal (VP) : (1) les antibiotiques ; (2) retrait du shunt infecté avec remplacement immédiat ; (3) externalisation du shunt avec remplacement éventuel ; (4) retrait du shunt infecté avec mise en place d'un drain ventriculaire externe (EVD) et réinsertion éventuelle du shunt. La dernière méthode est la meilleure avec un taux de réussite de plus de 95%.
Traitement médical de l'infection du shunt
Le traitement empirique initial de l'infection par shunt du LCR doit inclure une large couverture incluant les bacilles aérobies à Gram négatif, y compris les pseudomonas et les organismes à Gram positif, y compris Staph aureus et les staphylocoques à coagulase négative, comme une combinaison de ceftazidime et de vancomycine. Certains cliniciens ajoutent des aminosides parentéraux ou intrathécaux pour fournir une couverture améliorée des pseudomonas, bien que l'efficacité de ceci ne soit pas claire pour le moment. Le méropénem et l'aztréonam sont des options supplémentaires efficaces contre les infections bactériennes à Gram négatif.
Traitement chirurgical de l'infection du shunt
Pour évaluer le bénéfice de l'ablation chirurgicale du shunt ou de l'externalisation suivie d'une ablation, Wong et al. ont comparé deux groupes : un avec un traitement médical seul et un autre avec un traitement médical et chirurgical simultanément. 28 patients atteints d'infection après implantation d'un shunt ventriculopéritonéal sur une période de 8 ans dans leur centre de neurochirurgie ont été étudiés. 17 de ces patients ont été traités par ablation d'un shunt ou externalisation suivie d'une ablation en plus des antibiotiques IV tandis que les 11 autres ont été traités par des antibiotiques IV uniquement. Le groupe recevant à la fois l'ablation d'un shunt chirurgical et des antibiotiques a montré une mortalité plus faible – 19 % contre 42 % (p = 0,231). Bien que ces résultats ne soient pas statistiquement significatifs, Wong et al. suggèrent de gérer les infections du shunt VP via un traitement chirurgical et médical.
Une analyse de 17 études publiées au cours des 30 dernières années concernant les enfants atteints d'infections du shunt du LCR a révélé que le traitement à la fois avec le retrait du shunt et des antibiotiques a traité avec succès 88 % des 244 infections, tandis que l'antibiothérapie seule a traité avec succès l'infection du shunt du LCR dans seulement 33 % des 230 infections.
Alors que les méthodes chirurgicales typiques de traitement des infections du shunt VP impliquent le retrait et la réimplantation du shunt, différents types d'opérations ont été utilisées avec succès chez certains patients. Steinbok et al. a traité un cas d'infections récurrentes du shunt VP chez un patient eczémateux avec un shunt ventriculo-sous-galéal pendant deux mois jusqu'à la guérison complète de l'eczéma. Ce type de shunt leur a permis d'éviter la zone de peau malade qui servait de source d'infection. Jones et al. ont traité 4 patients atteints d'hydrocéphalie non communicante qui souffraient d'infections du shunt VP avec ablation du shunt et troisième ventriculostomie. Ces patients ont été guéris de l'infection et n'ont pas eu besoin de réinsertion de shunt, démontrant ainsi l'efficacité de cette procédure chez ces types de patients.
Obstruction
Une autre cause principale d'échec du shunt est le blocage du shunt à l'extrémité proximale ou distale. À l'extrémité proximale, la valve de dérivation peut se bloquer en raison de l'accumulation de protéines en excès dans le LCR. La protéine supplémentaire s'accumulera au point de drainage et obstruera lentement la valve. Le shunt peut également se bloquer à l'extrémité distale si le shunt est retiré de la cavité abdominale (dans le cas des shunts VP) ou à cause d'une accumulation de protéines similaire. D'autres causes de blocage sont le surdrainage et le syndrome du ventricule fendu.
Plus de drainage
Un drainage excessif se produit lorsqu'un shunt n'a pas été conçu de manière adéquate pour le patient en particulier. Un drainage excessif peut entraîner un certain nombre de complications différentes, dont certaines sont décrites ci-dessous.
Habituellement, l'un des deux types de surdrainage peut se produire. Premièrement, lorsque le LCR se draine trop rapidement, une condition connue sous le nom de collection de fluide extra-axiale peut se produire. Dans cette condition, le cerveau s'effondre sur lui-même, ce qui entraîne une accumulation de LCR ou de sang autour du cerveau. Cela peut causer de graves lésions cérébrales en comprimant le cerveau. De plus, un hématome sous-dural peut se développer. La collection extra-axiale de fluide peut être traitée de trois manières différentes selon la sévérité de la condition. Habituellement, le shunt sera remplacé ou reprogrammé pour libérer moins de LCR et le liquide collecté autour du cerveau sera drainé. La deuxième condition connue sous le nom de syndrome du ventricule fendu survient lorsque le LCR se draine lentement pendant plusieurs années. Plus d'informations sur le syndrome du ventricule fendu apparaissent ci-dessous.
Chiari I malformation
Des études récentes ont montré que le drainage sur du LCR en raison de shuntage peut conduire à acquérir une malformation de Chiari . On pensait auparavant que la malformation de Chiari I était le résultat d'une anomalie congénitale, mais de nouvelles études ont montré que le drainage excessif des shunts cysto-péritonéaux utilisés pour traiter les kystes arachnoïdiens peut entraîner le développement d'un surpeuplement de la fosse postérieure et d'une hernie amygdalienne , cette dernière étant la définition classique de la malformation de Chiari I. Les symptômes courants incluent des maux de tête majeurs, une perte auditive, de la fatigue, une faiblesse musculaire et une perte de la fonction du cervelet.
Syndrome du ventricule fendu
Le syndrome du ventricule fendu est un trouble rare associé aux patients shuntés, mais entraîne un grand nombre de reprises de shunt. La condition survient généralement plusieurs années après l'implantation du shunt. Les symptômes les plus courants sont similaires à un dysfonctionnement normal du shunt, mais il existe plusieurs différences clés. Premièrement, les symptômes sont souvent cycliques et apparaîtront puis disparaîtront plusieurs fois au cours de la vie. Deuxièmement, les symptômes peuvent être atténués en étant allongé sur le ventre. En cas de dysfonctionnement du shunt, ni le temps ni la position posturale n'affecteront les symptômes.
On pense souvent que la condition se produit pendant une période où le surdrainage et la croissance du cerveau se produisent simultanément. Dans ce cas, le cerveau remplit l'espace intraventriculaire, laissant les ventricules effondrés. De plus, la compliance du cerveau diminuera, ce qui empêchera les ventricules de s'élargir, réduisant ainsi les chances de guérir le syndrome. Les ventricules effondrés peuvent également bloquer la valve de dérivation, entraînant une obstruction. Étant donné que les effets du syndrome du ventricule fendu sont irréversibles, des soins constants dans la gestion de la maladie sont nécessaires.
Hémorragie intraventriculaire
Une hémorragie intraventriculaire peut survenir à tout moment pendant ou après l'insertion ou la reprise d'un shunt. Des hémorragies intraparenchymateuses de nature multifocale ont également été décrites dans la population pédiatrique après shunt ventriculopéritonéal. L'hémorragie peut entraîner une altération de la fonction shunt qui peut entraîner de graves déficiences neurologiques. Des études ont montré qu'une hémorragie intraventriculaire peut survenir dans près de 31 % des reprises de shunt.
Résultats et pronostic
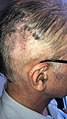
- Cicatrisation chirurgicale pour un shunt ventriculo-péritonéal (shunt VP)
Suppression du shunt
Bien qu'il y ait eu de nombreux cas de patients atteignant "l'indépendance du shunt", il n'y a pas d'accord commun dans lequel les médecins peuvent convenir qu'un patient pourrait survivre sans shunt. Un autre problème avec le retrait du shunt est qu'il est très difficile de discerner quand un patient peut être indépendant du shunt sans conditions très spécifiques. Le retrait global du shunt est une procédure rare mais pas inconnue.