Bromure de césium - Caesium bromide
|
|

|
|
| Noms | |
|---|---|
|
Nom IUPAC
Bromure de césium
|
|
| Autres noms
Bromure de césium, bromure de
césium(I) |
|
| Identifiants | |
|
Modèle 3D ( JSmol )
|
|
| ChemSpider | |
| Carte d'information de l'ECHA |
100.029.209 |
| Numéro CE | |
|
CID PubChem
|
|
| UNII | |
|
Tableau de bord CompTox ( EPA )
|
|
|
|
|
|
| Propriétés | |
| CsBr | |
| Masse molaire | 212,809 g/mol |
| Apparence | Solide blanc |
| Densité | 4,43 g / cm 3 |
| Point de fusion | 636 °C (1 177 °F ; 909 K) |
| Point d'ébullition | 1 300 °C (2 370 °F; 1 570 K) |
| 1230 g/L (25 °C) contesté.
420 g/L (11 °C) Voir Références |
|
| -67,2.10 -6 cm 3 /mol | |
|
Indice de réfraction ( n D )
|
1,8047 (0,3 µm) 1,6974 (0,59 µm) 1,6861 (0,75 µm) 1,6784 (1 µm) 1,6678 (5 µm) 1,6439 (20 µm) |
| Structure | |
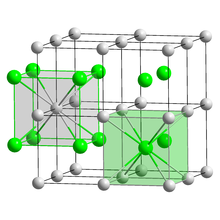
| CsCl , cP2 | |
| Pm 3 m, n° 221 | |
a = 0,4291 nm
|
|
|
Volume du réseau ( V )
|
0,0790 nm 3 |
|
Unités de formule ( Z )
|
1 |
| Cubique (Cs + ) Cubique (Br − ) |
|
| Dangers | |
| Pictogrammes SGH |

|
| Mention d'avertissement SGH | Avertissement |
| H302 , H315 , H319 , H335 | |
| P261 , P264 , P270 , P271 , P280 , P301 + 312 , P302 + 352 , P304 + 340 , P305 + 351 + 338 , P312 , P321 , P330 , P332 + 313 , P337 + 313 , P362 , P403 + 233 , P405 , P501 | |
| NFPA 704 (diamant de feu) | |
| point de rupture | Ininflammable |
| Dose ou concentration létale (LD, LC) : | |
|
DL 50 ( dose médiane )
|
1400 mg/kg (orale, rat) |
| Composés apparentés | |
|
Autres anions
|
Fluorure de césium Chlorure de césium Iodure de césium Astatide de césium |
|
Autres cations
|
Bromure de sodium Bromure de potassium Bromure de rubidium Bromure de francium |
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Références de l'infobox | |
Le bromure de césium ou bromure de césium est un composé ionique de césium et de brome de formule chimique CsBr. C'est un solide blanc ou transparent avec un point de fusion à 636 °C qui se dissout facilement dans l'eau. Ses cristaux en vrac ont la structure cubique CsCl, mais la structure change pour le type de sel gemme dans un film nanométrique développé sur des substrats de mica , LiF, KBr ou NaCl.
Synthèse
Le bromure de césium peut être préparé via les réactions suivantes :
- CsOH (aq) + HBr (aq) → CsBr (aq) + H 2 O (l)
- Cs 2 (CO 3 ) (aq) + 2 HBr (aq) → 2 CsBr (aq) + H 2 O (l) + CO 2 (g)
- Synthèse directe :
- 2 Cs (s) + Br 2 (g) → 2 CsBr (s)
La synthèse directe est une réaction vigoureuse du césium avec d'autres halogènes. En raison de son coût élevé, il n'est pas utilisé pour la préparation.
Les usages
Le bromure de césium est parfois utilisé en optique comme composant séparateur de faisceau dans les spectrophotomètres à large bande .
Les références
* Données expérimentales Crystran Ltd juillet 2021
Sources citées
- Haynes, William M., éd. (2011). CRC Handbook of Chemistry and Physics (92e éd.). Boca Raton, Floride : CRC Press . ISBN 1439855110.

