Choline - Choline
|
|

|
|
| Noms | |
|---|---|
|
Nom IUPAC préféré
2-Hydroxy- N , N , N -triméthyléthane-1-aminium |
|
| Autres noms
2-Hydroxy- N , N , N -triméthyléthanaminium
Bilineurine (2-Hydroxyéthyl)triméthylammonium |
|
| Identifiants | |
|
Modèle 3D ( JSmol )
|
|
| 1736748 | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| Banque de médicaments | |
| Carte d'information de l'ECHA |
100.000.487 |
| Numéro CE | |
| 324597 | |
| KEGG | |
|
CID PubChem
|
|
| UNII | |
|
Tableau de bord CompTox ( EPA )
|
|
|
|
|
|
| Propriétés | |
| C 5 H 14 NON + | |
| Masse molaire | 104,17 g/mol |
| Apparence | liquide visqueux déliquescent (hydroxyde de choline) |
| très soluble (hydroxyde de choline) | |
| Solubilité | soluble dans l' éthanol , insoluble dans l' éther diéthylique et le chloroforme (hydroxyde de choline) |
| Dangers | |
| Pictogrammes SGH |

|
| Mention d'avertissement SGH | Danger |
| H314 | |
| P260 , P264 , P280 , P301 + 330 + 331 , P303 + 361 + 353 , P304 + 340 , P305 + 351 + 338 , P310 , P321 , P363 , P405 , P501 | |
| NFPA 704 (diamant de feu) | |
| Dose ou concentration létale (LD, LC) : | |
|
DL 50 ( dose médiane )
|
3–6 g/kg pc , rats, orale |
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Références de l'infobox | |
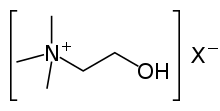
Choline / k oʊ l Ï n / est un élément nutritif essentiel pour l' homme et beaucoup d' autres animaux. La choline se présente sous la forme d'un cation qui forme divers sels (X - dans la formule illustrée est un contre-anion indéfini ). Pour maintenir la santé, il doit être obtenu à partir de l'alimentation sous forme de choline ou de phospholipides de la choline , comme la phosphatidylcholine . Les humains, ainsi que la plupart des autres espèces animales, fabriquent de la choline de novo , mais la production est généralement insuffisante. La choline n'est souvent pas classée comme une vitamine , mais comme un nutriment avec un métabolisme de type acide aminé . Chez la plupart des animaux, les phospholipides de la choline sont des composants nécessaires des membranes cellulaires , des membranes des organites cellulaires et des lipoprotéines de très basse densité . La choline est nécessaire pour produire de l' acétylcholine – un neurotransmetteur – et de la S- adénosylméthionine , un donneur universel de méthyle impliqué dans la synthèse de l' homocystéine .
Une carence symptomatique en choline - rare chez l'homme - provoque une stéatose hépatique non alcoolique et des lésions musculaires. Une consommation excessive de choline (supérieure à 7,5 g/jour) peut provoquer une hypotension artérielle , de la transpiration , de la diarrhée et une odeur corporelle semblable à celle du poisson en raison de la triméthylamine , qui se forme dans son métabolisme. Les riches sources alimentaires de choline et de phospholipides de choline comprennent les abats et les jaunes d'œufs , les produits laitiers et les légumes .
Chimie
La choline est une famille de composés d'ammonium quaternaire hydrosolubles . L' hydroxyde de choline est connu sous le nom de base de choline. Il est hygroscopique et donc souvent rencontré sous forme de sirop hydraté visqueux incolore qui sent la triméthylamine (TMA). Les solutions aqueuses de choline sont stables, mais le composé se décompose lentement en éthylène glycol , polyéthylène glycols et TMA.
Le chlorure de choline peut être fabriqué en traitant le TMA avec du 2-chloroéthanol :
- (CH 3 ) 3 N + ClCH 2 CH 2 OH → (CH 3 ) 3 N + CH 2 CH 2 OH · Cl –
Le 2-chloroéthanol peut être généré à partir d' oxyde d'éthylène . La choline a historiquement été produite à partir de sources naturelles, telles que l' hydrolyse de la lécithine .
Métabolisme
Biosynthèse
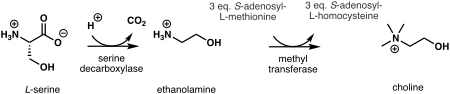
Chez les plantes, la première étape de la biosynthèse de novo de la choline est la décarboxylation de la sérine en éthanolamine , qui est catalysée par une sérine décarboxylase . La synthèse de la choline de l' éthanolamine peut avoir lieu dans trois voies parallèles, où trois consécutifs N méthylation étapes catalysées par une méthyl transférase sont effectués soit sur la base libre, phospho-bases, ou la phosphatidyl-bases. La source du groupe méthyle est la S- adénosyl- L- méthionine et la S- adénosyl- L- homocystéine est générée en tant que produit secondaire.
Chez l'homme et la plupart des autres animaux, la synthèse de novo de la choline se fait par la voie de la phosphatidyléthanolamine N-méthyltransférase (PEMT), mais la biosynthèse n'est pas suffisante pour répondre aux besoins humains. Dans la voie PEMT hépatique, le 3-phosphoglycérate (3PG) reçoit 2 groupes acyle de l' acyl-CoA formant un acide phosphatidique . Il réagit avec la cytidine triphosphate pour former la cytidine diphosphate-diacylglycérol. Son groupe hydroxyle réagit avec la sérine pour former de la phosphatidylsérine qui se décarboxyle en éthanolamine et en phosphatidyléthanolamine (PE). Une enzyme PEMT déplace trois groupes méthyle de trois donneurs de S- adénosylméthionines (SAM) vers le groupe éthanolamine de la phosphatidyléthanolamine pour former de la choline sous la forme d'une phosphatidylcholine. Trois S- adénosylhomocystéines ( SAH ) sont formées comme sous-produit.
La choline peut également être libérée à partir de molécules contenant de la choline plus complexes. Par exemple, les phosphatidylcholines (PC) peuvent être hydrolysées en choline (Chol) dans la plupart des types cellulaires. La choline peut également être produite par la voie CDP-choline, les choline kinases cytosoliques (CK) phosphorylent la choline avec l' ATP en phosphocholine (PChol). Cela se produit dans certains types de cellules comme le foie et les reins. Les cytidylyltransférases choline-phosphate (CPCT) transforment le PChol en CDP-choline (CDP-Chol) avec la cytidine triphosphate (CTP). La CDP-choline et le diglycéride sont transformés en PC par la diacylglycérol cholinephosphotransférase (CPT).
Chez l'homme, certaines mutations de l' enzyme PEMT et une carence en œstrogènes (souvent due à la ménopause ) augmentent les besoins alimentaires en choline. Chez les rongeurs, 70 % des phosphatidylcholines sont formées par la voie PEMT et seulement 30 % par la voie CDP-choline. Chez les souris knock-out , l'inactivation de la PEMT les rend complètement dépendantes de la choline alimentaire.
Absorption
Chez l'homme, la choline est absorbée par les intestins via la protéine membranaire SLC44A1 (CTL1) via une diffusion facilitée régie par le gradient de concentration de choline et le potentiel électrique à travers les membranes des entérocytes . SLC44A1 a une capacité limitée à transporter la choline : à des concentrations élevées, une partie de celle-ci n'est pas absorbée. La choline absorbée quitte les entérocytes par la veine porte , traverse le foie et entre dans la circulation systémique . Les microbes intestinaux dégradent la choline non absorbée en triméthylamine , qui est oxydée dans le foie en N- oxyde de triméthylamine .
La phosphocholine et les glycérophosphocholines sont hydrolysées via des phospholipases en choline, qui pénètre dans la veine porte. En raison de leur solubilité dans l'eau, certains d'entre eux s'échappent inchangés vers la veine porte. Les composés liposolubles contenant de la choline ( phosphatidylcholines et sphingomyélines ) sont soit hydrolysés par les phospholipases , soit pénètrent dans la lymphe incorporés dans les chylomicrons .
Transport
Chez l'homme, la choline est transportée sous forme de molécule libre dans le sang. Les phospholipides contenant de la choline et d'autres substances, comme les glycérophosphocholines, sont transportés dans les lipoprotéines sanguines . Les taux de choline dans le plasma sanguin chez les adultes en bonne santé à jeun sont de 7 à 20 micromoles par litre (μmol/l) et de 10 μmol/l en moyenne. Les niveaux sont régulés, mais l'apport et la carence en choline modifient ces niveaux. Les niveaux sont élevés pendant environ 3 heures après la consommation de choline. Les taux de phosphatidylcholine dans le plasma des adultes à jeun sont de 1,5 à 2,5 mmol/l. Sa consommation élève les niveaux de choline libre pendant environ 8 à 12 heures, mais n'affecte pas de manière significative les niveaux de phosphatidylcholine.
La choline est un ion hydrosoluble et nécessite donc que les transporteurs traversent les membranes cellulaires liposolubles . Trois types de transporteurs de choline sont connus :
- SLC5A7
- CTL : CTL1 ( SLC44A1 ), CTL2 ( SLC44A2 ) et CTL4 ( SLC44A4 )
- OCT : OCT1 ( SLC22A1 ) et OCT2 ( SLC22A2 )
Les SLC5A7 sont des transporteurs dépendants du sodium (Na + ) et de l' ATP . Ils ont une affinité de liaison élevée pour la choline, la transportent principalement vers les neurones et sont indirectement associés à la production d' acétylcholine . Leur fonction déficiente provoque une faiblesse héréditaire des muscles pulmonaires et autres chez l'homme via une carence en acétylcholine. Chez les souris knock-out , leur dysfonctionnement entraîne facilement la mort avec cyanose et paralysie .
Les CTL1 ont une affinité modérée pour la choline et la transportent dans presque tous les tissus, y compris les intestins, le foie, les reins, le placenta et les mitochondries . Les CTL1 fournissent de la choline pour la production de phosphatidylcholine et de triméthylglycine . Les CTL2 se produisent surtout dans les mitochondries de la langue, des reins, des muscles et du cœur. Ils sont associés à l' oxydation mitochondriale de la choline en triméthylglycine. Les CTL1 et les CTL2 ne sont pas associés à la production d'acétylcholine, mais transportent la choline ensemble via la barrière hémato-encéphalique . Seuls les CTL2 se produisent du côté cérébral de la barrière. Ils éliminent également l'excès de choline des neurones dans le sang. Les CTL1 se produisent uniquement du côté sanguin de la barrière, mais aussi sur les membranes des astrocytes et des neurones.
Les OCT1 et les OCT2 ne sont pas associés à la production d'acétylcholine. Ils transportent la choline avec une faible affinité. Les OCT1 transportent la choline principalement dans le foie et les reins ; OCT2 dans les reins et le cerveau.
Espace de rangement
La choline est stockée dans les membranes cellulaires et les organites sous forme de phospholipides et à l'intérieur des cellules sous forme de phosphatidylcholines et de glycérophosphocholines .
Excrétion
Même à des doses de choline de 2 à 8 g, peu de choline est excrétée dans l'urine chez l'homme. L'excrétion se fait via des transporteurs qui se produisent dans les reins (voir transport ). La triméthylglycine est déméthylée dans le foie et les reins en diméthylglycine (le tétrahydrofolate reçoit l'un des groupes méthyle). La méthylglycine se forme, est excrétée dans l'urine ou est déméthylée en glycine .
Fonction
La choline et ses dérivés ont de nombreuses fonctions chez l'homme et dans d'autres organismes. La fonction la plus notable est que la choline sert de précurseur synthétique pour d'autres composants cellulaires essentiels et molécules de signalisation, tels que les phospholipides qui forment les membranes cellulaires, le neurotransmetteur acétylcholine et l' osmorégulateur triméthylglycine ( bétaïne ). La triméthylglycine sert à son tour de source de groupes méthyle en participant à la biosynthèse de la S- adénosylméthionine .
Précurseur de phospholipide
La choline est transformée en différents phospholipides , comme les phosphatidylcholines et les sphingomyélines . Ceux-ci se trouvent dans toutes les membranes cellulaires et les membranes de la plupart des organites cellulaires . Les phosphatidylcholines sont une partie structurellement importante des membranes cellulaires. Chez l'homme, 40 à 50 % de leurs phospholipides sont des phosphatidylcholines.
Les phospholipides de la choline forment également des radeaux lipidiques dans les membranes cellulaires avec le cholestérol . Les radeaux sont des centres, par exemple pour les récepteurs et les enzymes de transduction du signal des récepteurs .
Les phosphatidylcholines sont nécessaires à la synthèse des VLDL : 70 à 95 % de leurs phospholipides sont des phosphatidylcholines chez l'homme.
La choline est également nécessaire à la synthèse du surfactant pulmonaire , qui est un mélange constitué principalement de phosphatidylcholines. Le surfactant est responsable de l'élasticité pulmonaire, c'est-à-dire de la capacité du tissu pulmonaire à se contracter et à se dilater. Par exemple, une carence en phosphatidylcholines dans les tissus pulmonaires a été liée au syndrome de détresse respiratoire aiguë .
Les phosphatidylcholines sont excrétées dans la bile et agissent avec les sels d' acides biliaires en tant que tensioactifs , aidant ainsi à l' absorption intestinale des lipides .
Synthèse d'acétylcholine
La choline est nécessaire pour produire l' acétylcholine . C'est un neurotransmetteur qui joue un rôle nécessaire dans la contraction musculaire , la mémoire et le développement neural , par exemple. Néanmoins, il y a peu d'acétylcholine dans le corps humain par rapport aux autres formes de choline. Les neurones stockent également la choline sous forme de phospholipides dans leurs membranes cellulaires pour la production d'acétylcholine.
Source de triméthylglycine
Chez l'homme, la choline est oxydée de manière irréversible dans les mitochondries hépatiques en glycine bétaïne aldéhyde par les choline oxydases . Celui-ci est oxydé par des bétaïne-aldéhyde déshydrogénases mitochondriales ou cytosoliques en triméthylglycine . La triméthylglycine est un osmorégulateur nécessaire . Il fonctionne également comme substrat pour l' enzyme BHMT , qui méthyle l' homocystéine en méthionine . Il s'agit d'un précurseur de la S- adénosylméthionine (SAM). SAM est un réactif commun dans les réactions de méthylation biologique . Par exemple, il méthyle les guanidines de l' ADN et certaines lysines des histones . Elle fait donc partie de l'expression des gènes et de la régulation épigénétique . Une carence en choline conduit ainsi à des niveaux élevés d'homocystéine et à une diminution des niveaux de SAM dans le sang.
Contenu dans les aliments
La choline est présente dans les aliments sous forme de molécule libre et sous forme de phospholipides , notamment sous forme de phosphatidylcholines . La choline est la plus élevée dans les abats et les jaunes d'œufs, bien qu'elle se trouve dans une moindre mesure dans les abats , les céréales , les légumes , les fruits et les produits laitiers . Les huiles de cuisson et autres graisses alimentaires contiennent environ 5 mg/100 g de choline totale. Aux États-Unis , les étiquettes des aliments expriment la quantité de choline dans une portion en pourcentage de la valeur quotidienne (% VQ) sur la base d' un apport adéquat de 550 mg/jour. 100 % de la valeur quotidienne signifie qu'une portion de nourriture contient 550 mg de choline.
Le lait maternel humain est riche en choline. L' allaitement exclusif correspond à environ 120 mg de choline par jour pour le bébé. L'augmentation de l'apport en choline de la mère augmente la teneur en choline du lait maternel et une faible consommation la diminue. Les préparations pour nourrissons peuvent contenir ou non suffisamment de choline. Dans l' UE et aux États - Unis , il est obligatoire d'ajouter au moins 7 mg de choline pour 100 kilocalories (kcal) à chaque préparation pour nourrissons. Dans l'UE, les niveaux supérieurs à 50 mg/100 kcal ne sont pas autorisés.
La triméthylglycine est un métabolite fonctionnel de la choline. Elle se substitue nutritionnellement à la choline, mais seulement partiellement. Des quantités élevées de triméthylglycine sont présentes dans le son de blé (1 339 mg/100 g), le germe de blé grillé (1 240 mg/100 g) et les épinards (600-645 mg/100 g), par exemple.
| Viandes | Des légumes | ||
|---|---|---|---|
| Bacon , cuit | 124,89 | Haricot, snap | 13.46 |
| Boeuf , paré, cuit | 78.15 | Betterave | 6.01 |
| Foie de boeuf poêlé | 418.22 | Brocoli | 40.06 |
| Poulet , rôti, avec la peau | 65,83 | chou de Bruxelles | 40,61 |
| Poulet, rôti, sans peau | 78,74 | Choux | 15h45 |
| Foie de poulet | 290.03 | Carotte | 8.79 |
| Cabillaud, atlantique | 83,63 | Chou-fleur | 39.10 |
| Boeuf haché , 75-85% maigre, grillé | 79,32–82,35 | Maïs doux , jaune | 21,95 |
| Longe de porc cuite | 102,76 | Concombre | 5,95 |
| Crevettes , en conserve | 70,60 | Laitue , iceberg | 6,70 |
| Produits laitiers (vache) | Laitue romaine | 9,92 | |
| Beurre , salé | 18,77 | Pois | 27.51 |
| Du fromage | 16.50–27.21 | Choucroute | 10,39 |
| Cottage cheese | 18.42 | Épinard | 22.08 |
| Lait , entier/écrémé | 14.29-16.40 | Patate douce | 13.11 |
| Crème fraîche | 20.33 | Tomate | 6,74 |
| Yaourt nature | 15h20 | Courgette | 9.36 |
| Céréales | Des fruits | ||
| Avoine son , cru | 58,57 | Pomme | 3,44 |
| Avoine , nature | 7.42 | Avocat | 14.18 |
| Riz, blanc | 2.08 | Banane | 9,76 |
| Riz, brun | 9.22 | Myrtille | 6.04 |
| Son de blé | 74,39 | Cantaloup | 7,58 |
| Germe de blé , grillé | 152.08 | Raisin | 7.53 |
| Autres | Pamplemousse | 5.63 | |
| Haricot, marine | 26,93 | Orange | 8.38 |
| Oeuf, poule | 251.00 | Pêche | 6.10 |
| Huile d'olive | 0,29 | Poire | 5.11 |
| Cacahuète | 52,47 | Prune | 9,66 |
| Soja , cru | 115,87 | fraise | 5.65 |
| Tofu , doux | 27.37 | Pastèque | 4.07 |
Valeurs quotidiennes
Le tableau suivant contient des sources de choline mises à jour pour refléter la nouvelle valeur quotidienne et les nouvelles étiquettes de la valeur nutritive et des suppléments. Il reflète les données du Département de l'agriculture des États-Unis, Service de recherche agricole. FoodData Central, 2019.
| Nourriture | Milligrammes (mg) par portion | Pourcentage DV* |
| Foie de boeuf , poêlé, 3 oz (85 g) | 356 | 65 |
| Egguf, dur, 1 gros œuf | 147 | 27 |
| Ronde de dessus de boeuf , maigre séparable seulement, braisée, 3 oz (85 g) | 117 | 21 |
| Soja , torréfié, 1 ⁄ 2 tasse | 107 | 19 |
| Poitrine de poulet, rôtie, 3 oz (85 g) | 72 | 13 |
| Boeuf, haché, 93% de viande maigre, grillé, 3 oz (85 g) | 72 | 13 |
| Morue de l'Atlantique , cuite, chaleur sèche, 3 oz (85 g) | 71 | 13 |
| Champignons, shiitake , cuits, morceaux de 1 ⁄ 2 tasse | 58 | 11 |
| Pommes de terre, rouges , cuites, chair et peau, 1 grosse pomme de terre | 57 | dix |
| Germe de blé , grillé, 1 oz (28 g) | 51 | 9 |
| Haricots, rognons , en conserve, 1 ⁄ 2 tasse | 45 | 8 |
| Quinoa , cuit, 1 tasse | 43 | 8 |
| Lait , 1% de matière grasse, 1 tasse | 43 | 8 |
| Yogourt , vanille, sans gras, 1 tasse | 38 | 7 |
| Choux de Bruxelles , bouillis, 1 ⁄ 2 tasse | 32 | 6 |
| Brocoli , haché, bouilli, égoutté, 1 ⁄ 2 tasse | 31 | 6 |
| Fromage cottage , sans gras, 1 tasse | 26 | 5 |
| Thon , blanc, en conserve dans l'eau, égoutté dans les solides, 3 oz (85 g) | 25 | 5 |
| Arachides , rôties à sec, 1 ⁄ 4 tasse | 24 | 4 |
| Chou - fleur , morceaux de 1 po (2,5 cm), bouillis, égouttés, 1 ⁄ 2 tasse | 24 | 4 |
| Pois, verts , bouillis, 1 ⁄ 2 tasse | 24 | 4 |
| Graines de tournesol , grillées à l'huile, 1 ⁄ 4 tasse | 19 | 3 |
| Riz, brun , à grains longs, cuit, 1 tasse | 19 | 3 |
| Pain, pita , blé entier, 1 gros ( 6+1 ⁄ 2 po ou 17 cm de diamètre) | 17 | 3 |
| Chou , bouilli, 1 ⁄ 2 tasse | 15 | 3 |
| Mandarine ( mandarine ), sections, 1 ⁄ 2 tasse | dix | 2 |
| Haricots, snap , crus, 1 ⁄ 2 tasse | 8 | 1 |
| Kiwi , cru, 1 ⁄ 2 tasse tranché | 7 | 1 |
| Carottes , crues, hachées, 1 ⁄ 2 tasse | 6 | 1 |
| Pommes , crues, avec la peau, coupées en quartiers ou hachées, 1 ⁄ 2 tasse | 2 | 0 |
DV = valeur quotidienne. La Food and Drug Administration (FDA) des États-Unis a mis au point des VQ pour aider les consommateurs à comparer la teneur en nutriments des aliments et des compléments alimentaires dans le contexte d'un régime alimentaire complet. La VQ pour la choline est de 550 mg pour les adultes et les enfants de 4 ans et plus. La FDA n'exige pas que les étiquettes des aliments indiquent la teneur en choline à moins que de la choline n'ait été ajoutée à l'aliment. Les aliments fournissant 20 % ou plus de la DV sont considérés comme des sources élevées d'un nutriment, mais les aliments fournissant des pourcentages inférieurs de la DV contribuent également à une alimentation saine.
Le FoodData Central du département américain de l'Agriculture (USDA) répertorie la teneur en éléments nutritifs de nombreux aliments et fournit une liste complète des aliments contenant de la choline classés par teneur en éléments nutritifs.
Recommandations diététiques
Les recommandations sont en milligrammes par jour (mg/jour). Les recommandations de l' Autorité européenne de sécurité des aliments (EFSA) sont des recommandations générales pour les pays de l' UE . L'EFSA n'a fixé aucune limite supérieure d'ingestion. Certains pays de l'UE peuvent avoir des recommandations plus spécifiques. Les recommandations de la National Academy of Medicine (NAM) s'appliquent aux États-Unis , en Australie et en Nouvelle-Zélande .
| Âge | Apport adéquat de l' EFSA | NAM américain apport adéquat | Niveaux d'apport supérieurs tolérables au NAM des États-Unis |
|---|---|---|---|
| Nourrissons et enfants | |||
| 0-6 mois | Non-établi | 125 | Non-établi |
| 7 à 12 mois | 160 | 150 | Non-établi |
| 1-3 ans | 140 | 200 | 1 000 |
| 4 à 6 ans | 170 | 250 | 1 000 |
| 7-8 ans | 250 | 250 | 1 000 |
| 9-10 ans | 250 | 375 | 1 000 |
| 11-13 ans | 340 | 375 | 2 000 |
| Mâles | |||
| 14 ans | 340 | 550 | 3 000 |
| 15-18 ans | 400 | 550 | 3 000 |
| 19+ ans | 400 | 550 | 3 500 |
| Femelles | |||
| 14 ans | 340 | 400 | 3 000 |
| 15-18 ans | 400 | 400 | 3 000 |
| 19+ ans | 400 | 425 | 3 500 |
| Si enceinte | 480 | 450 | 3 500 (3 000 si ≤18 ans) |
| Si allaiter | 520 | 550 | 3 500 (3 000 si ≤18 ans) |
Apport dans les populations
Douze enquêtes menées dans 9 pays de l' UE entre 2000 et 2011 ont estimé l'apport en choline des adultes dans ces pays à 269-468 milligrammes par jour. La prise était de 269 à 444 mg/jour chez les femmes adultes et de 332 à 468 mg/jour chez les hommes adultes. La prise était de 75 à 127 mg/jour chez les nourrissons, de 151 à 210 mg/jour chez les enfants de 1 à 3 ans, de 177 à 304 mg/jour chez les enfants de 3 à 10 ans et de 244 à 373 mg/jour chez les 10 à 18 ans. L'estimation moyenne de l'apport total en choline était de 336 mg/jour chez les adolescentes enceintes et de 356 mg/jour chez les femmes enceintes.
Une étude basée sur l' enquête NHANES 2009-2012 a estimé que l'apport en choline était trop faible dans certaines sous - populations américaines . L'apport était de 315,2 à 318,8 mg/j chez les enfants de 2 ans et plus entre cette période. Sur les 2 ans et plus, seulement15,6 ± 0,8 % des hommes et6,1 ± 0,6 % des femelles dépassaient l' apport adéquat (AS). L'IA a été dépassée de62,9 ± 3,1 % des 2 à 3 ans,45,4 ± 1,6 % des 4 à 8 ans,9,0 ± 1,0 % des 9 à 13 ans,1,8 ± 0,4 % des 14-18 et6,6 ± 0,5 % des 19+ ans. Le niveau d'apport supérieur n'a été dépassé dans aucune sous-population.
Une étude NHANES 2013-2014 de la population américaine a révélé que l'apport en choline des 2 à 19 ans était 256 ± 3,8 mg/jour et339 ± 3,9 mg/jour chez l'adulte de 20 ans et plus. L'admission était402 ± 6,1 mg/j chez l'homme de 20 ans et plus et 278 mg/j chez la femme de 20 ans et plus.
Carence
Signes et symptômes
La carence symptomatique en choline est rare chez l'homme. La plupart en tirent des quantités suffisantes dans l'alimentation et sont capables d'en biosynthétiser des quantités limitées. La carence symptomatique est souvent causée par certaines maladies ou par d'autres causes indirectes. Une carence sévère provoque des lésions musculaires et une stéatose hépatique non alcoolique , qui peut évoluer en cirrhose .
Outre les humains, la stéatose hépatique est également un signe typique de carence en choline chez d'autres animaux. Des saignements dans les reins peuvent également survenir chez certaines espèces. Ceci est soupçonné d'être dû à une carence en triméthylglycine dérivée de la choline , qui fonctionne comme un osmorégulateur .
Causes et mécanismes
La production d' œstrogènes est un facteur important qui prédispose les individus à une carence ainsi qu'à un faible apport alimentaire en choline. Les œstrogènes activent les enzymes PEMT productrices de phosphatidylcholine . Les femmes avant la ménopause ont des besoins alimentaires en choline inférieurs à ceux des hommes en raison de la production plus élevée d'œstrogènes des femmes. Sans thérapie oestrogénique , les besoins en choline des femmes post-ménopausées sont similaires à ceux des hommes. Certains polymorphismes mononucléotidiques (facteurs génétiques) affectant le métabolisme de la choline et du folate sont également pertinents. Certains microbes intestinaux dégradent également la choline plus efficacement que d'autres, ils sont donc également pertinents.
En cas de carence, la disponibilité des phosphatidylcholines dans le foie est diminuée - celles-ci sont nécessaires à la formation de VLDL . Ainsi , le transport des acides gras médiés par les VLDL hors du foie diminue, ce qui entraîne une accumulation de graisse dans le foie. D'autres mécanismes simultanés expliquant les lésions hépatiques observées ont également été suggérés. Par exemple, les phospholipides de la choline sont également nécessaires dans les membranes mitochondriales . Leur indisponibilité conduit à l'incapacité des membranes mitochondriales à maintenir un gradient électrochimique approprié , qui, entre autres, est nécessaire à la dégradation des acides gras via la β-oxydation . Le métabolisme des graisses dans le foie diminue donc.
Consommation excessive
Des doses excessives de choline peuvent avoir des effets indésirables. Des doses quotidiennes de 8 à 20 g de choline, par exemple, provoquent une hypotension artérielle , des nausées , de la diarrhée et une odeur corporelle semblable à celle du poisson . L'odeur est due à la triméthylamine (TMA) formée par les microbes intestinaux à partir de la choline non absorbée (voir triméthylaminurie ).
Le foie oxyde le TMA en triméthylamine N- oxyde (TMAO). Des niveaux élevés de TMA et de TMAO dans le corps ont été liés à un risque accru d' athérosclérose et de mortalité. Ainsi, une consommation excessive de choline a été supposée augmenter ces risques en plus de la carnitine , qui est également formée en TMA et TMAO par les bactéries intestinales. Cependant, il n'a pas été démontré que l'apport en choline augmente le risque de mourir de maladies cardiovasculaires . Il est plausible que des niveaux élevés de TMA et de TMAO ne soient qu'un symptôme d'autres maladies sous-jacentes ou de facteurs génétiques qui prédisposent les individus à une mortalité accrue. De tels facteurs peuvent ne pas avoir été correctement pris en compte dans certaines études observant la mortalité liée au niveau de TMA et de TMAO. La causalité peut être inversée ou confusionnelle et un apport important en choline pourrait ne pas augmenter la mortalité chez l'homme. Par exemple, la dysfonction rénale prédispose aux maladies cardiovasculaires , mais peut également diminuer l'excrétion de TMA et de TMAO.
Effets sur la santé
Fermeture du tube neural
Certaines études humaines ont montré qu'un faible apport maternel en choline augmentait considérablement le risque d' anomalies du tube neural (ATN) chez les nouveau-nés. Une carence en folate provoque également des ATN. La choline et le folate, interagissant avec la vitamine B 12 , agissent comme donneurs de méthyle à l' homocystéine pour former la méthionine , qui peut ensuite former la SAM ( S -adénosylméthionine ). SAM est le substrat de presque toutes les réactions de méthylation chez les mammifères. Il a été suggéré que la méthylation perturbée via SAM pourrait être responsable de la relation entre le folate et les MTN. Cela peut également s'appliquer à la choline. Certaines mutations qui perturbent le métabolisme de la choline augmentent la prévalence des ATN chez les nouveau-nés, mais le rôle de la carence en choline alimentaire reste incertain, à partir de 2015.
Maladies cardiovasculaires et cancer
Une carence en choline peut provoquer une stéatose hépatique , ce qui augmente le risque de cancer et de maladies cardiovasculaires . Une carence en choline diminue également la production de SAM, qui participe à la méthylation de l'ADN - cette diminution peut également contribuer à la cancérogenèse . Ainsi, la carence et son association avec de telles maladies ont été étudiées. Cependant, les études observationnelles de populations libres n'ont pas montré de manière convaincante une association entre un faible apport en choline et les maladies cardiovasculaires ou la plupart des cancers. Les études sur le cancer de la prostate sont contradictoires.
Cognition
Des études observant l'effet entre une consommation plus élevée de choline et la cognition ont été menées chez l'homme adulte, avec des résultats contradictoires. Des études similaires sur des nourrissons et des enfants humains ont été contradictoires et également limitées.
Développement périnatal
La grossesse et l'allaitement augmentent considérablement la demande de choline. Cette demande peut être satisfaite par une régulation à la hausse de la PEMT via l'augmentation des niveaux d' œstrogènes pour produire plus de choline de novo , mais même avec une activité PEMT accrue, la demande de choline est toujours si élevée que les réserves corporelles sont généralement épuisées. Ceci est illustré par l'observation que les souris Pemt −/− (souris dépourvues de PEMT fonctionnelle) avorteront au bout de 9 à 10 jours à moins qu'elles ne soient nourries avec de la choline supplémentaire.
Alors que les réserves maternelles de choline sont épuisées pendant la grossesse et l'allaitement, le placenta accumule la choline en pompant la choline contre le gradient de concentration dans les tissus, où elle est ensuite stockée sous diverses formes, principalement sous forme d' acétylcholine . Les concentrations de choline dans le liquide amniotique peuvent être dix fois plus élevées que dans le sang maternel.
Fonctions chez le fœtus
La choline est très demandée pendant la grossesse en tant que substrat pour la construction des membranes cellulaires (expansion rapide des tissus fœtaux et maternels), besoin accru de fragments à un carbone (un substrat pour la méthylation de l'ADN et d'autres fonctions), augmentant les réserves de choline dans les tissus fœtaux et placentaires , et pour une production accrue de lipoprotéines (protéines contenant des portions « graisses »). En particulier, on s'intéresse à l'impact de la consommation de choline sur le cerveau. Cela provient de l'utilisation de la choline comme matériau pour la fabrication de membranes cellulaires (en particulier pour la fabrication de phosphatidylcholine ). La croissance du cerveau humain est la plus rapide au cours du troisième trimestre de la grossesse et continue d'être rapide jusqu'à environ cinq ans. Pendant ce temps, la demande est forte pour la sphingomyéline , qui est fabriquée à partir de phosphatidylcholine (et donc de choline), car ce matériau est utilisé pour myéliniser (isoler) les fibres nerveuses . La choline est également demandée pour la production du neurotransmetteur acétylcholine , qui peut influencer la structure et l'organisation des régions du cerveau, la neurogenèse , la myélinisation et la formation des synapses . L'acétylcholine est même présente dans le placenta et peut aider à contrôler la prolifération et la différenciation cellulaires (augmentation du nombre de cellules et transformation des cellules multi-usages en fonctions cellulaires dédiées) et la parturition .
L'absorption de la choline dans le cerveau est contrôlée par un transporteur de faible affinité situé au niveau de la barrière hémato-encéphalique . Le transport se produit lorsque les concentrations plasmatiques de choline artérielle augmentent au-dessus de 14 μmol/l, ce qui peut se produire lors d'un pic de concentration de choline après la consommation d'aliments riches en choline. Les neurones , à l'inverse, acquièrent la choline par des transporteurs de haute et de faible affinité. La choline est stockée sous forme de phosphatidylcholine liée à la membrane, qui peut ensuite être utilisée pour la synthèse ultérieure du neurotransmetteur acétylcholine. L'acétylcholine est formée au besoin, traverse la synapse et transmet le signal au neurone suivant. Ensuite, l' acétylcholinestérase le dégrade et la choline libre est à nouveau absorbée par un transporteur de haute affinité dans le neurone.
Les usages
Le chlorure de choline et le bitartrate de choline sont utilisés dans les compléments alimentaires . Le bitartrate est utilisé plus souvent en raison de sa plus faible hygroscopicité . Certains sels de choline sont utilisés pour compléter le poulet , la dinde et certains autres aliments pour animaux . Certains sels sont également utilisés comme produits chimiques industriels : par exemple, en photolithographie pour éliminer la résine photosensible . Le théophyllinate de choline et le salicylate de choline sont utilisés comme médicaments, ainsi que des analogues structuraux , comme la méthacholine et le carbachol . Les cholines radiomarquées , comme la 11 C-choline , sont utilisées en imagerie médicale . D'autres sels commercialement utilisés comprennent le citrate de tricholine et le bicarbonate de choline .
Antagonistes et inhibiteurs
Des centaines d' antagonistes de la choline et d' inhibiteurs d'enzymes ont été développés à des fins de recherche. L'aminométhylpropanol est parmi les premiers utilisés comme outil de recherche. Il inhibe la synthèse de la choline et de la triméthylglycine . Il est capable d'induire une carence en choline qui à son tour entraîne une stéatose hépatique chez les rongeurs. La diéthanolamine est un autre de ces composés, mais aussi un polluant environnemental. La N- cyclohexylcholine inhibe l'absorption de la choline principalement dans le cerveau. L'hémicholinium-3 est un inhibiteur plus général, mais il inhibe également modérément les choline kinases . Des inhibiteurs plus spécifiques de la choline kinase ont également été développés. Il existe également des inhibiteurs de synthèse de la triméthylglycine : la carboxybutylhomocystéine est un exemple d' inhibiteur spécifique de la BHMT .
L' hypothèse cholinergique de la démence a non seulement conduit à des inhibiteurs médicinaux de l' acétylcholinestérase , mais aussi à une variété d' inhibiteurs de l' acétylcholine . Des exemples de tels produits chimiques de recherche inhibiteurs comprennent la triéthylcholine , l' homocholine et de nombreux autres dérivés N- éthyliques de la choline, qui sont de faux analogues de neurotransmetteurs de l'acétylcholine. Des inhibiteurs de la choline acétyltransférase ont également été développés.
Histoire
Découverte
En 1849, Adolph Strecker fut le premier à isoler la choline de la bile de porc . En 1852, L. Babo et M. Hirschbrunn extrayèrent la choline de graines de moutarde blanche et la nommèrent Sinkaline . En 1862, Strecker a répété son expérience avec la bile de porc et de bœuf, appelant la substance choline pour la première fois après le mot grec pour bile, cholé , et l'identifiant avec la formule chimique C 5 H 13 NO. En 1850, Théodore Nicolas Gobley extrait de la cervelle et des œufs de carpes une substance qu'il baptise lécithine d' après le mot grec désignant le jaune d' œuf , lekithos , démontrant en 1874 qu'il s'agit d'un mélange de phosphatidylcholines .
En 1865, Oscar Liebreich isola la « neurine » de cerveaux d'animaux. Les formules structurelles de l' acétylcholine et de la « neurine » de Liebreich ont été résolues par Adolf von Baeyer en 1867. Plus tard cette année-là, la « neurine » et la sindaline se sont avérées être les mêmes substances que la choline de Strecker. Ainsi, Bayer a été le premier à résoudre la structure de la choline. Le composé maintenant connu sous le nom de neurine n'est pas lié à la choline.
Découverte comme nutriment
Au début des années 1930, Charles Best et ses collègues ont noté que la stéatose hépatique chez les rats suivant un régime spécial et les chiens diabétiques pouvait être évitée en les nourrissant de lécithine , prouvant en 1932 que la choline contenue dans la lécithine était la seule responsable de cet effet préventif. En 1998, l' Académie nationale de médecine des États-Unis a publié ses premières recommandations concernant la choline dans l'alimentation humaine.
Les références


