Connexine - Connexin
| Connexine | |||||||||
|---|---|---|---|---|---|---|---|---|---|
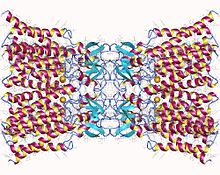 Dodécamère Connexin-26. Une jonction lacunaire, composée de douze protéines connexines identiques, six dans la membrane de chaque cellule. Chacune de ces six unités est un seul polypeptide qui traverse la membrane quatre fois (appelées protéines transmembranaires à quatre passes).
| |||||||||
| Identifiants | |||||||||
| symbole | Connexine | ||||||||
| Pfam | PF00029 | ||||||||
| InterPro | IPR013092 | ||||||||
| PROSITE | PDOC00341 | ||||||||
| TCDB | 1.A.24 | ||||||||
| superfamille OPM | 194 | ||||||||
| protéine OPM | 2zw3 | ||||||||
| |||||||||
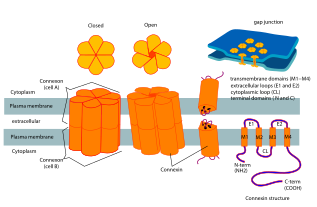
Les connexines ( Cx ) ( TC# 1.A.24 ), ou protéines de jonction lacunaire , sont des protéines transmembranaires structurellement apparentées qui s'assemblent pour former des jonctions lacunaires chez les vertébrés. Une famille entièrement différente de protéines, les innexines , forment des jonctions lacunaires chez les invertébrés . Chaque jonction lacunaire est composée de deux hémicanaux, ou connexons , qui consistent en des réseaux homo- ou hétérohexamériques de connexines, et le connexon d'une membrane plasmique s'arrime bout à bout avec un connexon dans la membrane d'une cellule étroitement opposée. L'hémicanal est composé de six sous-unités de connexine, chacune constituée de quatre segments transmembranaires. Les jonctions lacunaires sont essentielles pour de nombreux processus physiologiques, tels que la dépolarisation coordonnée du muscle cardiaque , le développement embryonnaire approprié et la réponse conduite dans la microvascularisation. Pour cette raison, des mutations dans les gènes codant pour la connexine peuvent entraîner des anomalies fonctionnelles et développementales.
Nomenclature
Les connexines sont communément nommées en fonction de leur poids moléculaire, par exemple Cx26 est la protéine connexine de 26 kDa. Une nomenclature concurrente est le système de protéines de jonction lacunaire , où les connexines sont triées par leurs formes (GJA) et (GJB), avec des connexines supplémentaires regroupées dans les groupes C, D et E, suivis d'un numéro d'identification, par exemple GJA1 correspond à Cx43. Suite à un vote lors de la conférence Gap Junction (2007) à Elseneur, la communauté a accepté d'utiliser le système de nomenclature GJ pour les gènes qui codent les connexines, mais a souhaité conserver la nomenclature des connexines pour les protéines codées en utilisant le poids de la protéine humaine pour la numérotation de protéines orthologues.
Structure
Les connexines contiennent quatre segments transmembranaires hautement ordonnés (TMS), principalement des extrémités cytoplasmiques C et N non structurées, une boucle cytoplasmique (CL) et deux boucles extracellulaires, (EL-1) et (EL-2). Les connexines sont assemblées par groupes de six pour former des hémicanaux, ou connexons, et deux hémicanaux se combinent ensuite pour former une jonction lacunaire.
La structure cristalline du canal de jonction lacunaire formé par le Cx26 humain (également connu sous le nom de GJB2) à une résolution de 3,5 Å est disponible. La carte de densité montrait les deux hémicanaux transmembranaires et la disposition des quatre TMS des six protomères formant chaque hémicanal. Les hémicanaux présentent une entrée cytoplasmique chargée positivement, un entonnoir, une voie transmembranaire chargée négativement et une cavité extracellulaire. Le pore est rétréci au niveau de l'entonnoir, qui est formé par les six hélices amino-terminales tapissant la paroi du canal, ce qui détermine ainsi la restriction de taille moléculaire à l'entrée du canal.
La famille des gènes de la connexine est diversifiée, avec vingt et un membres identifiés dans le génome humain séquencé et vingt chez la souris (dont dix-neuf paires orthologues). Ils pèsent généralement entre 25 et 60 kDa et ont une longueur moyenne de 380 acides aminés. Il a été observé que les diverses connexines se combinent en jonctions communicantes homomères et hétéromères, chacune pouvant présenter des propriétés fonctionnelles différentes, notamment la conductance des pores, la sélectivité de la taille, la sélectivité de la charge, le voltage dépendant et le déclenchement chimique.
Biosynthèse et internalisation
Un aspect remarquable des connexines est qu'elles ont une demi-vie relativement courte de quelques heures seulement. Le résultat est la présence d'un cycle dynamique par lequel les connexines sont synthétisées et remplacées. Il a été suggéré que cette courte durée de vie permet des processus physiologiques plus finement régulés, comme dans le myomètre .
Du noyau à la membrane
Lors de leur traduction par les ribosomes, les connexines sont insérées dans la membrane du réticulum endoplasmique (RE). C'est dans le RE que les connexines sont correctement repliées, donnant deux boucles extracellulaires, EL-1 et EL-2. C'est également dans le RE que commence l' oligomérisation des molécules de connexine en hémicanaux, un processus qui peut également se poursuivre dans le compartiment intermédiaire UR-Golgi. Les arrangements de ces hémicanaux peuvent être homotypiques, hétérotypiques et combinés hétérotypique/hétéromérique. Après avoir quitté l' ER et traversé l' ERGIC , les connexines repliées entreront généralement dans le réseau cis- Golgi. Cependant, certaines connexines, telles que la Cx26, peuvent être transportées indépendamment du Golgi.
Ensemble de jonction d'espace
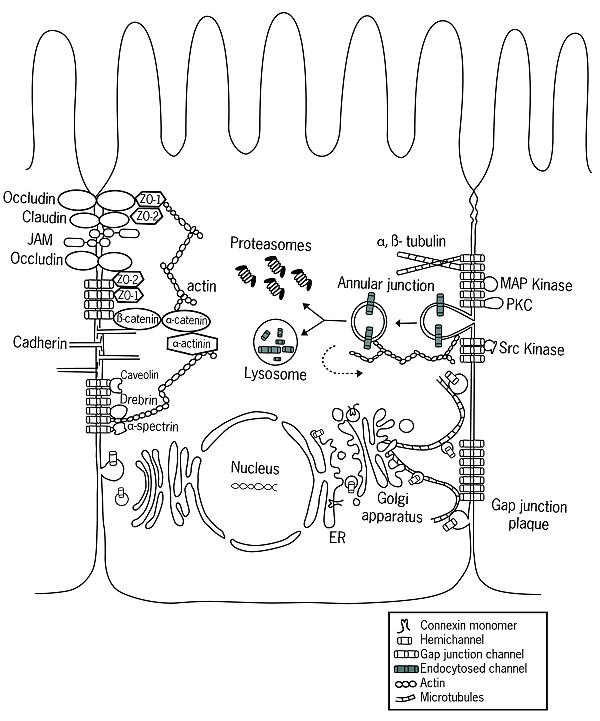
Après avoir été insérés dans la membrane plasmique de la cellule, les hémicanaux diffusent librement au sein de la bicouche lipidique. Grâce à l'aide de protéines spécifiques, principalement des cadhérines , les hémicanaux sont capables de s'arrimer aux hémicanaux de cellules adjacentes formant des jonctions communicantes. Des études récentes ont montré l'existence d'une communication entre les jonctions adhérentes et les jonctions lacunaires, suggérant un niveau de coordination plus élevé qu'on ne le pensait auparavant.
Une fonction
Les jonctions communicantes des connexines ne se trouvent que chez les vertébrés , tandis qu'un groupe de protéines fonctionnellement analogues (mais sans lien génétique), les innexines , sont responsables des jonctions communicantes chez les espèces d' invertébrés . Des orthologues d' Innexin ont également été identifiés dans les Chordés , mais ils ne sont plus capables de former des jonctions communicantes . Au lieu de cela, les canaux formés par ces protéines (appelées pannexines ) agissent comme de très grands pores transmembranaires qui relient les compartiments intra et extracellulaires.
Dans le SNC , les jonctions communicantes assurent le couplage électrique entre les cellules progénitrices, les neurones et les cellules gliales. En utilisant des souris knock-out pour les connexines spécifiques , des études ont révélé que le couplage cellulaire est essentiel pour la signalisation visuelle. Dans la rétine , les niveaux de lumière ambiante influencent le couplage cellulaire fourni par les canaux de jonction lacunaire, adaptant la fonction visuelle à diverses conditions d'éclairage. Le couplage cellulaire est régi par plusieurs mécanismes, dont l'expression des connexines.
Decrock et al. . ont discuté d'une plate-forme à plusieurs niveaux via laquelle les connexines et les pannexines peuvent influencer les fonctions cellulaires suivantes au sein d'un tissu : (1) les canaux jonctionnels de connexine (GJC) permettent la communication directe cellule-cellule de petites molécules, (2) les hémicanaux de connexine et les canaux de pannexine peuvent contribuer aux voies de signalisation autocrine / paracrine , et (3) différents domaines structuraux de ces protéines permettent des fonctions indépendantes des canaux, telles que l'adhésion cellule-cellule , les interactions avec le cytosquelette et l'activation des voies de signalisation intracellulaire. Ainsi, les connexines et les pannexines ont des contributions multiples au développement du cerveau et des processus spécifiques dans l'unité neuro-glio-vasculaire, y compris la transmission et la plasticité synaptique, la signalisation gliale, le contrôle vasomoteur et l'intégrité de la barrière hémato-encéphalique dans le SNC mature.
Spécificité du substrat
Différentes connexines peuvent présenter des spécificités différentes pour les solutés. Par exemple, l' adénosine passait environ 12 fois mieux à travers les canaux formés par Cx32 tandis que l' AMP et l' ADP passaient environ 8 fois mieux, et l' ATP plus de 300 fois mieux, à travers les canaux formés par Cx43. Ainsi, l'ajout de phosphate à l'adénosine semble déplacer sa perméabilité relative des canaux formés par Cx32 aux canaux formés par Cx43. Cela peut avoir des conséquences fonctionnelles car le statut énergétique d'une cellule pourrait être contrôlé via l'expression de la connexine et la formation de canaux.
Réaction de transport
La réaction de transport catalysée par les jonctions communicantes des connexines est :
- Petites molécules (cytoplasme de la cellule 1) ⇌ petites molécules (cytoplasme de la cellule 2)
Connexines humaines et implications dans la maladie
| Connexine | Gène | Emplacement et fonction |
|---|---|---|
| Cx43 | GJA1 | Exprimé à la surface du système vasculaire avec une plaque d'athérosclérose et régulé à la hausse pendant l'athérosclérose chez la souris. Peut avoir des effets pathologiques. Également exprimé entre les cellules de la granulosa , ce qui est nécessaire à la prolifération. Normalement exprimé dans les astrocytes, également détecté dans la plupart des astrocytomes humains et dans la composante astrogliale des tumeurs glioneuronales. C'est aussi la principale connexine cardiaque, trouvée principalement dans le myocarde ventriculaire. Associé à une dysplasie oculodentodigitale . |
| Cx46 | GJA3 | |
| Cx37 | GJA4 | Induite dans le muscle lisse vasculaire au cours de l'artériogenèse coronaire. Les mutations Cx37 ne sont pas mortelles. Forme des jonctions lacunaires entre les ovocytes et les cellules de la granulosa et est nécessaire à la survie des ovocytes. |
| Cx40 | GJA5 | Exprimé sélectivement dans les myocytes auriculaires. Responsable de la médiation de l'activation électrique coordonnée des oreillettes. |
| Cx33 |
GJA6 (GJA6P) |
Pseudogène chez l'homme |
| Cx50 | GJA8 | Jonctions lacunaires entre les cellules horizontales de type A dans la rétine de souris et de lapin |
| Cx59 | GJA10 | |
| Cx62 | GJA10 | Human Cx62 est conforme à Cx57 (souris). Localisation dans une cellule horizontale de type B portant des axones dans la rétine de lapin |
| Cx32 | GJB1 | Composant majeur de la myéline périphérique. Des mutations dans le gène humain provoquent la maladie de Charcot-Marie-Tooth liée à l'X , une neuropathie héréditaire. Dans le cerveau humain normal CX32 exprimé dans les neurones et les oligodendrocytes. |
| Cx26 | GJB2 | Muté dans le syndrome de Vohwinkel ainsi que dans le syndrome de kératite-ichtyose-surdité (KID) . |
| Cx31 | GJB3 | Peut être associé à Erythrokeratodermia variabilis . |
| Cx30.3 | GJB4 | Fonseca et al. a confirmé l'expression de Cx30.3 dans les thymocytes . Peut être associé à Erythrokeratodermia variabilis. |
| Cx31.1 | GJB5 | |
| Cx30 | GJB6 | Mutation dans le syndrome de Clouston (dysplasie ectodermique hydrotique) |
| Cx25 | GJB7 | |
| Cx45 | GJC1 /GJA7 | Cellules épithéliales canalaires pancréatiques humaines. Nœud auriculo-ventriculaire. |
| Cx47 | GJC2 /GJA12 | Exprimé dans les jonctions communicantes des oligodentrocytes |
| Cx31.3 | GJC3 | Orthologue humain du Cx29 murin. Pas connu pour former des jonctions communicantes. |
| Cx36 | GJD2 /GJA9 | Fonction des cellules bêta du pancréas, médiateur de la libération d'insuline. Les neurones dans tout le système nerveux central où ils synchronisent l'activité neuronale. |
| Cx31.9 | GJD3 /GJC1 | |
| Cx39 | GJD4 | |
| Cx40.1 | GJD4 | |
| Cx23 | GJE1 |
Les jonctions lacunaires sont essentielles pour de nombreux processus physiologiques, tels que la dépolarisation coordonnée du muscle cardiaque , le développement embryonnaire approprié et la réponse conduite dans la microvascularisation. Pour cette raison, la délétion ou la mutation des diverses isoformes de connexine produit des phénotypes et des pathologies distinctifs. Alors que les mutations de Cx43 sont principalement liées à la dysplasie oculodentodigitale, les mutations de Cx47 sont associées à une maladie de type Pelizaeus-Merzbacher et à un lymphœdème. Les mutations Cx40 sont principalement liées à la fibrillation auriculaire. Des mutations dans Cx37 n'ont pas encore été décrites, mais des polymorphismes dans le gène Cx37 ont été impliqués dans le développement de la maladie artérielle.
Les références
Liens externes
-
 Médias liés aux connexines sur Wikimedia Commons
Médias liés aux connexines sur Wikimedia Commons - Connexins à la National Library of Medicine Medical Subject Headings (MeSH) des États-Unis
À partir de cette modification , cet article utilise le contenu de "1.A.24 The Gap Junction-forming Connexin (Connexin) Family" , qui est concédé sous licence d'une manière qui permet la réutilisation sous la licence Creative Commons Attribution-ShareAlike 3.0 Unported , mais pas dans le cadre de la GFDL . Tous les termes pertinents doivent être respectés.