Groupe fonctionnel - Functional group
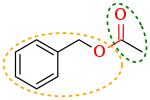
En chimie organique , un groupe fonctionnel est un substituant ou un fragment dans une molécule qui provoque les réactions chimiques caractéristiques de la molécule . Le même groupe fonctionnel subira des réactions chimiques identiques ou similaires quel que soit le reste de la composition de la molécule. Cela permet la prédiction systématique des réactions chimiques et du comportement des composés chimiques et la conception de la synthèse chimique . La réactivité d'un groupe fonctionnel peut être modifiée par d'autres groupes fonctionnels à proximité. L'interconversion des groupes fonctionnels peut être utilisée dans l'analyse rétrosynthétique pour planifier la synthèse organique .
Un groupe fonctionnel est un groupe d'atomes dans une molécule avec des propriétés chimiques distinctives , indépendamment des autres atomes de la molécule. Les atomes d'un groupe fonctionnel sont liés entre eux et au reste de la molécule par des liaisons covalentes . Pour les unités répétitives des polymères , les groupes fonctionnels se fixent à leur noyau non polaire d' atomes de carbone et ajoutent ainsi un caractère chimique aux chaînes carbonées. Des groupes fonctionnels peuvent également être chargés , par exemple dans des sels carboxylates (–COO − ), qui transforment la molécule en un ion polyatomique ou un ion complexe . Les groupes fonctionnels se liant à un atome central dans un complexe de coordination sont appelés ligands . La complexation et la solvatation sont également causées par des interactions spécifiques de groupes fonctionnels. Dans la règle empirique commune « comme dissout comme », ce sont les groupes fonctionnels partagés ou interagissant mutuellement bien qui donnent lieu à la solubilité . Par exemple, le sucre se dissout dans l'eau car les deux partagent le groupe fonctionnel hydroxyle (-OH) et les hydroxyles interagissent fortement les uns avec les autres. De plus, lorsque les groupes fonctionnels sont plus électronégatifs que les atomes auxquels ils se fixent, les groupes fonctionnels deviennent polaires et les molécules par ailleurs non polaires contenant ces groupes fonctionnels deviennent polaires et deviennent ainsi solubles dans un environnement aqueux .
La combinaison des noms de groupes fonctionnels avec les noms des alcanes parents génère ce que l'on appelle une nomenclature systématique pour nommer les composés organiques . Dans la nomenclature traditionnelle, le premier atome de carbone après le carbone qui s'attache au groupe fonctionnel est appelé le carbone alpha ; le deuxième, le carbone bêta, le troisième, le carbone gamma, etc. S'il y a un autre groupe fonctionnel à un carbone, il peut être nommé avec la lettre grecque, par exemple, la gamma-amine dans l'acide gamma-aminobutyrique est sur le troisième carbone de la chaîne carbonée attachée au groupe acide carboxylique. Les conventions de l'IUPAC exigent un étiquetage numérique de la position, par exemple l'acide 4-aminobutanoïque. Dans les noms traditionnels, divers qualificatifs sont utilisés pour étiqueter les isomères , par exemple, l'isopropanol (nom IUPAC : propan-2-ol) est un isomère du n-propanol (propan-1-ol). Le terme fraction a un certain chevauchement avec le terme "groupe fonctionnel". Cependant, une fraction est une "moitié" entière d'une molécule, qui peut être seulement un seul groupe fonctionnel, mais aussi une unité plus grande constituée de plusieurs groupes fonctionnels. Par exemple, un « fragment aryle » peut être n'importe quel groupe contenant un cycle aromatique , quel que soit le nombre de groupes fonctionnels dudit aryle.
Tableau des groupes fonctionnels communs
Ce qui suit est une liste de groupes fonctionnels communs. Dans les formules, les symboles R et R' désignent généralement un hydrogène attaché, ou une chaîne latérale hydrocarbonée de n'importe quelle longueur, mais peuvent parfois se référer à n'importe quel groupe d'atomes.
Hydrocarbures
Les hydrocarbures sont une classe de molécules définie par des groupes fonctionnels appelés hydrocarbyles qui ne contiennent que du carbone et de l'hydrogène, mais dont le nombre et l'ordre des doubles liaisons varient. Chacun diffère par le type (et la portée) de la réactivité.
| Classe chimique | Grouper | Formule | Formule structurelle | Préfixe | Suffixe | Exemple |
|---|---|---|---|---|---|---|
| Hydrocarbure | Alkyle | R(CH 2 ) n H |
|
alkyle- | -ane |
 Éthane |
| Alcène | alcényle | R 2 C=CR 2 |
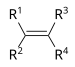
|
alcényle- | -ene |
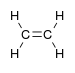 Éthylène (Éthène) |
| Alcyne | Alcynyle | RC≡CR' | alcynyle- | -yne |
Acétylène (Éthyne) |
|
| Dérivé du benzène | Phényle | RC 6 H 5 RPh |
|
phényle | -benzène |
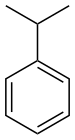 Cumène (Isopropylbenzène) |
Il existe également un grand nombre d'alcanes ramifiés ou cycliques qui ont des noms spécifiques, par exemple, tert-butyle , bornyle , cyclohexyle , etc. Les hydrocarbures peuvent former des structures chargées : carbocations chargés positivement ou carbanions négatifs . Les carbocations sont souvent nommés -um . Des exemples sont les cations tropylium et triphénylméthyle et l' anion cyclopentadiényle .
Groupes contenant des halogènes
Les haloalcanes sont une classe de molécules définies par une liaison carbone- halogène . Cette liaison peut être relativement faible (cas d'un iodoalcane) ou assez stable (cas d'un fluoroalcane). En général, à l'exception des composés fluorés , les haloalcanes subissent facilement des réactions de substitution nucléophile ou des réactions d'élimination . La substitution sur le carbone, l'acidité d'un proton adjacent, les conditions du solvant, etc. peuvent tous influencer le résultat de la réactivité.
| Classe chimique | Grouper | Formule | Formule structurelle | Préfixe | Suffixe | Exemple |
|---|---|---|---|---|---|---|
| haloalcane | Halo | Réception | Halo- | halogénure d' alkyle |
Chloroéthane (chlorure d'éthyle) |
|
| fluoroalcane | fluor | RF | fluoro- | fluorure d' alkyle |
 Fluorométhane (fluorure de méthyle) |
|
| chloroalcane | chloro | RCl | chloro- | chlorure d' alkyle |
 Chlorométhane (chlorure de méthyle) |
|
| bromoalcane | bromo | RBr | bromo- | bromure d' alkyle |
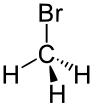 Brométhane (bromure de méthyle) |
|
| iodoalcane | iodo | IR | iodo- | iodure d' alkyle |
 Iodométhane (iodure de méthyle) |
Groupes contenant de l'oxygène
Les composés qui contiennent des liaisons CO possèdent chacun une réactivité différente en fonction de l'emplacement et de l' hybridation de la liaison CO, en raison de l'effet attracteur d'électrons de l'oxygène hybride sp (groupes carbonyle) et des effets donneurs de l' oxygène hybride sp 2 (groupes alcool) .
| Classe chimique | Grouper | Formule | Formule structurelle | Préfixe | Suffixe | Exemple |
|---|---|---|---|---|---|---|
| De l'alcool | hydroxyle | ROH | hydroxy- | -ol |
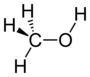 Méthanol |
|
| Cétone | Carbonyle | RCOR' |
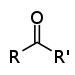
|
-oyl- (-COR') ou oxo- (=O) |
-une |
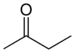 Butanone ( Méthyléthylcétone ) |
| Aldéhyde | Aldéhyde | RCHO |

|
formyl- (-COH) ou oxo- (=O) |
-Al |
 Acétaldéhyde (Éthanal) |
| halogénure d'acyle | Haloformyle | RCOX |

|
carbonofluoridoyl- carbonochloridoyl- carbonobromidoyl- carbonoiodidoyl- |
-oyl fluorure -oyl chlorure -oyl bromure -oyl iodure |
 Chlorure d'acétyle (chlorure d'éthanol) |
| Carbonate | Ester carbonaté | ROCOOR' |
|
(alcoxycarbonyl)oxy- | carbonate d' alkyle |
Triphosgène ( carbonate de bis(trichlorométhyle)) |
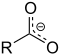
| Carboxylate | Carboxylate | RCOO − |
|
carboxy- | -avoine |
Acétate de sodium (Ethanoate de sodium) |
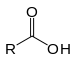
| Acide carboxylique | Carboxyle | RCOOH |
|
carboxy- | -oic acide |
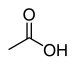 Acide acétique (acide éthanoïque) |
| Ester | Carboalcoxy | RCOOR' |
|
alcanoyloxy- ou alcoxycarbonyle |
alkyle alkan oate |
Butyrate d'éthyle (butanoate d'éthyle) |
| Hydroperoxyde | Hydroperoxy | ROOH |
|
hydroperoxy- | hydroperoxyde d' alkyle |
tert -butyl hydroperoxyde |
| Peroxyde | Peroxy | ROOR' |
|
peroxy- | peroxyde d' alkyle |
Peroxyde de di-tert-butyle |
| Éther | Éther | ROR' | alcoxy- | éther d' alkyle |
Ether diéthylique (Ethoxyéthane) |
|
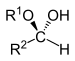
| Hémiacétal | Hémiacétal | R 2 CH(OU 1 )(OH) |
|
alcoxy-ol | -al alkyl hémiacétal | |
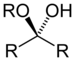
| Hémiketal | Hémiketal | RC(ORʺ)(OH)R' |
|
alcoxy-ol | -un alkyl hémicétal | |
| Acétal | Acétal | RCH(OU')(OU") |

|
dialcoxy- | -al dialkyl acétal | |
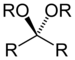
| Cétal (ou Acétal ) | Cétal (ou Acétal ) | RC(OU")(OU‴)R' |
|
dialcoxy- | -un dialkyl cétal | |
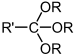
| Orthoester | Orthoester | RC(OU')(OU")(OU‴) |
|
trialcoxy- | ||
|
Hétérocycle (si cyclique) |
Méthylènedioxy | (–OCH 2 O–) | méthylènedioxy- | -dioxole |
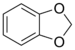 1,2-Méthylènedioxybenzène (1,3-Benzodioxole) |
|
| Ester d'orthocarbonate | Ester d'orthocarbonate | C(OU)(OU')(OU")(OU‴) |
|
tétralkoxy- | orthocarbonate de tétraalkyle |
 Tétraméthoxyméthane |
| Anhydride d'acide organique | Anhydride carboxylique | R 1 (CO)O(CO)R 2 |
|
anhydride |
Anhydride butyrique |
Groupes contenant de l'azote
Les composés qui contiennent de l'azote dans cette catégorie peuvent contenir des liaisons CO, comme dans le cas des amides .
| Classe chimique | Grouper | Formule | Formule structurelle | Préfixe | Suffixe | Exemple |
|---|---|---|---|---|---|---|
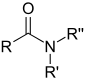
| Amide | Carboxamide | RCONR'R" |
|
carboxamido- ou carbamoyl- |
-amide |
 Acétamide (Éthanamide) |
| Amidine | Amidine | RC(NR)NR 2 |

|
-amidino | -amidine |
 acétamidine acétamidine
(acétimidamide) |
| Amines | Amine primaire | RNH 2 |
|
amino- | -amine |
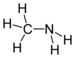 Méthylamine (Méthanamine) |
| Amine secondaire | R'R"NH |

|
amino- | -amine |
Diméthylamine |
|
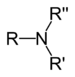
| Amine tertiaire | R 3 N |
|
amino- | -amine |
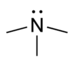 Triméthylamine |
|
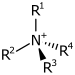
| 4° ion ammonium | R 4 N + |
|
ammoniac- | -ammonium |
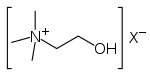 Choline |
|
| Imine | Cétimine primaire | RC(=NH)R' |
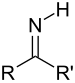
|
imino- | -imine | |
| Cétimine secondaire |
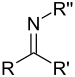
|
imino- | -imine | |||
| Aldimine primaire | RC(=NH)H |

|
imino- | -imine |
Ethanimine |
|
| Aldimine secondaire | RC(=NR')H |
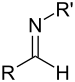
|
imino- | -imine | ||
| Imide | Imide | (RCO) 2 NR' |
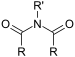
|
imido- | -imide |
 Succinimide (Pyrrolidine-2,5-dione) |
| Azide | Azide | RN 3 |
|
azido- | azoture d' alkyle |
 Azoture de phényle (Azidobenzène) |
| Composé azoïque |
Azo (Diimide) |
RN 2 R' |
|
azo- | -diazène |
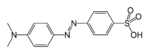 Orange de méthyle (acide p-diméthylamino-azobenzènesulfonique) |
| Cyanates | cyanate | ROCN |
|
cyanato- | cyanate d' alkyle |
cyanate de méthyle |
| Isocyanate | RNCO |
|
isocyanato- | isocyanate d' alkyle |
Isocyanate de méthyle |
|
| Nitrate | Nitrate | RONO 2 |
|
nitrooxy-, nitroxy- |
nitrate d' alkyle |
 Nitrate d'amyle (1-nitrooxypentane) |
| Nitrile | Nitrile | RCN | cyano- | cyanure d' alkyle alcane nitrile |
 Benzonitrile (cyanure de phényle) |
|
| Isonitrile | RNC | isocyano- | isocyanure d' alcane isonitrile alkyle |
Isocyanure de méthyle |
||
| Nitrite | Nitrosoxy | RONO |
|
nitrosooxy- |
nitrite d' alkyle |
 Nitrite d'isoamyle (3-méthyl-1-nitrosooxybutane) |
| Composé nitro | Nitro | RNO 2 |
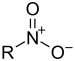
|
nitro- |
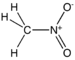 Nitrométhane |
|
| Composé nitroso | nitroso | RNO |
|
nitroso- (Nitrosyl-) |
Nitrosobenzène |
|
| Oxime | Oxime | RCH=NOH |
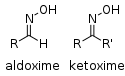
|
Oxime |
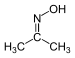 Acétone oxime (2-Propanone oxime) |
|
| Dérivé de pyridine | Pyridyle | RC 5 H 4 N |
4-pyridyle 3-pyridyle 2-pyridyle |
-pyridine |
 Nicotine |
|
| Ester de carbamate | Carbamate | RO(C=O)NR 2 |

|
(-carbamoyl)oxy- | -carbamate |
Chlorprophame (isopropyl (3-chlorophényl)carbamate) |
Groupes contenant du soufre
Les composés contenant du soufre présentent une chimie unique en raison de leur capacité à former plus de liaisons que l'oxygène, leur analogue plus léger dans le tableau périodique. La nomenclature de substitution (marquée comme préfixe dans le tableau) est préférée à la nomenclature des classes fonctionnelles (marquée comme suffixe dans le tableau) pour les sulfures, disulfures, sulfoxydes et sulfones.
| Classe chimique | Grouper | Formule | Formule structurelle | Préfixe | Suffixe | Exemple |
|---|---|---|---|---|---|---|
| Thiol | sulfhydryle | RSH |
|
sulfanyle- (-SH) |
- thiol |
Éthanethiol |
|
Sulfure ( thioéther ) |
Sulfure | RSR' |
|
substituant sulfanyle- (-SR') |
di( substituant ) sulfure |
(Méthylsulfanyl)méthane (préfixe) ou sulfure de diméthyle (suffixe) |
| disulfure | disulfure | RSSR' |
|
substituant disulfanyl- (-SSR') |
di( substituant ) disulfure |
(Méthyldisulfanyl)méthane (préfixe) ou Diméthyldisulfure (suffixe) |
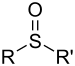
| Sulfoxyde | Sulfinyle | RSOR' |
|
-sulfinyl- (-SOR') |
di( substituant ) sulfoxyde |
 (Méthanesulfinyl)méthane (préfixe) ou Diméthylsulfoxyde (suffixe) |
| sulfone | Sulfonyle | RSO 2 R' |

|
-sulfonyle- (-SO 2 R') |
di( substituant ) sulfone |
(Méthanesulfonyl)méthane (préfixe) ou Diméthylsulfone (suffixe) |
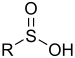
| Acide sulfinique | sulfino | RSO 2 H |
|
sulfino- (- SO 2 H) |
- acide sulfinique |
Acide 2-aminoéthanesulfinique |
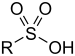
| Acide sulfonique | Sulfo | RSO 3 H |
|
sulfo- (- SO 3 H) |
- acide sulfonique |
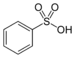 Acide benzènesulfonique |
| Ester sulfonate | Sulfo | RSO 3 R' |
|
(-sulfonyl)oxy- ou alcoxysulfonyl- |
R' R - sulfonate |
Trifluorométhanesulfonate de méthyle ou méthoxysulfonyl trifluorométhane (préfixe) |
| Thiocyanate | Thiocyanate | RSCN |
|
thiocyanato- (-SCN) |
substituant thiocyanate |
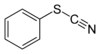 thiocyanate de phényle |
| Isothiocyanate | RNCS |
|
isothiocyanato- (-NCS) |
substituant isothiocyanate |
Isothiocyanate d'allyle |
|
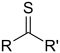
| Thioketone | Carbonothioyle | RCSR' |
|
-thioyl- (-CSR') ou sulfanylidène- (=S) |
- le thione |
Diphénylméthanethione ( Thiobenzophénone ) |
| Thial | Carbonothioyle | RCSH |

|
méthanethioyl- (-CSH) ou sulfanylidene- (=S) |
- thial | |
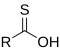
| Acide thiocarboxylique | Acide S carbothioique | RC=SST | mercaptocarbonyl- | - thioique S - acide |
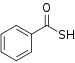 Acide thiobenzoïque ( acide benzothioique S ) |
|
| Carbothioïque O -acide | RC=SOH | hydroxy(thiocarbonyle)- | - thioique O - acide | |||
| Thioester | Thiolester | RC=OSR' |
|
S -alkyl-alcane- thioate |
S-méthyl thioacrylate ( S -méthyl prop-2-ènethioate) |
|
| thionoester | RC=SOR' |
|
O -alkyl-alcane- thioate | |||
| Acide dithiocarboxylique | Acide carbodithioïque | RCS 2 H | dithiocarboxy- | - acide dithioïque |
 Acide dithiobenzoïque (acide benzènecarbodithioïque) |
|
| Ester d'acide dithiocarboxylique | Carbodithio | RC=SSR' |
|
- dithioate |
Groupes contenant du phosphore
Les composés qui contiennent du phosphore présentent une chimie unique en raison de leur capacité à former plus de liaisons que l'azote, leurs analogues plus légers dans le tableau périodique.
| Classe chimique | Grouper | Formule | Formule structurelle | Préfixe | Suffixe | Exemple |
|---|---|---|---|---|---|---|
|
Phosphine ( phosphane ) |
Phosphino | R 3 P |
|
phosphanyl- | -phosphane |
Méthylpropylphosphane |
| Acide phosphonique | Phosphono |
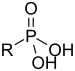
|
phosphono- | acide phosphonique substituant |
Acide benzylphosphonique |
|
| Phosphate | Phosphate |

|
phosphonooxy- ou O -phosphono- (phospho-) |
phosphate de substitution |
Glycéraldéhyde 3-phosphate (suffixe) |
|
|
O -Phosphonocholine (préfixe) ( Phosphocholine ) |
||||||
| Phosphodiester | Phosphate | HOPO(OU) 2 |
|
[(alcoxy)hydroxyphosphoryl]oxy- ou O -[(alcoxy)hydroxyphosphoryl]- |
di ( substituant ) hydrogène phosphate ou di acide phosphorique ( substituant ) ester |
ADN |
|
O ‑[(2‑guanidinoéthoxy)hydroxyphosphoryl]‑
l ‑sérine (préfixe) ( Lombricine ) |
Groupes contenant du bore
Les composés contenant du bore présentent une chimie unique en raison de leurs octets partiellement remplis et agissant donc comme des acides de Lewis .
| Classe chimique | Grouper | Formule | Formule structurelle | Préfixe | Suffixe | Exemple |
|---|---|---|---|---|---|---|
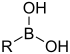
| Acide boronique | Borono | RB(OH) 2 | Borono- |
acide boronique substituant |
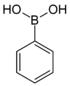 Acide phénylboronique |
|
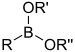
| Ester boronique | Boronate | RB(OU) 2 | O-[bis(alcoxy)alkylboronyl]- |
substituant acide boronique di( substituant ) ester |
||
| Acide borinique | Borino | R 2 BOH | Hydroxyborino- | acide di( substituant ) borinique |
||
| Ester borique | Borinate | R 2 BOR | O-[alcoxydialkylboronyl]- | ester de substituant d' acide borinique di( substituant ) |
 Ester 2-aminoéthylique de l'acide diphénylborinique ( borate de 2-aminoéthoxydiphényle ) |
Groupes contenant des métaux
| Classe chimique | Formule structurelle | Préfixe | Suffixe | Exemple |
|---|---|---|---|---|
| Alkyllithium | RLi | (tri/di)alkyle- | -lithium |
|
| Halogénure d'alkylmagnésium | RMgX (X=Cl, Br, I) | -halogénure de magnésium |
|
|
| Alkylaluminium | Al 2 R 6 | -aluminium |

|
|
| éther silylique | R 3 SiOR | -éther silylique |

|
note 1 Le fluorest trop électronégatif pour être lié au magnésium ; il devientplutôtunsel ionique.
Noms de radicaux ou de fragments
Ces noms sont utilisés pour désigner les fragments eux-mêmes ou des espèces radicalaires, et également pour former les noms d'halogénures et de substituants dans des molécules plus grosses.
Lorsque l'hydrocarbure parent est insaturé, le suffixe ("-yl", "-ylidène" ou "-ylidyne") remplace "-ane" (par exemple, "éthane" devient "éthyle"); sinon, le suffixe ne remplace que le "-e" final (par exemple, " éthyne " devient " éthynyle ").
Lorsqu'elles sont utilisées pour désigner des fragments, les liaisons simples multiples diffèrent d'une liaison multiple unique. Par exemple, un pont méthylène (méthanediyle) a deux liaisons simples, alors qu'un groupe méthylène (méthylidène) a une double liaison. Les suffixes peuvent être combinés, comme dans méthylidyne (triple liaison) vs méthylylidène (simple liaison et double liaison) vs méthanetriyle (trois doubles liaisons).
Certains noms ont été retenus, tels que méthylène pour méthanediyle, 1,x- phénylène pour phényl-1,x-diyle (où x est 2, 3 ou 4), carbyne pour méthylidyne et trityle pour triphénylméthyle.
| Classe chimique | Grouper | Formule | Formule structurelle | Préfixe | Suffixe | Exemple |
|---|---|---|---|---|---|---|
| Obligation simple | R• | Ylo- | -yl |
méthyle Radical méthyle |
||
| Double liaison | R : | ? | -ylidène |
|
||
| Triple liaison | R⫶ | ? | -ylidyne |
|
||
| radical acyle carboxylique | acyle | R−C(=O)• | ? | -oyl |
|
Voir également
Les références
Liens externes
- Livre bleu IUPAC (nomenclature biologique)
- "Abréviations de ligands IUPAC" (PDF) . IUPAC . 2 avril 2004. Archivé de l'original (PDF) le 27 septembre 2007 . Consulté le 25 février 2015 .
- Vidéo de groupe fonctionnel
- Synthèse de groupes fonctionnels de organic-reaction.com