Exostoses multiples héréditaires - Hereditary multiple exostoses
| Ostéochondromes multiples héréditaires | |
|---|---|
| Autres noms | Exostoses multiples héréditaires |
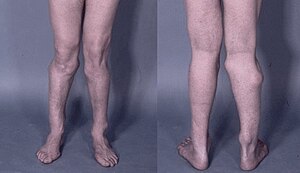 | |
| Photographie des jambes d'un homme de 26 ans montrant de multiples bosses entraînant une déformation. | |
| Spécialité |
Génétique médicale |
Les ostéochondromes multiples héréditaires ( HMO ), également appelés exostoses multiples héréditaires , sont une maladie caractérisée par le développement de multiples masses ostéocartilagineuses bénignes ( exostoses ) en relation avec les extrémités des os longs des membres inférieurs tels que les fémurs et les tibias et des membres supérieurs tels que l'humérus et les os de l'avant-bras. Ils sont également connus sous le nom d' ostéochondromes . Les autres sites d'occurrence comprennent les os plats tels que l'os pelvien et l'omoplate. La distribution et le nombre de ces exostoses montrent une grande diversité parmi les individus atteints. Exostoses généralement présentes pendant l'enfance. La grande majorité des personnes affectées deviennent cliniquement manifestes au moment où elles atteignent l'adolescence. Un petit pourcentage d'individus affectés est à risque de développer une transformation maligne, à savoir des sarcomes. L'incidence des exostoses multiples héréditaires est d'environ 1 individu sur 50 000. Les ostéochondromes multiples héréditaires sont le terme préféré utilisé par l' Organisation mondiale de la santé .
Présentation
Une grosseur perceptible par rapport à une extrémité peut être le premier symptôme de présentation. De multiples déformations peuvent survenir, à savoir des déformations du plan coronal autour des genoux, des chevilles, des épaules, des coudes et des poignets. Par exemple, le genu valgum (coup de genou), le valgus de la cheville, la courbure et le raccourcissement ulnaire et la subluxation de la tête radiale sont rencontrés. La majorité des personnes atteintes présentent des ostéochondromes cliniquement manifestes autour du genou. L'implication de l'avant-bras dans l'HMO est considérable. De plus, une petite taille peut survenir et est généralement disproportionnée. De telles manifestations résultent généralement d'une perturbation de la croissance de la physe, en particulier du fait que les ostéochondromes surviennent généralement aux extrémités métaphysaires des os longs à proximité immédiate de la physe. Les ostéochondromes intra-articulaires de la hanche peuvent induire une limitation de l'amplitude des mouvements, des douleurs articulaires et une dysplasie acétabulaire. De même, des douleurs articulaires à d'autres endroits et une compression neurovasculaire peuvent survenir. De plus, l'incapacité fonctionnelle en ce qui concerne les activités de la vie quotidienne peut être une caractéristique de présentation. Des douleurs de déformation rachidienne ou une atteinte neurologique doivent faire suspecter une atteinte des vertèbres.
Lien possible avec l'autisme
Certains parents d'enfants atteints d'EHM ont observé des problèmes sociaux de type autistique chez leurs enfants. Pour explorer ces observations plus en profondeur, une étude réalisée en 2012 par le Sanford-Burnham Medical Research Institute a utilisé un modèle murin de HME pour observer la fonction cognitive. Les résultats ont indiqué que les souris mutantes endossaient trois caractéristiques autistiques : une déficience sociale, des déficiences dans la vocalisation ultrasonore et un comportement répétitif.
La génétique
L'HME est une maladie héréditaire autosomique dominante . Cela signifie qu'un patient atteint d'EMH a 50% de chances de transmettre ce trouble à ses enfants. La plupart des personnes atteintes d'EHM ont un parent qui est également atteint de la maladie. Cependant, environ 10 à 20 % des personnes atteintes d'EHM souffrent de la maladie à la suite d'une mutation spontanée et sont donc la première personne de leur famille à être affectée.
L'HME a jusqu'à présent été liée à des mutations dans trois gènes :
- EXT1 qui correspond au chromosome 8q24.1
- EXT2 qui correspond à 11p13
- EXT3 qui correspond au bras court du chromosome 19 (bien que son emplacement exact n'ait pas encore été déterminé avec précision)
Des mutations dans ces gènes conduisent généralement à la synthèse d'une protéine EXT tronquée qui ne fonctionne pas normalement. On sait que les protéines EXT sont des enzymes importantes dans la synthèse de l' héparane sulfate ; cependant, le mécanisme exact par lequel la synthèse altérée du sulfate d'héparane qui pourrait conduire à la croissance osseuse anormale associée à l'HME n'est pas clair. On pense que la prolifération et la différenciation normales des chondrocytes peuvent être affectées, entraînant une croissance osseuse anormale. Les gènes HME étant impliqués dans la synthèse d'un glycane ( héparane sulfate ), l'HME peut être considéré comme un trouble congénital de la glycosylation selon la nouvelle nomenclature CDG proposée en 2009.
Pour les personnes atteintes d'EMH qui envisagent de fonder une famille, des tests génétiques préimplantatoires et un diagnostic prénatal sont disponibles pour déterminer si leur enfant à naître a hérité de la maladie. HME a une pénétrance de 96%, ce qui signifie que si le gène affecté est effectivement transmis à un enfant, l'enfant aura 96% de risque de manifester réellement la maladie et 4% de chance d'avoir la maladie mais de ne jamais la manifester. Le chiffre de 96% de pénétrance provient d'une seule étude. D'autres études ont observé à la fois une pénétrance incomplète et variable mais sans calculer le % de pénétrance, par ex. En effet, d'autres travaux ont montré que les garçons/hommes ont tendance à avoir une maladie plus grave que les femmes, ainsi que le nombre d'exostoses chez les membres touchés d'une même famille peut varier considérablement. Il est également possible que les femmes soient gravement touchées. La gravité des symptômes varie d'un individu à l'autre, même au sein d'une même famille.
Les symptômes sont plus susceptibles d'être graves si la mutation est sur le gène ext1 plutôt que sur ext2 ou ext3 ; ext1 est également le gène le plus fréquemment affecté chez les patients atteints de ce trouble.
Physiopathologie
Elle se caractérise par la croissance de tumeurs osseuses bénignes à coiffe cartilagineuse autour des zones de croissance osseuse active, en particulier la métaphyse des os longs. En règle générale, cinq ou six exostoses se trouvent dans les membres supérieurs et inférieurs. Les emplacements les plus courants sont :
L'HME peut entraîner un raccourcissement et une courbure des os ; les personnes atteintes ont souvent une petite taille. Selon leur localisation, les exostoses peuvent causer les problèmes suivants : douleur ou engourdissement dus à la compression nerveuse, atteinte vasculaire, inégalité de la longueur des membres, irritation des tendons et des muscles, déformation de Madelung ainsi qu'une amplitude de mouvement limitée au niveau des articulations sur lesquelles elles empiètent. . Une personne avec HME a un risque accru de développer une forme rare de cancer des os appelée chondrosarcome à l' âge adulte. Des problèmes peuvent survenir plus tard dans la vie et peuvent inclure des os faibles et des lésions nerveuses. Le taux de transformation signalé varie d'aussi peu que 0,57 % à 8,3 % des personnes atteintes d'EMH.
Diagnostic
Le diagnostic de HMO est basé sur l'établissement d'une corrélation précise entre les caractéristiques cliniques mentionnées ci-dessus et les caractéristiques radiographiques caractéristiques. Les antécédents familiaux peuvent fournir un indice important pour le diagnostic. Ceci est complété par des tests pour les deux gènes dans lesquels des variants pathogènes sont connus pour provoquer des HMO, à savoir EXT1 et EXT2. Une combinaison d'analyse de séquence et d'analyse de délétion de l'ensemble des régions codantes d'EXT1 et d'EXT2 détecte les variantes pathogènes chez 70 à 95 % des individus affectés. La caractéristique du diagnostic radiographique est la présence d'ostéochondromes aux extrémités métaphysaires des os longs dans lesquels le cortex et la moelle de l'ostéochondrome représentent une extension continue de l'os hôte. Ceci est facilement démontrable sur les radiographies des genoux.
Traitement
Les indications d'une intervention chirurgicale chez les personnes atteintes d'HMO restent floues et varient considérablement dans la littérature médicale. En général, le traitement chirurgical de l'HMO comprend une ou plusieurs des procédures suivantes : excision de l'ostéochondrome, allongement osseux progressif ou aigu tel que l'allongement du cubitus, ostéotomies correctives, hémiépiphysiodèse temporaire pour corriger les déformations articulaires angulaires telles que l'hémiépiphysiodèse du radius distal et l'hémiépiphysiodèse tibiale distale médiale. Néanmoins, il existe peu de preuves pour soutenir la pratique orthopédique pédiatrique en cours dans les ostéochondromes multiples héréditaires. Des revues systématiques récentes ont trouvé des preuves insuffisantes pour prouver que le traitement chirurgical en cours de l'HMO améliore considérablement la fonction ou pour prouver qu'il a un impact sur la qualité de vie des enfants affectés. Pour augmenter la quantité de preuves dans la littérature médicale, certaines recommandations ont été avancées. La construction d'études prospectives bien conçues qui peuvent fournir une relation plus claire entre les procédures chirurgicales, les caractéristiques des patients et les résultats est en forte demande. Sinon, suivre les modèles d'étude actuels continuera à soulever plus de questions que de réponses. L'arthroplastie totale de la hanche a été utilisée pour remédier aux HMO sévères et douloureuses de l'articulation de la hanche. L'arthroplastie totale de la hanche chez les personnes atteintes d'HMO est difficile en raison de la distorsion de l'anatomie et des chirurgies répétées effectuées pour traiter les plaintes liées à l'exostose.
Épidémiologie
On estime que l'EMH survient chez 1 personne sur 50 000.
Images supplémentaires
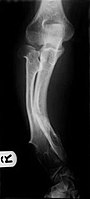
Ostéochondromes multiples provoquant une déformation de l'avant-bras (raccourcissement du radius avec courbure secondaire de l' ulna ).
Les références
Liens externes
| Classification | |
|---|---|
| Ressources externes |