Hexaméthylènetétramine - Hexamethylenetetramine
|
|
|||
| Noms | |||
|---|---|---|---|
|
Nom IUPAC préféré
1,3,5,7-tétraazaadamantane |
|||
| Autres noms
Hexamine; méthénamine;
Urotropine; Formine, Aminoforme |
|||
| Identifiants | |||
|
Modèle 3D ( JSmol )
|
|||
| 2018 | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| Banque de médicaments | |||
| Carte d'information de l'ECHA |
100.002.642 |
||
| Numéro CE | |||
| numéro E | E239 (conservateurs) | ||
| 26964 | |||
| KEGG | |||
| Engrener | Méthénamine | ||
|
CID PubChem
|
|||
| Numéro RTECS | |||
| UNII | |||
| Numéro ONU | 1328 | ||
|
Tableau de bord CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriétés | |||
| C 6 H 12 N 4 | |||
| Masse molaire | 140,186 g/mol | ||
| Apparence | Solide cristallin blanc | ||
| Odeur | Poisson, comme l'ammoniaque | ||
| Densité | 1,33 g / cm 3 (à 20 ° C) | ||
| Point de fusion | 280 °C (536 °F; 553 K) ( sublime ) | ||
| 85,3 g/100 ml | |||
| Solubilité | Soluble dans le chloroforme , le méthanol , l' éthanol , l' acétone , le benzène , le xylène , l' éther | ||
| Solubilité dans le chloroforme | 13,4 g/100 g (20 °C) | ||
| Solubilité dans le méthanol | 7,25 g/100 g (20 °C) | ||
| Solubilité dans l' éthanol | 2,89 g/100 g (20 °C) | ||
| Solubilité dans l' acétone | 0,65 g/100 g (20 °C) | ||
| Solubilité dans le benzène | 0,23 g/100 g (20 °C) | ||
| Acidité (p K a ) | 4.89 | ||
| Pharmacologie | |||
| J01XX05 ( OMS ) | |||
| Dangers | |||
| Principaux dangers | Hautement combustible, nocif | ||
| Pictogrammes SGH |
 
|
||
| Mention d'avertissement SGH | Avertissement | ||
| H228 , H317 | |||
| P210 , P240 , P241 , P261 , P272 , P280 , P302+352 , P321 , P333+313 , P363 , P370+378 , P501 | |||
| NFPA 704 (diamant de feu) | |||
| point de rupture | 250 °C (482 °F; 523 K) | ||
| 410 °C (770 °F; 683 K) | |||
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 °C [77 °F], 100 kPa). |
|||
|
|
|||
| Références de l'infobox | |||
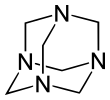
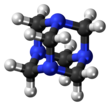
L'hexaméthylènetétramine , également connue sous le nom de méthénamine , hexamine ou urotropine , est un composé organique hétérocyclique de formule (CH 2 ) 6 N 4 . Ce composé cristallin blanc est très soluble dans l'eau et les solvants organiques polaires. Il a une structure en forme de cage similaire à l' adamantane . Il est utile dans la synthèse d'autres composés organiques, y compris les plastiques, les produits pharmaceutiques et les additifs pour caoutchouc. Il se sublime sous vide à 280°C.
Synthèse, structure, réactivité
L'hexaméthylènetétramine a été découverte par Aleksandr Butlerov en 1859. Elle est préparée industriellement en combinant du formaldéhyde et de l' ammoniac . La réaction peut être conduite en phase gazeuse et en solution.
La molécule a une structure en forme de cage tétraédrique , similaire à l' adamantane . Quatre sommets sont occupés par des atomes d' azote , qui sont liés par des groupes méthylène . Bien que la forme moléculaire définisse une cage, aucun espace vide n'est disponible à l'intérieur pour lier d'autres atomes ou molécules, contrairement aux éthers couronnes ou aux structures de cryptand plus grandes .
La molécule se comporte comme une base amine, subissant une protonation et une N - alkylation (par exemple Quaternium-15 ).
Applications
L'utilisation dominante de l'hexaméthylènetétramine est dans la production de préparations pulvérulentes ou liquides de résines phénoliques et de composés de moulage de résine phénolique , où elle est ajoutée en tant que composant durcissant. Ces produits sont utilisés comme liants, par exemple dans les garnitures de frein et d'embrayage, les produits abrasifs, les textiles non tissés, les pièces formées produites par des procédés de moulage et les matériaux ignifuges.
Utilisations médicales
En tant que sel d' acide mandélique (mandélate de méthénamine générique, USP), il est utilisé pour le traitement des infections des voies urinaires. Dans un environnement acide, on pense que la méthénamine agit comme un antimicrobien en se convertissant en formaldéhyde . Une revue systématique de son utilisation à cette fin chez les femmes adultes a révélé qu'il n'y avait aucune preuve solide de bénéfice.
La méthamine agit est un antisudorifique en vente libre en raison de la propriété astringente du formaldéhyde.
Taches histologiques
Les colorants à la méthénamine à l'argent sont utilisés pour la coloration en histologie , y compris les types suivants :
- Colorant à l'argent à la méthénamine de Grocott , largement utilisé comme écran pour les organismes fongiques .
- La coloration de Jones , une méthénamine argent -acide périodique-Schiff qui colore la membrane basale , permet de visualiser la membrane basale glomérulaire "à pointes" associée à la glomérulonéphrite membraneuse .
Combustible solide
Avec le 1,3,5-trioxane , l'hexaméthylènetétramine est un composant des comprimés de carburant à base d'hexamine utilisés par les campeurs, les amateurs, les militaires et les organisations de secours pour chauffer les aliments de camping ou les rations militaires. Il brûle sans fumée, a une densité énergétique élevée de 30,0 mégajoules par kilogramme (MJ/kg), ne se liquéfie pas en brûlant et ne laisse pas de cendres, bien que ses fumées soient toxiques.
Des comprimés normalisés de 0,149 g de méthénamine (hexamine) sont utilisés par les laboratoires de protection contre l'incendie comme source d'incendie propre et reproductible pour tester l'inflammabilité des tapis et moquettes.
Additif alimentaire
L'hexaméthylène tétramine ou l'hexamine est également utilisé comme additif alimentaire en tant que conservateur ( numéro SIN 239). Il est approuvé pour une utilisation à cette fin dans l'UE, où il est répertorié sous le numéro E E239, mais il n'est pas approuvé aux États-Unis, en Russie, en Australie ou en Nouvelle-Zélande.
Réactif en chimie organique
L'hexaméthylènetétramine est un réactif polyvalent en synthèse organique . Il est utilisé dans la réaction de Duff (formylation des arènes), la réaction de Sommelet (conversion des halogénures de benzyle en aldéhydes) et dans la réaction de Delépine (synthèse d'amines à partir d'halogénures d'alkyle).
Explosifs
L'hexaméthylènetétramine est le composant de base pour produire le RDX et, par conséquent, le C-4 ainsi que l' Octogen , le dinitrate d'hexamine, le diperchlorate d'hexamine et le HMTD .
Utilisations historiques
L'hexaméthylènetétramine a été introduite pour la première fois dans le milieu médical en 1899 comme antiseptique urinaire . Cependant, il n'était utilisé que dans les cas d'urines acides, alors que l'acide borique était utilisé pour traiter les infections des voies urinaires avec des urines alcalines . Le scientifique De Eds a découvert qu'il existait une corrélation directe entre l'acidité de l'environnement de l'hexaméthylènetétramine et la vitesse de sa décomposition. Par conséquent, son efficacité en tant que médicament dépendait grandement de l'acidité de l'urine plutôt que de la quantité de médicament administrée. Dans un environnement alcalin, l'hexaméthylènetétramine s'est avérée presque complètement inactive.
L'hexaméthylènetétramine a également été utilisée comme méthode de traitement pour les soldats exposés au phosgène pendant la Première Guerre mondiale . Des études ultérieures ont montré que de fortes doses d'hexaméthylènetétramine offrent une certaine protection si elles sont prises avant l'exposition au phosgène, mais aucune si elles sont prises après.
Producteurs
Depuis 1990, le nombre de producteurs européens est en baisse. L'usine française SNPE a fermé en 1990 ; en 1993, la production d'hexaméthylènetétramine à Leuna , en Allemagne, a cessé ; en 1996, l'usine italienne d'Agrolinz a fermé ; en 2001, le producteur britannique Borden a fermé ses portes ; en 2006, la production à Chemko, en République slovaque, a été fermée. Les autres producteurs sont INEOS en Allemagne, Caldic aux Pays-Bas et Hexion en Italie. Aux États-Unis, Eli Lilly and Company a cessé de produire des comprimés de méthénamine en 2002. En Australie, les comprimés d'Hexamine pour le carburant sont fabriqués par Thales Australia Ltd. Au Mexique, l'Hexamine est produit par Abiya.