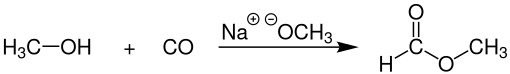Formiate de méthyle - Methyl formate
|
|
|||
| Des noms | |||
|---|---|---|---|
|
Nom IUPAC préféré
Formiate de méthyle |
|||
|
Nom IUPAC systématique
Méthanoate de méthyle |
|||
| Autres noms
R-611
|
|||
| Identifiants | |||
|
Modèle 3D ( JSmol )
|
|||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| Carte Info ECHA | 100.003.166 | ||
|
PubChem CID
|
|||
| UNII | |||
|
Tableau de bord CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriétés | |||
| C 2 H 4 O 2 | |||
| Masse molaire | 60,052 g · mol −1 | ||
| Apparence | Liquide incolore | ||
| Odeur | agréable | ||
| Densité | 0,98 g / cm 3 | ||
| Point de fusion | −100 ° C (−148 ° F; 173 K) | ||
| Point d'ébullition | 32 ° C (90 ° F; 305 K) | ||
| 30% (20 ° C) | |||
| La pression de vapeur | 634 hPa (476 mmHg) (20 ° C) | ||
| -32,0 · 10 -6 cm 3 / mol | |||
| Dangers | |||
| Fiche de données de sécurité | Oxford MSDS | ||
|
Classification UE (DSD) (obsolète)
|
Facilement inflammable (F +); Nocif (Xn) | ||
| point de rupture | −19 ° C; -2 ° F; 254 K | ||
| Limites explosives | 4,5% -23% | ||
| Dose ou concentration létale (DL, LC): | |||
|
DL 50 ( dose médiane )
|
1622 mg / kg (oral, lapin) | ||
|
LC Lo (le plus bas publié )
|
50000 ppm (cobaye, 20 min) | ||
| NIOSH (limites d'exposition pour la santé aux États-Unis): | |||
|
PEL (autorisé)
|
TWA 100 ppm (250 mg / m 3 ) | ||
|
REL (recommandé)
|
TWA 100 ppm (250 mg / m 3 ) ST 150 ppm (375 mg / m 3 ) | ||
|
IDLH (danger immédiat)
|
4500 ppm | ||
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Références Infobox | |||
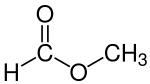
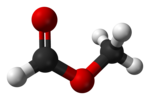
Le formiate de méthyle , également appelé méthanoate de méthyle , est l' ester méthylique de l'acide formique . L'exemple le plus simple d'un ester, c'est un liquide incolore avec une odeur éthérée, une pression de vapeur élevée et une faible tension superficielle . C'est un précurseur de nombreux autres composés d'intérêt commercial.
Production
En laboratoire, le formiate de méthyle peut être produit par la réaction de condensation du méthanol et de l'acide formique , comme suit:
- HCOOH + CH 3 OH → HCO 2 CH 3 + H 2 O
Le formiate de méthyle industriel, cependant, est généralement produit par la combinaison de méthanol et de monoxyde de carbone ( carbonylation ) en présence d'une base forte, telle que le méthylate de sodium :
Ce procédé, pratiqué commercialement par BASF parmi d'autres sociétés, donne une sélectivité de 96% envers le formiate de méthyle. Le catalyseur de ce procédé est sensible à l'eau, qui peut être présente dans la charge de monoxyde de carbone , qui est généralement dérivée du gaz de synthèse . Le monoxyde de carbone très sec est donc essentiel.
Les usages
Le formiate de méthyle est principalement utilisé pour fabriquer du formamide , du diméthylformamide et de l'acide formique . Ces composés sont des précurseurs ou des éléments constitutifs de nombreux dérivés utiles.
En raison de sa pression de vapeur élevée , il est utilisé pour les finitions à séchage rapide et comme agent gonflant pour certaines applications de mousse de polyuréthane et en remplacement des CFC , HCFC et HFC . Le formiate de méthyle a un potentiel d'appauvrissement de la couche d'ozone nul et un potentiel de réchauffement planétaire nul . Il est également utilisé comme insecticide .
Une utilisation historique du formiate de méthyle, qui attire parfois l'attention, était en réfrigération. Avant l'introduction de réfrigérants moins toxiques, le formiate de méthyle était utilisé comme alternative au dioxyde de soufre dans les réfrigérateurs domestiques, comme certains modèles du célèbre GE Monitor Top.