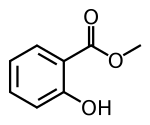
Le salicylate de méthyle - Methyl salicylate
|
|||
|
|
|||

|
|||
| Noms | |||
|---|---|---|---|
|
Nom IUPAC préféré
2-hydroxybenzoate de méthyle |
|||
| Autres noms | |||
| Identifiants | |||
|
Modèle 3D ( JSmol )
|
|||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| Carte d'information de l'ECHA |
100.003.925 |
||
| Numéro CE | |||
| KEGG | |||
|
CID PubChem
|
|||
| Numéro RTECS | |||
| UNII | |||
|
Tableau de bord CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriétés | |||
| C 8 H 8 O 3 | |||
| Masse molaire | 152,149 g/mol | ||
| Apparence | Liquide incolore | ||
| Odeur | Doux, enraciné | ||
| Densité | 1,174 g / cm 3 | ||
| Point de fusion | -8,6 °C (16,5 °F; 264,5 K) | ||
| Point d'ébullition | 222 °C (432 °F; 495 K) Se décompose à 340–350 °C |
||
| 0,639 g/L (21 °C) 0,697 g/L (30 °C) |
|||
| Solubilité | Miscible dans les solvants organiques | ||
| Solubilité dans l' acétone | 10,1 g/g (30 °C) | ||
| La pression de vapeur | 1 mmHg (54 °C) | ||
| Acidité (p K a ) | 9.8 | ||
| −8.630 × 10 −5 cm 3 /mol | |||
|
Indice de réfraction ( n D )
|
1.538 | ||
| Dangers | |||
| Principaux dangers | Nocif | ||
| Pictogrammes SGH |

|
||
| Mention d'avertissement SGH | Avertissement | ||
| H302 | |||
| P264 , P270 , P280 , P301+312 , P302+352 , P305+351+338 , P321 , P330 , P332+313 , P337+313 , P362 , P501 | |||
| NFPA 704 (diamant de feu) | |||
| point de rupture | 96 °C (205 °F; 369 K) | ||
| 452,7 °C (846,9 °F; 725,8 K) | |||
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 °C [77 °F], 100 kPa). |
|||
|
|
|||
| Références de l'infobox | |||
Le salicylate de méthyle ( huile de gaulthérie ou huile de gaulthérie ) est un composé organique de formule C 6 H 4 (OH) (CO 2 CH 3 ). C'est l' ester méthylique de l'acide salicylique . C'est un liquide incolore et visqueux avec une odeur sucrée et fruitée rappelant la racinette , mais souvent appelé associativement "menthe", car c'est un ingrédient des bonbons à la menthe. Il est produit par de nombreuses espèces de plantes , en particulier les gaulthéries . Il est également produit synthétiquement, utilisé comme parfum et comme agent aromatisant.
Biosynthèse et occurrence
Le salicylate de méthyle a été isolé pour la première fois (à partir de la plante Gaultheria procumbens ) en 1843 par le chimiste français Auguste André Thomas Cahours (1813-1891), qui l'a identifié comme un ester d' acide salicylique et de méthanol .
La biosynthèse du salicylate de méthyle se produit via l' hydroxylation de l'acide benzoïque par un cytochrome P450 suivie d'une méthylation par une enzyme méthylase .
Le salicylate de méthyle comme métabolite végétal
De nombreuses plantes produisent du salicylate de méthyle en petites quantités. Les niveaux de salicylate de méthyle sont souvent régulés à la hausse en réponse au stress biotique, en particulier l'infection par des agents pathogènes, où il joue un rôle dans l'induction de la résistance . On pense que le salicylate de méthyle fonctionne en étant métabolisé en acide salicylique, une hormone végétale. Étant donné que le salicylate de méthyle est volatil, ces signaux peuvent se propager dans l'air aux parties distales de la même plante ou même aux plantes voisines, après quoi ils peuvent fonctionner comme un mécanisme de communication plante-plante , "avertissant" les voisins du danger. Le salicylate de méthyle est également libéré dans certaines plantes lorsqu'elles sont endommagées par des insectes herbivores, où elles peuvent servir d'indice facilitant le recrutement de prédateurs.
Certaines plantes produisent du salicylate de méthyle en plus grande quantité, où il est probablement impliqué dans la défense directe contre les prédateurs ou les agents pathogènes. Des exemples de cette dernière classe comprennent : certaines espèces du genre Gaultheria dans la famille des Ericaceae , y compris Gaultheria procumbens , la gaulthérie ou le teaberry oriental ; certaines espèces du genre Betula de la famille des Betulaceae , en particulier celles du sous-genre Betulenta telles que B. lenta , le bouleau noir ; toutes les espèces du genre Spiraea de la famille des Rosacées , aussi appelées reines des prés ; espèce du genre Polygala de la famille des Polygalacées . Le salicylate de méthyle peut également être un composant des parfums floraux , en particulier chez les plantes dépendantes des pollinisateurs nocturnes comme les mites, les scarabées et les abeilles (nocturnes).
Fabrication commerciale
Le salicylate de méthyle peut être produit en estérifiant l'acide salicylique avec du méthanol . Le salicylate de méthyle commercial est maintenant synthétisé, mais dans le passé, il était couramment distillé à partir des brindilles de Betula lenta (bouleau doux) et de Gaultheria procumbens (thé rouge ou gaulthérie).
Les usages

Le salicylate de méthyle est utilisé à des concentrations élevées comme rubéfiant et analgésique dans les liniments chauffants en profondeur (comme le Bengay ) pour traiter les douleurs articulaires et musculaires. Des essais randomisés en double aveugle rapportent que les preuves de son efficacité sont faibles, mais plus fortes pour la douleur aiguë que pour la douleur chronique, et que l'efficacité peut être entièrement due à la contre-irritation . Cependant, dans l'organisme, il se métabolise en salicylates, dont l'acide salicylique, un AINS connu .
Le salicylate de méthyle est utilisé à de faibles concentrations (0,04 % et moins) comme agent aromatisant dans les chewing-gums et les menthes . Lorsqu'il est mélangé avec du sucre et séché, c'est une source potentiellement divertissante de triboluminescence , par exemple en écrasant les Wint-O-Green Life Savers dans une pièce sombre. Lorsqu'ils sont écrasés, les cristaux de sucre émettent de la lumière ; le salicylate de méthyle amplifie l'étincelle car il est fluorescent , absorbant la lumière ultraviolette et la réémettant dans le spectre visible. Il est utilisé comme antiseptique dans les bains de bouche Listerine produits par la société Johnson & Johnson . Il parfume divers produits et sert d'agent masquant les odeurs pour certains pesticides organophosphorés .
Le salicylate de méthyle est aussi utilisé comme un appât pour attirer les mâles abeilles d'orchidée pour l' étude, qui regroupent apparemment le produit chimique de phéromones de synthétiser et d'échantillons de tissus de plantes claires ou animales de couleur, et en tant que telle est utile pour la microscopie et l' immunohistochimie lorsque l' excès de pigments structures obscures ou bloquer la lumière dans le tissu examiné. Ce nettoyage ne prend généralement que quelques minutes, mais le tissu doit d'abord être déshydraté dans l'alcool. Il a également été découvert que le salicylate de méthyle fonctionne comme une kairomone qui attire certains insectes, tels que la mouche lanterne tachetée .
Les applications supplémentaires incluent : utilisé comme simulant ou substitut pour la recherche de l'agent de guerre chimique moutarde au soufre , en raison de ses propriétés chimiques et physiques similaires., dans la restauration (au moins temporairement) des propriétés élastomères des vieux rouleaux en caoutchouc, en particulier dans les imprimantes, comme un agent de transfert en gravure (pour libérer le toner des images photocopiées et les appliquer sur d'autres surfaces) et comme huile pénétrante pour détacher les pièces rouillées.
Sécurité et toxicité
Le salicylate de méthyle est potentiellement mortel, en particulier pour les jeunes enfants. Une seule cuillère à café (5 ml) de salicylate de méthyle contient environ 6 g de salicylate, ce qui équivaut à près de vingt comprimés d' aspirine à 300 mg (5 ml × 1,174 g/ml = 5,87 g). Des ingestions toxiques de salicylates se produisent généralement avec des doses d'environ 150 mg/kg de poids corporel. Ceci peut être réalisé avec 1 ml d'huile de gaulthérie, ce qui équivaut à 140 mg/kg de salicylates pour un enfant de 10 kg (22 lb). La dose létale la plus faible publiée est de 101 mg/kg de poids corporel chez l'homme adulte (ou 7,07 grammes pour un adulte de 70 kg). Il s'est avéré mortel pour les petits enfants à des doses aussi faibles que 4 ml. Une coureuse de fond de dix-sept ans à l' Académie Notre Dame de Staten Island est décédée en avril 2007 après que son corps ait absorbé du salicylate de méthyle suite à une utilisation excessive de produits topiques de soulagement des douleurs musculaires (en utilisant plusieurs patchs contre les instructions du fabricant).
La plupart des cas de toxicité humaine due au salicylate de méthyle sont le résultat d'une application excessive d'analgésiques topiques, en particulier chez les enfants. Le salicylate, le principal métabolite du salicylate de méthyle, peut s'accumuler dans le sang , le plasma ou le sérum pour confirmer un diagnostic d'empoisonnement chez les patients hospitalisés ou pour faciliter une autopsie .




