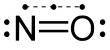L'oxyde nitrique - Nitric oxide

|
|||
|
|
|||
| Noms | |||
|---|---|---|---|
|
Nom IUPAC
L'oxyde nitrique
|
|||
|
Nom IUPAC systématique
Oxydoazote(•) (additif) |
|||
| Autres noms
Oxyde d'
azote Monoxyde d' azote Oxyde d' azote (II) Oxoazote |
|||
| Identifiants | |||
|
Modèle 3D ( JSmol )
|
|||
| 3DMet | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| Banque de médicaments | |||
| Carte d'information de l'ECHA |
100.030.233 |
||
| Numéro CE | |||
| 451 | |||
| KEGG | |||
|
CID PubChem
|
|||
| Numéro RTECS | |||
| UNII | |||
| Numéro ONU | 1660 | ||
|
Tableau de bord CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriétés | |||
| N O | |||
| Masse molaire | 30,006 g·mol -1 | ||
| Apparence | Gaz incolore | ||
| Densité | 1.3402 g/L | ||
| Point de fusion | −164 °C (−263 °F; 109 K) | ||
| Point d'ébullition | −152 °C (−242 °F; 121 K) | ||
| 0,0098 g/100 ml (0 °C) 0,0056 g/100 ml (20 °C) |
|||
|
Indice de réfraction ( n D )
|
1.0002697 | ||
| Structure | |||
| linéaire ( groupe Point C ∞ v ) | |||
| Thermochimie | |||
|
Entropie molaire standard ( S |
210,76 J/(K·mol) | ||
|
Std enthalpie de
formation (Δ f H ⦵ 298 ) |
91,29 kJ/mol | ||
| Pharmacologie | |||
| R07AX01 ( OMS ) | |||
| Données de licence | |||
| Inhalation | |||
| Pharmacocinétique : | |||
| bon | |||
| via lit capillaire pulmonaire | |||
| 2 à 6 secondes | |||
| Dangers | |||
| Principaux dangers | |||
| Fiche de données de sécurité | FDS externe | ||
| Pictogrammes SGH |
   
|
||
| Mention d'avertissement SGH | Danger | ||
| H270 , H280 , H330 , H314 | |||
| P244 , P260 , P220 , P280 , P304 + 340 + 315 , P303 + 361 + 353 + 315 , P305 + 351 + 338 + 315 , P370 + 376 , P403 , P405 | |||
| NFPA 704 (diamant de feu) | |||
| Dose ou concentration létale (LD, LC) : | |||
|
CL 50 ( concentration médiane )
|
315 ppm (lapin, 15 min ) 854 ppm (rat, 4 h ) 2500 ppm (souris, 12 min) |
||
|
LC Lo (le plus bas publié )
|
320 ppm (souris) | ||
| Composés apparentés | |||
|
Oxydes d'azote apparentés
|
Pentoxyde de diazote Tétroxyde de |
||
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 °C [77 °F], 100 kPa). |
|||
|
|
|||
| Références de l'infobox | |||
L'oxyde nitrique ( oxyde d'azote ou monoxyde d'azote) est un gaz incolore de formule NO . C'est l'un des principaux oxydes d'azote . L'oxyde nitrique est un radical libre : il possède un électron non apparié , qui est parfois désigné par un point dans sa formule chimique (·N=O ou ·NO). L'oxyde nitrique est également une molécule diatomique hétéronucléaire , une classe de molécules dont l'étude a engendré les premières théories modernes de la liaison chimique .
Intermédiaire important en chimie industrielle , l'oxyde nitrique se forme dans les systèmes de combustion et peut être généré par la foudre lors d'orages. Chez les mammifères, y compris les humains, l'oxyde nitrique est une molécule de signalisation dans de nombreux processus physiologiques et pathologiques. Il a été proclamé « Molécule de l'année » en 1992. Le prix Nobel de physiologie ou médecine 1998 a été décerné pour la découverte du rôle de l'oxyde nitrique en tant que molécule de signalisation cardiovasculaire.
Le monoxyde d'azote ne doit pas être confondu avec le dioxyde d'azote (NO 2 ), un gaz brun et polluant atmosphérique majeur , ni avec le protoxyde d'azote (N 2 O), un anesthésique .
Réactions
Avec des molécules di- et triatomiques
Lors de la condensation en un liquide, l'oxyde nitrique se dimérise en dioxyde de diazote , mais l'association est faible et réversible. La distance N–N dans le NO cristallin est de 218 pm, soit près du double de la distance N–O.
Puisque la chaleur de formation de ·NO est endothermique , NO peut être décomposé en éléments. Les convertisseurs catalytiques des voitures exploitent cette réaction :
- 2 NO → O 2 + N 2
Lorsqu'il est exposé à l' oxygène , le monoxyde d'azote se transforme en dioxyde d'azote :
- 2 NO + O 2 → 2 NO 2
Cette conversion a été supposée se produire via l'intermédiaire ONOONO.
Dans l'eau, l'oxyde nitrique réagit avec l'oxygène pour former de l'acide nitreux (HNO 2 ). On pense que la réaction se déroule via la stoechiométrie suivante :
- 4 NO + O 2 + 2 H 2 O → 4 HNO 2
L'oxyde nitrique réagit avec le fluor , le chlore et le brome pour former les halogénures de nitrosyle, tels que le chlorure de nitrosyle :
- 2 NO + Cl 2 → 2 NOCl
Avec NO 2 , également un radical, NO se combine pour former le trioxyde de diazote intensément bleu :
- NO + NO 2 ON−NO 2
Chimie organique
L'ajout d'un fragment d' oxyde nitrique à une autre molécule est souvent appelé nitrosylation . La réaction de Traube est l' ajout de deux équivalents d'oxyde nitrique sur un énolate , donnant un diazéniumdiolate (également appelé nitrosohydroxylamine ). Le produit peut subir une réaction rétro- aldolique ultérieure , donnant un processus global similaire à la réaction haloforme . Par exemple, l'oxyde nitrique réagit avec l' acétone et un alcoxyde pour former un diazéniumdiolate sur chaque position α , avec une perte subséquente d' acétate de méthyle comme sous-produit :
Cette réaction, découverte vers 1898, reste intéressante pour la recherche sur les prodrogues à base d' oxyde nitrique . L'oxyde nitrique peut également réagir directement avec le méthoxyde de sodium , formant finalement du formiate de sodium et de l'oxyde nitreux au moyen d'un N- méthoxydiazéniumdiolate.
Complexes de coordination
L'oxyde nitrique réagit avec les métaux de transition pour donner des complexes appelés nitrosyles métalliques . Le mode de liaison le plus courant de l'oxyde nitrique est le type linéaire terminal (M-NO). Alternativement, l'oxyde nitrique peut servir de pseudohalogénure à un électron. Dans de tels complexes, le groupe M-N-O est caractérisé par un angle compris entre 120° et 140°. Le groupe NO peut également établir un pont entre les centres métalliques via l'atome d'azote dans une variété de géométries.
Fabrication et préparation
Dans les milieux commerciaux, l'oxyde nitrique est produit par l' oxydation de l' ammoniac à 750-900 °C (normalement à 850 °C) avec du platine comme catalyseur dans le procédé d'Ostwald :
- 4 NH 3 + 5 O 2 → 4 NO + 6 H 2 O
La réaction endothermique non catalysée de l' oxygène (O 2 ) et de l' azote (N 2 ), qui est effectuée à haute température (> 2000 ° C) par la foudre n'a pas été développée en une synthèse commerciale pratique (voir processus Birkeland-Eyde ):
- N 2 + O 2 → 2 NON
Méthodes de laboratoire
En laboratoire, l'oxyde nitrique est commodément généré par réduction de l'acide nitrique dilué avec du cuivre :
- 8 HNO 3 + 3 Cu → 3 Cu(NO 3 ) 2 + 4 H 2 O + 2 NO
Une voie alternative consiste à réduire l'acide nitreux sous forme de nitrite de sodium ou de nitrite de potassium :
- 2 NaNO 2 + 2 NaI + 2 H 2 SO 4 → I 2 + 2 Na 2 SO 4 + 2 H 2 O + 2 NO
- 2 NaNO 2 + 2 FeSO 4 + 3 H 2 SO 4 → Fe 2 (SO 4 ) 3 + 2 NaHSO 4 + 2 H 2 O + 2 NO
- 3 KNO 2 + KNO 3 + Cr 2 O 3 → 2 K 2 CrO 4 + 4 NO
La voie du sulfate de fer (II) est simple et a été utilisée dans des expériences de laboratoire de premier cycle. Les composés dits NONOate sont également utilisés pour la génération d'oxyde nitrique.
Détection et dosage
La concentration d'oxyde nitrique peut être déterminée à l'aide d'une réaction chimiluminescente impliquant l' ozone . Un échantillon contenant de l'oxyde nitrique est mélangé à une grande quantité d'ozone. L'oxyde nitrique réagit avec l'ozone pour produire de l' oxygène et du dioxyde d'azote , accompagnés d'émission de lumière ( chimiluminescence ) :
- NO + O 3 → NO 2 + O 2 + hν
qui peut être mesuré avec un photodétecteur . La quantité de lumière produite est proportionnelle à la quantité d'oxyde nitrique dans l'échantillon.
D'autres méthodes de test incluent l' électroanalyse (approche ampérométrique), où ·NO réagit avec une électrode pour induire un changement de courant ou de tension. La détection des radicaux NO dans les tissus biologiques est particulièrement difficile en raison de la courte durée de vie et de la concentration de ces radicaux dans les tissus. L'une des rares méthodes pratiques est le piégeage par spin de l'oxyde nitrique avec des complexes fer- dithiocarbamate et la détection ultérieure du complexe mono-nitrosyl-fer avec la résonance paramagnétique électronique (RPE).
Il existe un groupe d' indicateurs de colorants fluorescents également disponibles sous forme acétylée pour les mesures intracellulaires. Le composé le plus courant est la 4,5-diaminofluorescéine (DAF-2).
Effets environnementaux
Dépôt de pluie acide
L'oxyde nitrique réagit avec le radical hydroperoxy (HO 2 • ) pour former du dioxyde d'azote (NO 2 ), qui peut ensuite réagir avec un radical hydroxyle ( • OH ) pour produire de l'acide nitrique (HNO 3 ) :
- ·NO + HO 2 • → • NO 2 + • OH
- ·NO 2 + • OH → HNO 3
L'acide nitrique, avec l'acide sulfurique , contribue au dépôt des pluies acides .
Appauvrissement de l'ozone
·NO participe à l' appauvrissement de la couche d'ozone . L'oxyde nitrique réagit avec l' ozone stratosphérique pour former de l'O 2 et du dioxyde d'azote :
- ·NO + O 3 → NO 2 + O 2
Cette réaction est également utilisée pour mesurer les concentrations de ·NO dans les volumes de contrôle.
Précurseur du NO 2
Comme vu dans la section Dépôts acides, le monoxyde d'azote peut se transformer en dioxyde d'azote (cela peut arriver avec le radical hydroperoxy, HO 2 • , ou l'oxygène diatomique, O 2 ). Les symptômes d'une exposition à court terme au dioxyde d'azote comprennent des nausées, une dyspnée et des maux de tête. Les effets à long terme pourraient inclure une altération des fonctions immunitaires et respiratoires .
Fonctions biologiques
Le NO est une molécule de signalisation gazeuse . C'est un messager biologique clé des vertébrés , jouant un rôle dans une variété de processus biologiques. C'est un bioproduit dans presque tous les types d'organismes, y compris les bactéries, les plantes, les champignons et les cellules animales.
L'oxyde nitrique, un facteur relaxant dérivé de l'endothélium (EDRF), est biosynthétisé de manière endogène à partir de la L- arginine , de l' oxygène et du NADPH par diverses enzymes de l'oxyde nitrique synthase (NOS) . La réduction du nitrate inorganique peut également produire de l'oxyde nitrique. L'une des principales cibles enzymatiques du monoxyde d'azote est la guanylyl cyclase . La liaison de l'oxyde nitrique à la région hème de l'enzyme conduit à l'activation, en présence de fer. L'oxyde nitrique est très réactif (ayant une durée de vie de quelques secondes), mais diffuse librement à travers les membranes. Ces attributs rendent l'oxyde nitrique idéal pour une molécule de signalisation transitoire paracrine (entre des cellules adjacentes) et autocrine (au sein d'une seule cellule). Une fois que l'oxyde nitrique est converti en nitrates et nitrites par l'oxygène et l'eau, la signalisation cellulaire est désactivée.
L' endothélium (revêtement interne) des vaisseaux sanguins utilise de l'oxyde nitrique pour signaler au muscle lisse environnant de se détendre, ce qui entraîne une vasodilatation et une augmentation du flux sanguin. Le sildénafil (Viagra) est un médicament qui utilise la voie de l'oxyde nitrique. Le sildénafil ne produit pas d'oxyde nitrique, mais améliore les signaux en aval de la voie de l'oxyde nitrique en protégeant la guanosine monophosphate cyclique (cGMP) de la dégradation par la phosphodiestérase de type 5 (PDE5) spécifique de la cGMP dans le corps caverneux , permettant au signal d'être amélioré, et donc la vasodilatation . Un autre transmetteur gazeux endogène, le sulfure d'hydrogène (H 2 S) travaille avec le NO pour induire la vasodilatation et l'angiogenèse de manière coopérative.
La respiration nasale produit de l'oxyde nitrique dans le corps, contrairement à la respiration buccale .
Sécurité et santé au travail
Aux États-Unis, l' Occupational Safety and Health Administration (OSHA) a fixé la limite légale (limite d' exposition admissible ) pour l'exposition à l'oxyde nitrique sur le lieu de travail à 25 ppm (30 mg/m 3 ) sur une journée de travail de 8 heures. L' Institut national pour la sécurité et la santé au travail (NIOSH) a fixé une limite d'exposition recommandée (REL) de 25 ppm (30 mg/m 3 ) sur une journée de travail de 8 heures. A des niveaux de 100 ppm, le monoxyde d'azote est immédiatement dangereux pour la vie et la santé .
Les références
Lectures complémentaires
- Butler A. et Nicholson R.; "La vie, la mort et NON." Cambridge 2003. ISBN 978-0-85404-686-7 .
- van Faassen, EE ; Vanin, AF (dir.); "Les radicaux pour la vie : Les différentes formes d'oxyde nitrique." Elsevier, Amsterdam 2007. ISBN 978-0-444-52236-8 .
- Ignarro, LJ (éd.); "Oxyde nitrique: biologie et pathobiologie." Presse académique, San Diego 2000. ISBN 0-12-370420-0 .
Liens externes
- Carte internationale de sécurité chimique 1311
- "L'oxyde nitrique et son rôle dans la santé et le diabète" . 21 octobre 2015.
- Chimie des gaz à micro-échelle : expériences avec des oxydes d'azote
- Votre cerveau démarre comme un ordinateur - de nouvelles informations sur le rôle biologique de l'oxyde nitrique.
- Évaluer le potentiel de l'oxyde nitrique dans le pied diabétique
- De nouvelles découvertes sur l'oxyde nitrique peuvent fournir des médicaments pour la schizophrénie
- Oxyde nitrique dans la base de données chimiques
- "Concentrations immédiatement dangereuses pour la vie ou la santé (IDLH) : oxyde nitrique" . Institut national pour la sécurité et la santé au travail . 2 novembre 2018.