Acétate d'octyle - Octyl acetate

|
|
|
|

|
|
| Noms | |
|---|---|
|
Nom IUPAC préféré
Acétate d'octyle |
|
| Autres noms
acétate de n- octyle
|
|
| Identifiants | |
|
Modèle 3D ( JSmol )
|
|
| ChEBI | |
| ChemSpider | |
| Carte d'information de l'ECHA |
100.003.581 |
|
CID PubChem
|
|
| Numéro RTECS | |
| UNII | |
|
Tableau de bord CompTox ( EPA )
|
|
|
|
|
|
| Propriétés | |
| C 10 H 20 O 2 | |
| Masse molaire | 172,268 g·mol -1 |
| Apparence | Liquide incolore |
| Odeur | Odeur florale fruitée légèrement cireuse |
| Densité | 0,863 à 0,87 g / cm 3 |
| Point de fusion | −38,5 à −38 °C (−37,3 à −36,4 °F; 234,7 à 235,2 K) |
| Point d'ébullition | 203 à 211,3 °C (397,4 à 412,3 °F ; 476,1 à 484,4 K) 112,55 °C (234,59 °F ; 385,70 K) à 30 mmHg |
| 0,021 g/100 g (0 °C) 0,018 g/100 g (29,7 °C) 0,018 g/100 g (40 °C) 0,012 g/100 g (92,1 °C) |
|
| Solubilité | Soluble dans EtOH , éther |
| La pression de vapeur | 0,01 kPa (−3 °C) 0,0072–0,0073 (14,75 °C) 0,02–0,1 kPa (27 °C) 1 kPa (66,3 °C) 10 kPa (120 °C) |
|
Indice de réfraction ( n D )
|
1,415-1,422 (20 °C) |
| Thermochimie | |
|
Capacité calorifique ( C )
|
331-343,74 J/mol·K |
| Dangers | |
| NFPA 704 (diamant de feu) | |
| point de rupture | 83 à 86 °C (181 à 187 °F ; 356 à 359 K) |
| 268 à 268,3 °C (514,4 à 514,9 °F ; 541,1 à 541,5 K) | |
| Limites d'explosivité | 0,76-8,14 % |
| Dose ou concentration létale (LD, LC) : | |
|
DL 50 ( dose médiane )
|
3000 mg/kg (oral, rat) 5000 mg/kg (cutané, lapin) |
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Références de l'infobox | |
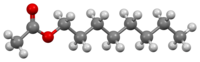
L'acétate d'octyle , ou éthanoate d'octyle, est un composé organique de formule CH 3 (CH 2 ) 7 O 2 CCH 3 . Il est classé comme un ester formé à partir de 1-octanol (alcool octylique) et d'acide acétique . On le trouve dans les oranges , les pamplemousses et autres agrumes .
L'acétate d'octyle peut être synthétisé par estérification de Fischer du 1-octanol et de l'acide acétique :
- CH 3 (CH 2 ) 7 OH + CH 3 CO 2 H → CH 3 (CH 2 ) 7 O 2 CCH 3 + H 2 O
Les usages
En raison de son odeur fruitée, l'acétate d'octyle est utilisé comme base d'arômes artificiels et en parfumerie. C'est aussi un solvant pour la nitrocellulose, les cires, les huiles et certaines résines.

