Ornithine - Ornithine
|
|
|
|
| Des noms | |
|---|---|
|
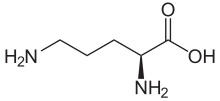
Nom IUPAC
L -Ornithine
|
|
| Autres noms
Acide (+) - ( S ) -2,5-diaminovalérique
(+) - ( S ) -2,5-diaminopentanoïque |
|
| Identifiants | |
|
Modèle 3D ( JSmol )
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| DrugBank | |
| Carte Info ECHA |
100 000,665 |
| Numéro CE | |
| KEGG | |
| Engrener | Ornithine |
|
PubChem CID
|
|
| UNII | |
|
Tableau de bord CompTox ( EPA )
|
|
|
|
|
|
| Propriétés | |
| C 5 H 12 N 2 O 2 | |
| Masse molaire | 132,16 g / mol |
| Point de fusion | 140 ° C (284 ° F; 413 K) |
| soluble | |
| Solubilité | soluble dans l' éthanol |
| Acidité (p K a ) | 1,94 |
|
Rotation chirale ([α] D )
|
+11,5 (H 2 O, c = 6,5) |
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Références Infobox | |
L'ornithine est un acide aminé non protéinogène qui joue un rôle dans le cycle de l' urée . L'ornithine s'accumule anormalement dans l'organisme en cas de déficit en ornithine transcarbamylase . Le radical est l' ornithyle .
Rôle dans le cycle de l'urée
La L -Ornithine est l'un des produits de l'action de l'enzyme arginase sur la L - arginine , créant de l' urée . Par conséquent, l'ornithine est une partie centrale du cycle de l'urée, ce qui permet l'élimination de l'excès d' azote . L'ornithine est recyclée et, d'une certaine manière, est un catalyseur. Premièrement, l'ammoniac est converti en phosphate de carbamoyle ( H
2 NC (O) OPO 2−
3 ). L'ornithine est convertie en un dérivé d'urée au niveau de l'azote δ (terminal) par la carbamoyl phosphate synthétase. Un autre azote est ajouté à partir de l' aspartate , produisant le fumarate dénitrogéné , et l' arginine résultante (un composé de guanidinium ) est réhydrolysée en ornithine, produisant de l'urée. Les azotes de l'urée proviennent de l'ammoniac et de l'aspartate, et l'azote de l'ornithine reste intact.
L'ornithine n'est pas un acide aminé codé par l' ADN , c'est-à-dire non protéinogène . Cependant, dans les tissus non hépatiques de mammifères, l'utilisation principale du cycle de l'urée est dans la biosynthèse de l'arginine, donc, en tant qu'intermédiaire dans les processus métaboliques, l'ornithine est assez importante.
Autres réactions
L'ornithine, via l'action de l' ornithine décarboxylase (EC 4.1.1.17), est le point de départ de la synthèse de polyamines comme la putrescine .
Dans les bactéries, telles que E. coli , l'ornithine peut être synthétisée à partir du L- glutamate .
Recherche
Fatigue de l'exercice
La supplémentation en L -Ornithine a atténué la fatigue chez les sujets dans une étude contrôlée par placebo utilisant un vélo ergomètre. Les résultats suggèrent que la L -ornithine a un effet antifatigue en augmentant l'efficacité de la consommation d'énergie et en favorisant l'excrétion de l'ammoniac.
Supplément d'haltérophilie
Les suppléments d' acides aminés , y compris la L -ornithine, sont fréquemment commercialisés auprès des culturistes et des haltérophiles avec des revendications pour des niveaux croissants d'hormone de croissance humaine (HGH), de masse musculaire et de force. Une courte étude clinique de 4 jours de 1993 a rapporté que la L -ornithine en association avec la L -arginine et la L -lysine à 2 g / j chacune n'augmentait pas la HGH. Une revue de 2002 sur le sujet a conclu: "L'utilisation d'acides aminés spécifiques pour stimuler la libération de GH par les athlètes n'est pas recommandée."
Cirrhose
L -Ornithine L -aspartate (LOLA), un sel stable d'ornithine et d'acide aspartique, a été utilisé dans le traitement de la cirrhose .

