Indicateur de pH - pH indicator
Un indicateur de pH est un composé chimique halochrome ajouté en petites quantités à une solution afin que le pH ( acidité ou basicité ) de la solution puisse être déterminé visuellement. Par conséquent, un indicateur de pH est un détecteur chimique d' ions hydronium (H 3 O + ) ou d'ions hydrogène (H + ) dans le modèle d'Arrhenius . Normalement, l'indicateur fait changer la couleur de la solution en fonction du pH. Les indicateurs peuvent également montrer un changement dans d'autres propriétés physiques ; par exemple, les indicateurs olfactifs montrent un changement dans leur odeur . Le pH d'une solution neutre est de 7,0 à 25°C ( conditions de laboratoire standard ). Les solutions dont le pH est inférieur à 7,0 sont considérées comme acides et les solutions dont le pH est supérieur à 7,0 sont basiques (alcalines). Comme la plupart des composés organiques naturels sont des protolytes faibles, des acides carboxyliques et des amines , les indicateurs de pH trouvent de nombreuses applications en biologie et en chimie analytique. De plus, les indicateurs de pH constituent l'un des trois principaux types de composés indicateurs utilisés en analyse chimique. Pour l'analyse quantitative des cations métalliques, l'utilisation d' indicateurs complexométriques est préférée, tandis que la troisième classe de composés, les indicateurs redox , sont utilisés dans les titrages impliquant une réaction redox comme base de l'analyse.
Théorie
En eux-mêmes, les indicateurs de pH sont souvent des acides faibles ou des bases faibles. Le schéma réactionnel général d'un indicateur de pH peut être formulé comme suit :
- DERRIÈRE + H
2O ⇌ H
3O+
+ Ind−
Ici, HInd représente la forme acide et Ind − la base conjuguée de l'indicateur. Le rapport de ceux-ci détermine la couleur de la solution et relie la couleur à la valeur du pH. Indicateurs de pH qui sont des protolytes faibles, l' équation de Henderson-Hasselbalch pour eux peut être écrite comme suit :
- pH = p K a + log 10
[ Ind−
] / [De derrière]
L'équation, dérivée de la constante d'acidité , indique que lorsque le pH est égal à la valeur p K a de l'indicateur, les deux espèces sont présentes dans un rapport 1:1. Si le pH est supérieur à la valeur p K a , la concentration de la base conjuguée est supérieure à la concentration de l'acide et la couleur associée à la base conjuguée domine. Si le pH est inférieur à la valeur p K a , l'inverse est vrai.
Habituellement, le changement de couleur n'est pas instantané à la valeur p K a , mais il existe une plage de pH où un mélange de couleurs est présent. Cette plage de pH varie selon les indicateurs, mais en règle générale, elle se situe entre la valeur p K a plus ou moins un. Cela suppose que les solutions conservent leur couleur tant qu'au moins 10 % des autres espèces persistent. Par exemple, si la concentration de la base conjuguée est 10 fois supérieure à la concentration de l'acide, leur rapport est de 10:1, et par conséquent le pH est p K a + 1. Inversement, si un excès de 10 fois de l'acide se produit par rapport à la base, le rapport est de 1:10 et le pH est p K a − 1.
Pour une précision optimale, la différence de couleur entre les deux espèces doit être aussi claire que possible, et plus la plage de pH du changement de couleur est étroite, mieux c'est. Dans certains indicateurs, comme la phénolphtaléine , l'une des espèces est incolore, alors que dans d'autres indicateurs, comme le rouge de méthyle , les deux espèces confèrent une couleur. Alors que les indicateurs de pH fonctionnent efficacement dans leur plage de pH désignée, ils sont généralement détruits aux extrémités de l'échelle de pH en raison de réactions secondaires indésirables.
Application
Les indicateurs de pH sont fréquemment utilisés dans les titrages en chimie analytique et en biologie pour déterminer l'étendue d'une réaction chimique . En raison du choix subjectif (détermination) de la couleur, les indicateurs de pH sont susceptibles de lectures imprécises. Pour les applications nécessitant une mesure précise du pH, un pH-mètre est fréquemment utilisé. Parfois, un mélange de différents indicateurs est utilisé pour obtenir plusieurs changements de couleur en douceur sur une large gamme de valeurs de pH. Ces indicateurs commerciaux (par exemple, l'indicateur universel et les papiers Hydrion ) sont utilisés lorsque seule une connaissance approximative du pH est nécessaire.
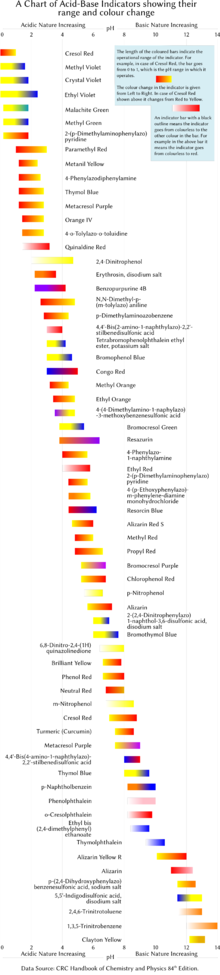
Le tableau ci-dessous présente plusieurs indicateurs de pH de laboratoire courants. Les indicateurs présentent généralement des couleurs intermédiaires à des valeurs de pH à l'intérieur de la plage de transition répertoriée. Par exemple, le rouge de phénol présente une couleur orange entre pH 6,8 et pH 8,4. La plage de transition peut légèrement se déplacer en fonction de la concentration de l'indicateur dans la solution et de la température à laquelle il est utilisé. La figure de droite montre les indicateurs avec leur plage de fonctionnement et leurs changements de couleur.
| Indicateur | Couleur à faible pH | Bas de gamme de transition |
Transition haut de gamme |
Couleur à pH élevé |
|---|---|---|---|---|
| Violet de gentiane ( Violet de méthyle 10B ) | jaune | 0.0 | 2.0 | bleu-violet |
| Vert malachite (première transition) | jaune | 0.0 | 2.0 | vert |
| Vert malachite (deuxième transition) | vert | 11.6 | 14,0 | incolore |
| Bleu de thymol (première transition) | rouge | 1.2 | 2.8 | jaune |
| Bleu de thymol (deuxième transition) | jaune | 8.0 | 9.6 | bleu |
| Jaune de méthyle | rouge | 2.9 | 4.0 | jaune |
| Bleu de bromophénol | jaune | 3.0 | 4.6 | bleu |
| Rouge Congo | bleu-violet | 3.0 | 5.0 | rouge |
| Orange de méthyle | rouge | 3.1 | 4.4 | jaune |
| Méthylorange tamisé (première transition) | rouge | 0.0 | 3.2 | gris-violet |
| Méthylorange tamisé (deuxième transition) | gris-violet | 3.2 | 4.2 | vert |
| Vert de bromocrésol | jaune | 3.8 | 5.4 | bleu |
| Rouge de méthyle | rouge | 4.4 | 6.2 | jaune |
| Pourpre de méthyle | violet | 4.8 | 5.4 | vert |
| Azolitmine (tournesol) | rouge | 4.5 | 8.3 | bleu |
| Violet de bromocrésol | jaune | 5.2 | 6.8 | violet |
| Bleu de bromothymol (première transition) | magenta | <0 | 6.0 | jaune |
| Bleu de bromothymol (deuxième transition) | jaune | 6.0 | 7.6 | bleu |
| Rouge de phénol | jaune | 6.4 | 8.0 | rouge |
| Rouge neutre | rouge | 6.8 | 8.0 | jaune |
| naphtolphtaléine | rouge pâle | 7.3 | 8.7 | bleu verdâtre |
| Rouge crésol | jaune | 7.2 | 8.8 | rouge-violet |
| Crésolphtaléine | incolore | 8.2 | 9.8 | violet |
| Phénophtaléine (première transition) | rouge-orange | <0 | 8.3 | incolore |
| Phénophtaléine (deuxième transition) | incolore | 8.3 | 10,0 | mauve rose |
| Phénophtaléine (troisième transition) | mauve rose | 12,0 | 13.0 | incolore |
| Thymophtaléine (première transition) | rouge | <0 | 9.3 | incolore |
| Thymophtaléine (deuxième transition) | incolore | 9.3 | 10.5 | bleu |
| Jaune alizarine R | jaune | 10.2 | 12,0 | rouge |
| Carmin indigo | bleu | 11.4 | 13.0 | jaune |
Indicateur universel
| Gamme de pH | La description | Couleur |
|---|---|---|
| 1-3 | Acide fort | rouge |
| 3 – 6 | Acide faible | Orange jaune |
| 7 | Neutre | Vert |
| 8 – 11 | Base faible | Bleu |
| 11-14 | Base solide | Violet/Indigo |
Mesure précise du pH
Un indicateur peut être utilisé pour obtenir des mesures assez précises du pH en mesurant quantitativement l'absorbance à deux ou plusieurs longueurs d'onde. Le principe peut être illustré en prenant comme indicateur un acide simple, HA, qui se dissocie en H + et A − .
- HA H + + A −
La valeur de la constante de dissociation acide , p K a , doit être connue. Les absorbances molaires , e HA et e A - des deux espèces de HA et A - aux longueurs d' onde λ x et λ y doit aussi avoir été déterminé par l' expérience précédente. En supposant que la loi de Beer soit respectée, les absorbances mesurées A x et A y aux deux longueurs d'onde sont simplement la somme des absorbances dues à chaque espèce.
Ce sont deux équations aux deux concentrations [HA] et [A − ]. Une fois résolu, le pH est obtenu comme
Si les mesures sont effectuées à plus de deux longueurs d'onde, les concentrations [HA] et [A − ] peuvent être calculées par les moindres carrés linéaires . En fait, tout un spectre peut être utilisé à cette fin. Le processus est illustré pour l'indicateur vert de bromocrésol . Le spectre observé (vert) est la somme des spectres de HA (or) et de A − (bleu), pondérés pour la concentration des deux espèces.
Lorsqu'un seul indicateur est utilisé, cette méthode est limitée aux mesures dans la plage de pH p K a ± 1, mais cette plage peut être étendue en utilisant des mélanges de deux ou plusieurs indicateurs. Étant donné que les indicateurs ont des spectres d'absorption intenses, la concentration de l'indicateur est relativement faible et l'indicateur lui-même est supposé avoir un effet négligeable sur le pH.
Point d'équivalence
Dans les titrages acido-basiques, un indicateur de pH inapproprié peut induire un changement de couleur dans la solution contenant l'indicateur avant ou après le point d'équivalence réel. En conséquence, différents points d'équivalence pour une solution peuvent être conclus en fonction de l'indicateur de pH utilisé. En effet, le moindre changement de couleur de la solution contenant l'indicateur suggère que le point d'équivalence a été atteint. Par conséquent, l'indicateur de pH le plus approprié a une plage de pH efficace, où le changement de couleur est apparent, qui englobe le pH du point d'équivalence de la solution titrée.
Indicateurs de pH naturels
De nombreuses plantes ou parties de plantes contiennent des produits chimiques de la famille des composés anthocyanes naturellement colorés . Ils sont rouges dans les solutions acides et bleus dans les solutions basiques. Les anthocyanes peuvent être extraites avec de l'eau ou d'autres solvants d'une multitude de plantes colorées qui sont des parties de plantes, notamment à partir de feuilles ( chou rouge ) ; fleurs ( géranium , coquelicot ou pétales de rose ); baies ( myrtilles , cassis ) ; et tiges ( rhubarbe ). L'extraction d'anthocyanes à partir de plantes domestiques, en particulier de chou rouge , pour former un indicateur de pH brut est une démonstration populaire d'introduction à la chimie.
Le tournesol , utilisé par les alchimistes au Moyen Âge et encore facilement disponible, est un indicateur de pH naturel fabriqué à partir d'un mélange d' espèces de lichens , en particulier Roccella tinctoria . Le mot tournesol vient littéralement de « mousse colorée » en vieux norrois (voir Litr ). La couleur change entre le rouge dans les solutions acides et le bleu dans les alcalis. Le terme « test décisif » est devenu une métaphore largement utilisée pour tout test qui prétend distinguer avec autorité entre les alternatives.
Les fleurs d' Hydrangea macrophylla peuvent changer de couleur en fonction de l'acidité du sol. Dans les sols acides, des réactions chimiques se produisent dans le sol qui rendent l' aluminium disponible pour ces plantes,rendantles fleurs bleues. Dans les sols alcalins, ces réactions ne peuvent pas se produire et donc l'aluminium n'est pas absorbé par la plante. En conséquence, les fleurs restent roses.
Un autre indicateur de pH naturel utile est l'épice Curcuma . Il est jaune lorsqu'il est exposé aux acides et brun rougeâtre lorsqu'il est en présence d'un alcali .
| Indicateur | Couleur à faible pH | Couleur à pH élevé |
|---|---|---|
| Fleurs d' hortensia | bleu | rose à violet |
| Anthocyanes | rouge | bleu |
| Tournesol | rouge | bleu |
| Curcuma | jaune | brun rougeâtre |
Chou-fleur violet trempé dans du bicarbonate de soude (à gauche) et du vinaigre (à droite). L'anthocyane agit comme un indicateur de pH.
Voir également
Les références
- Longue liste d'indicateurs
- "Liste d'indicateurs complet" (PDF) (en français). (57,3 Kio )




![{\displaystyle {\begin{aligned}A_{x}&=[{\ce {HA}}]\varepsilon _{{\ce {HA}}}^{x}+[{\ce {A-}} ]\varepsilon _{{\ce {A-}}}^{x}\\A_{y}&=[{\ce {HA}}]\varepsilon _{{\ce {HA}}}^{y }+[{\ce {A-}}]\varepsilon _{{\ce {A-}}}^{y}\end{aligned}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/407bba3b954782cbec25c32d99393bf282c2c36d)
![{\displaystyle \mathrm {pH} =\mathrm {p} K_{\mathrm {a} }+\log {\frac {[{\ce {A-}}]}{[{\ce {HA}}] }}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/2ed476e8f78a1980748a81ec195978b60032411f)




