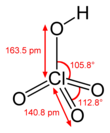
Acide perchlorique - Perchloric acid
|
|
|||

|
|||
| Noms | |||
|---|---|---|---|
|
Nom IUPAC systématique
acide chlorique(VII) |
|||
| Autres noms
Acide hyperchlorique
|
|||
| Identifiants | |||
|
Modèle 3D ( JSmol )
|
|||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| Carte d'information de l'ECHA |
100.028.648 |
||
| Numéro CE | |||
|
CID PubChem
|
|||
| Numéro RTECS | |||
| UNII | |||
| Numéro ONU | 1873 | ||
|
Tableau de bord CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriétés | |||
| HClO 4 | |||
| Masse molaire | 100,46 g/mol | ||
| Apparence | liquide incolore | ||
| Odeur | inodore | ||
| Densité | 1,768 g / cm 3 | ||
| Point de fusion | −17 °C (1 °F; 256 K) ( azéotrope ) −112 °C ( anhydre ) |
||
| Point d'ébullition | 203 °C (397 °F; 476 K) ( azéotrope ) | ||
| miscible | |||
| Acidité (p K a ) | -15,2 (±2,0); −10 | ||
| Base conjuguée | Perchlorate | ||
| Dangers | |||
| Fiche de données de sécurité | ICSC 1006 | ||
| Pictogrammes SGH |
   
|
||
| Mention d'avertissement SGH | Danger | ||
| H271 , H290 , H302 , H314 , H373 | |||
| P210 , P280 , P303+361+353 , P304+340 , P310 , P305+351+338 , P371 , P380 , P375 | |||
| NFPA 704 (diamant de feu) | |||
| point de rupture | Ininflammable | ||
| Composés apparentés | |||
|
Composés apparentés
|
Acide chlorhydrique Acide hypochloreux Acide chloreux Acide chlorique |
||
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 °C [77 °F], 100 kPa). |
|||
|
|
|||
| Références de l'infobox | |||
L'acide perchlorique est un acide minéral de formule H Cl O 4 . Habituellement trouvé sous forme de solution aqueuse, ce composé incolore est un acide plus fort que l'acide sulfurique , l'acide nitrique et l'acide chlorhydrique . C'est un oxydant puissant lorsqu'il est chaud, mais les solutions aqueuses jusqu'à environ 70 % en poids à température ambiante sont généralement sans danger, ne présentant que des caractéristiques acides fortes et aucune propriété oxydante. L'acide perchlorique est utile pour préparer des sels de perchlorate , en particulier le perchlorate d'ammonium , un composant important du carburant de fusée . L'acide perchlorique est dangereusement corrosif et forme facilement des mélanges potentiellement explosifs.
Production
L'acide perchlorique est produit industriellement par deux voies. La méthode traditionnelle exploite la haute solubilité aqueuse du perchlorate de sodium (209 g/100 mL d'eau à température ambiante). Le traitement de telles solutions avec de l'acide chlorhydrique donne de l'acide perchlorique, précipitant du chlorure de sodium solide :
- NaClO 4 + HCl → NaCl + HClO 4
L'acide concentré peut être purifié par distillation . La voie alternative, plus directe et évitant les sels, consiste en une oxydation anodique du chlore aqueux au niveau d'une électrode de platine.
Préparations de laboratoire
Le traitement du perchlorate de baryum avec de l'acide sulfurique précipite le sulfate de baryum , laissant l'acide perchlorique. Il peut également être fabriqué en mélangeant de l'acide nitrique avec du perchlorate d'ammonium et en le faisant bouillir tout en ajoutant de l'acide chlorhydrique. La réaction donne l' oxyde nitreux et l' acide perchlorique en raison d'une réaction simultanée impliquant l' ammonium ion et peut être concentré et purifié de manière significative par l' ébullition de l'acide nitrique et l' acide chlorhydrique restant
Propriétés
L'acide perchlorique anhydre est un liquide huileux instable à température ambiante. Il forme au moins cinq hydrates dont plusieurs ont été caractérisés cristallographiquement . Ces solides sont constitués de l' anion perchlorate lié par des liaisons hydrogène aux centres H 2 O et H 3 O + L'acide perchlorique forme un azéotrope avec l'eau, constitué d'environ 72,5 % d'acide perchlorique. Cette forme de l'acide est stable indéfiniment et est disponible dans le commerce. De telles solutions sont hygroscopiques . Ainsi, s'il est laissé à l'air libre, l'acide perchlorique concentré se dilue en absorbant l'eau de l'air.
La déshydratation de l'acide perchlorique donne l'anhydride dichloré heptoxyde :
- 2 HClO 4 + P 4 O 10 → Cl 2 O 7 + H 2 P 4 O 11
Les usages
L'acide perchlorique est principalement produit comme précurseur du perchlorate d'ammonium , qui est utilisé dans le carburant des fusées. La croissance des fusées a conduit à une augmentation de la production d'acide perchlorique. Plusieurs millions de kilogrammes sont produits chaque année. L'acide perchlorique est l'un des matériaux les plus éprouvés pour la gravure d' écrans à cristaux liquides et les applications électroniques critiques ainsi que pour l'extraction de minerai et possède des propriétés uniques en chimie analytique. De plus, c'est un composant utile dans la gravure du chrome
En tant qu'acide
L'acide perchlorique, un superacide , est l'un des acides de Brønsted-Lowry les plus puissants . Que son p K a soit inférieur à -9 est mis en évidence par le fait que son monohydrate contient des ions hydronium discrets et peut être isolé sous la forme d'un solide cristallin stable, formulé sous la forme [H 3 O + ][ ClO–
4]. La plus récente estimation de sa solution aqueuse p K a est−15,2 ± 2,0 . Il fournit une forte acidité avec un minimum d'interférences car le perchlorate est faiblement nucléophile (expliquant la forte acidité de HClO 4 ). D'autres acides d' anions non coordinants , tels que l'acide fluoroborique et l'acide hexafluorophosphorique, sont sensibles à l'hydrolyse, contrairement à l'acide perchlorique. Malgré les dangers liés à l'explosivité de ses sels, l'acide est souvent préféré dans certaines synthèses. Pour des raisons similaires, c'est un éluant utile en chromatographie échangeuse d'ions.
Il est également utilisé pour le polissage électrolytique ou la gravure de l'aluminium, du molybdène et d'autres métaux.
Sécurité
Compte tenu de ses fortes propriétés oxydantes , l'acide perchlorique est soumis à une réglementation importante. Il est très réactif avec les métaux (par exemple, l' aluminium ) et les matières organiques (bois, plastiques). Les travaux effectués avec de l'acide perchlorique doivent être effectués dans des hottes avec une capacité de lavage pour éviter l'accumulation d'oxydants dans les conduits.
Le 20 février 1947, à Los Angeles, en Californie , 17 personnes ont été tuées et 150 blessées lorsqu'un bain, composé de plus de 1 000 litres d'acide perchlorique à 75 % et à 25 % d'anhydride acétique en volume, a explosé. L'usine d'électrodéposition d'O'Connor, 25 autres bâtiments et 40 automobiles ont été détruits et 250 maisons voisines ont été endommagées. Le bain servait à polir électrolytiquement les meubles en aluminium. De plus, des composés organiques ont été ajoutés au bain de surchauffe lorsqu'une grille en fer a été remplacée par une autre enduite d' acétobutyrate de cellulose ( plastique Tenit-2 ). Quelques minutes plus tard, le bain a explosé.