1-Propanol - 1-Propanol

|
|

|
|
| Noms | |
|---|---|
|
Nom IUPAC préféré
Propane-1-ol |
|
| Autres noms | |
| Identifiants | |
|
Modèle 3D ( JSmol )
|
|
| 3DMet | |
| 1098242 | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| Banque de médicaments | |
| Carte d'information de l'ECHA |
100.000.679 |
| Numéro CE | |
| 25616 | |
| KEGG | |
| Engrener | 1-Propanol |
|
CID PubChem
|
|
| Numéro RTECS | |
| UNII | |
| Numéro ONU | 1274 |
|
Tableau de bord CompTox ( EPA )
|
|
|
|
|
|
| Propriétés | |
| C 3 H 8 O | |
| Masse molaire | 60,096 g·mol -1 |
| Apparence | Liquide incolore |
| Odeur | doux, semblable à l'alcool |
| Densité | 0,803 g/mL |
| Point de fusion | -126 °C ; −195 °F; 147 K |
| Point d'ébullition | 97 à 98 °C ; 206 à 208 °F; 370 à 371 K |
| miscible | |
| log P | 0,329 |
| La pression de vapeur | 1,99 kPa (à 20 °C) |
| Acidité (p K a ) | 16 |
| Basicité (p K b ) | -2 |
| −45,176·10 −6 cm 3 /mol | |
|
Indice de réfraction ( n D )
|
1,387 |
| Viscosité | 1,959 mPa·s (à 25 °C) |
| 1,68 D | |
| Thermochimie | |
|
Capacité calorifique ( C )
|
143,96 J/(K·mol) |
|
Entropie molaire standard ( S |
192,8 J/(K·mol) |
|
Std enthalpie de
formation (Δ f H ⦵ 298 ) |
−302,79…−302,29 kJ/mol |
|
Std enthalpie de
combustion (Δ c H ⦵ 298 ) |
−2.02156…−2.02106 MJ/mol |
| Pharmacologie | |
| D08AX03 ( OMS ) | |
| Dangers | |
| Pictogrammes SGH |
  
|
| Mention d'avertissement SGH | Danger |
| H225 , H318 , H336 | |
| P210 , P261 , P280 , P305+351+338 | |
| NFPA 704 (diamant de feu) | |
| point de rupture | 22 °C (72 °F; 295 K) |
| 371 °C (700 °F; 644 K) | |
| Limites d'explosivité | 2,2–13,7% |
| Dose ou concentration létale (LD, LC) : | |
|
DL 50 ( dose médiane )
|
2800 mg/kg (lapin, oral) 6800 mg/kg (souris, oral) 1870 mg/kg (rat, oral) |
| NIOSH (limites d'exposition pour la santé aux États-Unis) : | |
|
PEL (Autorisé)
|
TWA 200 ppm (500 mg/m 3 ) |
|
REL (recommandé)
|
TWA 200 ppm (500 mg/m 3 ) ST 250 ppm (625 mg/m 3 ) [peau] |
|
IDLH (Danger immédiat)
|
800 ppm |
| Composés apparentés | |
|
Composés apparentés
|
Propane Alcool isopropylique Propanamine Éthanol Butanol |
| Page de données supplémentaires | |
|
Indice de réfraction ( n ), Constante diélectrique (ε r ), etc. |
|
|
Données thermodynamiques |
Comportement des phases solide-liquide-gaz |
| UV , IR , RMN , MS | |
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Références de l'infobox | |
Le 1-Propanol est un alcool primaire de formule CH
3CH
2CH
2OH et parfois représenté par PrOH ou n- PrOH . C'est un liquide incolore et un isomère du 2-propanol . Il se forme naturellement en petites quantités au cours de nombreux processus de fermentation et est utilisé comme solvant dans l'industrie pharmaceutique, principalement pour les résines et les esters de cellulose, et, parfois, comme agent désinfectant .
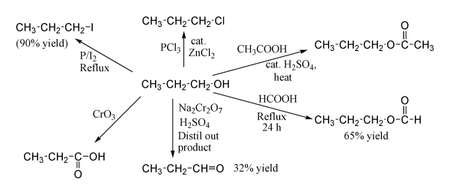
Propriétés chimiques
Le 1-Propanol montre les réactions normales d'un alcool primaire . Ainsi, il peut être converti en halogénures d'alkyle ; par exemple, le phosphore rouge et l' iode produisent de l'iodure de n-propyle avec un rendement de 80 %, tandis que le PCl
3avec ZnCl catalytique
2donne du chlorure de n-propyle . Réaction avec l'acide acétique en présence d'un H
2DONC
4le catalyseur dans des conditions d' estérification de Fischer donne de l'acétate de propyle , tandis que le reflux du propanol pendant une nuit avec de l'acide formique seul peut produire du formiate de propyle avec un rendement de 65 %. Oxydation du 1-propanol avec Na
2Cr
2O
7et H
2DONC
4ne donne qu'un rendement de 36% en propionaldéhyde , et par conséquent, pour ce type de réaction, des méthodes à rendement plus élevé utilisant le PCC ou l'oxydation de Swern sont recommandées. L'oxydation avec l'acide chromique donne l'acide propionique .
Préparation
Le 1-propanol est fabriqué par hydrogénation catalytique du propionaldéhyde . Le propionaldéhyde est produit via le procédé oxo par hydroformylation d' éthylène en utilisant du monoxyde de carbone et de l' hydrogène en présence d'un catalyseur tel que l'octacarbonyle de cobalt ou un complexe de rhodium .
- H
2C=CH
2 + CO + H
2 → CH
3CH
2CH=O
- CH
3CH
2CH=O + H
2 → CH
3CH
2CH
2OH
Une préparation traditionnelle en laboratoire du 1-propanol consiste à traiter l' iodure de n- propyle avec de l' Ag humide
2O .
Sécurité
On pense que le 1-propanol est similaire à l' éthanol dans ses effets sur le corps humain, mais 2 à 4 fois plus puissant. La DL 50 orale chez le rat est de 1870 mg/kg (contre 7060 mg/kg pour l'éthanol). Il est métabolisé en acide propionique . Les effets comprennent une intoxication alcoolique et une acidose métabolique à trou anionique élevé . En 2011, un seul cas d'empoisonnement mortel au 1-propanol a été signalé.
Le propanol comme carburant
Le 1-propanol a un indice d'octane élevé et convient à la consommation de carburant du moteur . Cependant, le propanol est trop coûteux à utiliser comme carburant. L' indice d'octane de recherche (RON) du propanol est de 118 et l'indice antidétonant (AKI) est de 108.
Les références
Lectures complémentaires
- Furniss, BS ; Hannaford, AJ; Smith, PWG ; Tatchell, AR (1989), Vogel's Textbook of Practical Organic Chemistry (5e éd.), Harlow: Longman, ISBN 0-582-46236-3
- Lide DR, éd. (2006). CRC Handbook of Chemistry and Physics (87e éd.). TF-CRC. ISBN 0849304873.
- O'Neil MJ, éd. (2006). L'index de Merck : Une encyclopédie des produits chimiques, des médicaments et des produits biologiques (14e éd.). Merck. ISBN 091191000X.
- Perkin WH, Kipping FS (1922). Chimie Organique . Londres : W. & R. Chambers. ISBN 0080223540.