Oxyde de propylène - Propylene oxide
|
|

|
|
| Des noms | |
|---|---|
|
Nom IUPAC préféré
(2R)-2-Méthyloxirane (2S)-2-Méthyloxirane |
|
| Autres noms
Oxyde de propylène
Epoxypropane Epoxyde de propylène Oxyde de 1,2-propylène Oxyrane de méthyle 1,2-Epoxypropane Oxyde de propène Oxyde de méthyléthylène Oxyde de méthyléthylène |
|
| Identifiants | |
|
Modèle 3D ( JSmol )
|
|
| ChEBI | |
| ChemSpider | |
| Carte d'information de l'ECHA |
100.000.800 |
| Numéro CE | |
| KEGG | |
|
CID PubChem
|
|
| UNII | |
|
Tableau de bord CompTox ( EPA )
|
|
|
|
|
|
| Propriétés | |
| C 3 H 6 O | |
| Masse molaire | 58,080 g·mol -1 |
| Apparence | Liquide incolore |
| Odeur | semblable au benzène |
| Densité | 0,859 g / cm 3 |
| Point de fusion | −111,9 °C (−169,4 °F; 161,2 K) |
| Point d'ébullition | 35 °C (95 °F; 308 K) |
| 41 % (20 °C) | |
| La pression de vapeur | 445 mmHg (20 °C) |
| −4,25 × 10 −5 cm 3 /mol | |
|
Indice de réfraction ( n D )
|
1.3660 |
| Thermochimie | |
|
Capacité calorifique ( C )
|
120,4 J·(K·mol) -1 |
|
Entropie molaire standard ( S |
196,5 J·(K·mol) -1 |
|
Std enthalpie de
formation (Δ f H ⦵ 298 ) |
−123,0 kJ·mol −1 |
| Dangers | |
| Principaux dangers | Extrêmement inflammable |
| Pictogrammes SGH |
  
|
| Mention d'avertissement SGH | Danger |
| NFPA 704 (diamant de feu) | |
| point de rupture | −37 °C (−35 °F; 236 K) |
| 747 °C (1 377 °F; 1 020 K) | |
| Limites d'explosivité | 2,3-36% |
| Dose ou concentration létale (LD, LC) : | |
|
DL 50 ( dose médiane )
|
660 mg/kg (cobaye, oral) 380 mg/kg (rat, oral) 440 mg/kg (souris, oral) 1140 mg/kg (rat, oral) 690 mg/kg (cobaye, oral) |
|
CL 50 ( concentration médiane )
|
1740 ppm (souris, 4 h) 4000 ppm (rat, 4 h) |
|
LC Lo (le plus bas publié )
|
2005 ppm (chien, 4 h) 4000 ppm (cochon d'Inde, 4 h) |
| NIOSH (limites d'exposition pour la santé aux États-Unis) : | |
|
PEL (Autorisé)
|
TWA 100 ppm (240 mg/m 3 ) |
|
REL (recommandé)
|
Californie |
|
IDLH (Danger immédiat)
|
Ca [400 ppm] |
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Références de l'infobox | |
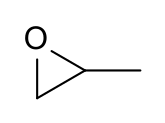
L'oxyde de propylène est un composé organique de formule moléculaire CH 3 CHCH 2 O. Ce liquide volatil incolore à l'odeur proche de l'éther est produit à grande échelle industriellement. Son application principale est son utilisation pour la production de polyéther polyols destinés à être utilisés dans la fabrication de plastiques polyuréthanes . C'est un époxyde chiral , bien qu'il soit couramment utilisé comme mélange racémique .
Ce composé est parfois appelé oxyde de 1,2-propylène pour le distinguer de son isomère oxyde de 1,3-propylène, mieux connu sous le nom d' oxétane .
Production
La production industrielle d'oxyde de propylène commence à partir du propylène . Deux approches générales sont utilisées, l'une impliquant l'hydrochloration et l'autre impliquant l'oxydation. En 2005, environ la moitié de la production mondiale était assurée par la technologie de la chlorhydrine et l'autre moitié par des voies d'oxydation. Cette dernière approche prend de plus en plus d'importance.
Voie d'hydrochloration
La voie traditionnelle passe par la conversion du propène en propylène chlorhydrine selon le schéma simplifié suivant :
Le mélange de 1-chloro-2-propanol et de 2-chloro-1-propanol est ensuite déshydrochloré. Par example:
La chaux ( hydroxyde de calcium ) est souvent utilisée pour absorber le HCl .
Oxydation du propylène
L'autre voie générale vers l'oxyde de propylène implique l'oxydation du propylène avec un peroxyde organique. La réaction suit cette stoechiométrie :
- CH 3 CH=CH 2 + RO 2 H → CH 3 CHCH 2 O + ROH
Le procédé est pratiqué avec quatre hydroperoxydes :
- Dans le processus de Halcon , t - butyl hydroperoxyde dérivé d'oxygénation de l' isobutane , ce qui donne t - butanol . Ce coproduit peut être déshydraté en isobutène, transformé en MTBE , un additif pour l' essence .
- Hydroperoxyde d'éthylbenzène, issu de l'oxygénation de l' éthylbenzène , qui donne le 1-phényléthanol. Ce coproduit peut être déshydraté pour donner du styrène , un monomère utile.
- Hydroperoxyde de cumène issu de l'oxygénation du cumène (isopropylbenzène), qui donne l'alcool cumylique. Par déshydratation et hydrogénation, ce coproduit peut être recyclé en cumène. Cette technologie a été commercialisée par Sumitomo Chemical.
- Le peroxyde d'hydrogène est l'oxydant dans le procédé du peroxyde d'hydrogène en oxyde de propylène (HPPO), catalysé par une silicalite dopée au titane :
- C 3 H 6 + H 2 O 2 → C 3 H 6 O + H 2 O
En principe, ce processus ne produit que de l'eau était un produit secondaire. En pratique, certains dérivés à cycle ouvert de PO sont générés.
Réactions
Comme les autres époxydes, le PO subit des réactions d'ouverture de cycle. Avec de l'eau, du propylène glycol est produit. Avec les alcools, des réactions, appelées hydroxypropylation , analogues à l' éthoxylation se produisent. Les réactifs de Grignard s'ajoutent à l'oxyde de propylène pour donner des alcools secondaires.
Certaines autres réactions de l'oxyde de propylène comprennent :
- La réaction avec l'oxyde d'aluminium à 250-260 °C conduit au propionaldéhyde et à un peu d' acétone .
- La réaction avec l' oxyde d' argent (I) conduit à l'acide acétique .
- La réaction avec l'amalgame sodium-mercure et l'eau conduit à l' isopropanol .
Les usages
Entre 60 et 70 % de tout l'oxyde de propylène est converti en polyéther polyols par le processus appelé alcoxylation . Ces polyols sont des éléments constitutifs de la production de plastiques polyuréthanes . Environ 20% de l'oxyde de propylène est hydrolysé en propylène glycol , via un procédé qui est accéléré par catalyse acide ou basique . Les autres principaux produits sont le polypropylène glycol , les éthers de propylène glycol et le carbonate de propylène .
Utilisations de niche
Fumigant
La Food and Drug Administration des États-Unis a approuvé l'utilisation d'oxyde de propylène pour pasteuriser les amandes crues à compter du 1er septembre 2007, en réponse à deux incidents de contamination par Salmonella dans des vergers commerciaux, un incident survenu au Canada et un aux États-Unis. Les pistaches peuvent également être soumises à de l'oxyde de propylène pour contrôler les salmonelles .
Microscopie
L'oxyde de propylène est couramment utilisé dans la préparation d'échantillons biologiques pour la microscopie électronique , pour éliminer l' éthanol résiduel précédemment utilisé pour la déshydratation. Dans une procédure typique, l'échantillon est d'abord immergé dans un mélange de volumes égaux d'éthanol et d'oxyde de propylène pendant 5 minutes, puis quatre fois dans de l'oxyde pur, 10 minutes chacune.
Sécurité
C'est un cancérogène potentiel pour l'homme, et est inclus dans la liste des cancérogènes du groupe 2B du CIRC .
Occurrence naturelle
En 2016, il a été signalé que de l'oxyde de propylène avait été détecté dans Sagittarius B2 , un nuage de gaz dans la Voie lactée pesant trois millions de masses solaires . C'est la première molécule chirale à être détectée dans l'espace, mais sans excès énantiomérique.
Les références
Sources citées
- Haynes, William M., éd. (2011). CRC Handbook of Chemistry and Physics (92e éd.). Boca Raton, Floride : CRC Press . ISBN 1439855110.
Liens externes
- Page WebBook pour C3H6O
- Oxyde de propylène à l' Agence de protection de l'environnement des États-Unis
- Oxyde de propylène – informations sur les produits chimiques : propriétés, production, applications.
- Oxyde de propylène sur le site Web du Réseau de transfert de technologie sur les substances toxiques de l'air
- CDC - NIOSH Pocket Guide to Chemical Hazards

