Peroxyde de sodium - Sodium peroxide

|
|
|
|

|
|
| Noms | |
|---|---|
| Autres noms
Dioxyde disodique
Flocool Solozone Peroxyde disodique |
|
| Identifiants | |
|
Modèle 3D ( JSmol )
|
|
| ChemSpider | |
| Carte d'information de l'ECHA |
100.013.828 |
| Numéro CE | |
|
CID PubChem
|
|
| Numéro RTECS | |
| UNII | |
| Numéro ONU | 1504 |
|
Tableau de bord CompTox ( EPA )
|
|
|
|
|
|
| Propriétés | |
| Na 2 O 2 | |
| Masse molaire | 77,98 g/mol |
| Apparence | poudre jaune à blanche |
| Densité | 2,805 g / cm 3 |
| Point de fusion | 460 °C (860 °F; 733 K) (se décompose) |
| Point d'ébullition | 657 °C (1 215 °F; 930 K) (se décompose) |
| réagit violemment | |
| Solubilité | soluble dans l'acide insoluble dans la base réagit avec l' éthanol |
| −28.10·10 −6 cm 3 /mol | |
| Structure | |
| hexagonal | |
| Thermochimie | |
|
Capacité calorifique ( C )
|
89,37 J/(mol·K) |
|
Entropie molaire standard ( S |
95 J/(mol·K) |
|
Std enthalpie de
formation (Δ f H ⦵ 298 ) |
−515 kJ·mol −1 |
|
Énergie libre de Gibbs (Δ f G ˚)
|
-446,9 kJ/mol |
| Dangers | |
| Fiche de données de sécurité | FDS externe |
|
Classification UE (DSD) (obsolète)
|
|
| Phrases R (obsolètes) | R8 , R35 |
| Phrases S (obsolètes) | (S1/2) , S8 , S27 , S39 , S45 |
| NFPA 704 (diamant de feu) | |
| point de rupture | Ininflammable |
| Composés apparentés | |
|
Autres cations
|
Peroxyde de lithium Peroxyde de potassium Peroxyde de rubidium Peroxyde de césium |
|
Oxyde de sodium Superoxyde de sodium |
|
|
Composés apparentés
|
Hydroxyde de sodium Peroxyde d'hydrogène |
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Références de l'infobox | |
Le peroxyde de sodium est le composé inorganique de formule Na 2 O 2 . Ce solide jaunâtre est le produit du sodium enflammé dans un excès d'oxygène. C'est une base solide. Ce peroxyde métallique existe dans plusieurs hydrates et peroxyhydrates dont Na 2 O 2 ·2H 2 O 2 ·4H 2 O, Na 2 O 2 ·2H 2 O, Na 2 O 2 ·2H 2 O 2 et Na 2 O 2 ·8H 2 O. L'octahydrate, simple à préparer, est blanc, contrairement à la matière anhydre.
Propriétés
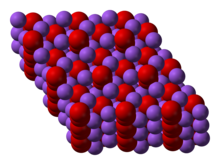
Le peroxyde de sodium cristallise avec une symétrie hexagonale. Lors du chauffage, la forme hexagonale subit une transition vers une phase de symétrie inconnue à 512 °C. Avec un chauffage supplémentaire au-dessus du point d'ébullition de 657 °C, le composé se décompose en Na 2 O, libérant O 2 .
- 2 Na 2 O 2 → 2 Na 2 O + O 2
Préparation
L'octahydrate est produit en traitant l'hydroxyde de sodium avec du peroxyde d'hydrogène.
Le peroxyde de sodium peut être préparé à grande échelle par la réaction du sodium métallique avec l'oxygène à 130-200 ° C, un processus qui génère de l'oxyde de sodium , qui dans une étape séparée absorbe l'oxygène :
- 4 Na + O 2 → 2 Na 2 O
- 2 Na 2 O + O 2 → 2 Na 2 O 2
Il peut également être produit en faisant passer de l'ozone gazeux sur de l'iodure de sodium solide à l' intérieur d'un tube en platine ou en palladium . L'ozone oxyde le sodium pour former du peroxyde de sodium. L' iode peut être sublimé par un léger chauffage. Le platine ou le palladium catalyse la réaction et n'est pas attaqué par le peroxyde de sodium.
Les usages
Le peroxyde de sodium s'hydrolyse pour donner de l'hydroxyde de sodium et du peroxyde d'hydrogène selon la réaction
- Na 2 O 2 + 2 H 2 O → 2 NaOH + H 2 O 2
Le peroxyde de sodium était utilisé pour blanchir la pâte de bois pour la production de papier et de textiles. Actuellement, il est principalement utilisé pour des opérations de laboratoire spécialisées, par exemple, l'extraction de minéraux à partir de divers minerais. Le peroxyde de sodium peut porter les noms commerciaux de Solozone et Flocool . Dans les préparations chimiques, le peroxyde de sodium est utilisé comme agent oxydant. Il est également utilisé comme source d'oxygène en le faisant réagir avec du dioxyde de carbone pour produire de l'oxygène et du carbonate de sodium :
- 2 Na 2 O 2 + 2 CO 2 → 2 Na 2 CO 3 + O 2
Il est donc particulièrement utile dans les équipements de plongée, les sous-marins, etc. Le peroxyde de lithium et le superoxyde de potassium ont des utilisations similaires.

