Spinodal - Spinodal
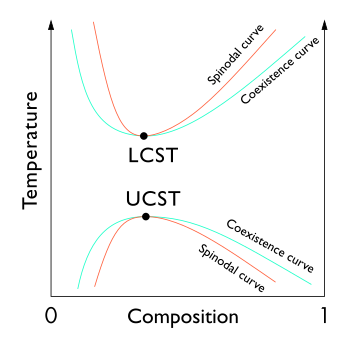
En thermodynamique , la limite de stabilité locale par rapport aux petites fluctuations est clairement définie par la condition que la dérivée seconde de l'énergie libre de Gibbs est nulle. Le lieu de ces points (le point d'inflexion dans une courbe Gx ou Gc, énergie libre de Gibbs en fonction de la composition) est connu sous le nom de courbe spinodale . Pour les compositions au sein de cette courbe, des fluctuations infiniment petites de composition et de densité conduiront à une séparation de phase via la décomposition spinodale . En dehors de la courbe, la solution sera au moins métastable vis-à-vis des fluctuations. En d'autres termes, en dehors de la courbe spinodale, un processus minutieux peut obtenir un système monophasé. À l'intérieur, seuls des procédés éloignés de l'équilibre thermodynamique, comme le dépôt physique en phase vapeur, permettront de préparer des compositions monophasées. Les points locaux des compositions coexistantes, définis par la construction tangente commune, sont connus sous le nom de courbe binodale (coexistence), qui désigne l'état d'équilibre d'énergie minimale du système. L'augmentation de la température entraîne une différence décroissante entre l'entropie de mélange et l'enthalpie de mélange, et ainsi les compositions coexistantes se rapprochent. La courbe binodale constitue la base de l' écart de miscibilité dans un diagramme de phase. L'énergie libre du mélange change avec la température et la concentration, et le binodal et le spinodal se rencontrent à la température et à la composition critiques ou consolidées .
Critère
Pour les solutions binaires, le critère thermodynamique qui définit la courbe spinodale est que la deuxième dérivée de l'énergie libre par rapport à la densité ou à une variable de composition est nulle.
Point critique
Les extrema du spinodal dans un graphique température / composition coïncident avec ceux de la courbe binodale et sont appelés points critiques .
Equilibres liquide-liquide isotherme
Dans le cas des équilibres liquide-liquide isothermes ternaires, la courbe spinodale (obtenue à partir de la matrice de Hesse) et le point critique correspondant peuvent être utilisés pour aider le processus de corrélation des données expérimentales.
Les références
- ^ G. Astarita: Thermodynamique: Un manuel avancé pour les ingénieurs chimistes (Springer 1990), chapitres 4, 8, 9, 12.
- ^ Sandler SI, Thermodynamique chimique et technique . 1999 John Wiley & Sons, Inc., p 571.
- ^ A b c d Koningsveld K., Stockmayer WH, Nies, E., Polymer Phase Diagrams: A Textbook . 2001 Oxford, p 12.
- ^ PH Mayrhofer et al. Progrès de la science des matériaux 51 (2006) 1032-1114 doi : 10.1016 / j.pmatsci.2006.02.002
- ^ Cahn RW, Haasen P. Métallurgie physique. 4e éd. Cambridge: Univ Press; 1996
- ^ Sandler SI, Thermodynamique chimique et technique . 1999 John Wiley & Sons, Inc., p 557.
- ^ un b Koningsveld K., Stockmayer WH, Nies, E., Diagrammes de phase de polymère: Un manuel . 2001 Oxford, pages 46-47.
- ^ Marcilla, A .; Serrano, MD; Reyes-Labarta, JA; Olaya, MM (2012). "Vérification des conditions de point critique liquide-liquide et leur application dans les systèmes ternaires". Recherche en chimie industrielle et technique . 51 (13): 5098-5102. doi : 10.1021 / ie202793r .
- ^ Marcilla, A .; Reyes-Labarta, JA; Serrano, MD; Olaya, MM (2011). "Modèles GE et algorithmes pour la régression de données en équilibre de phase condensée dans les systèmes ternaires: limitations et propositions" . Le journal ouvert de la thermodynamique . 5 : 48–62. doi : 10.2174 / 1874396X01105010048 .
-
^ Interface utilisateur graphique, (GUI) (2015-11-27). "Analyse topologique de la fonction d'énergie de Gibbs (données de corrélation d'équilibre liquide-liquide. Y compris une revue thermodinamique et des lignes de liaison / analyse de matrice de Hesse)". Université d'Alicante (Reyes-Labarta et al.2015-18). hdl : 10045/51725 . Citer le journal nécessite
|journal=( aide )
