Streptococcus mutans -Streptococcus mutans
| Streptocoque mutant | |
|---|---|
|
|
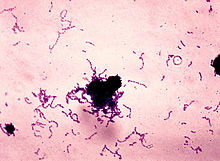
| Coloration de S. mutans dans un bouillon de culture au thioglycolate . | |
|
Classement scientifique |
|
| Domaine: | Bactéries |
| Phylum: | Firmicutes |
| Classer: | Bacilles |
| Commander: | Lactobacilles |
| Famille: | Streptococcacées |
| Genre: | Streptocoque |
| Espèce: |
S. mutans
|
| Nom binomial | |
|
Streptocoque mutant Clarke 1924
|
|
Streptococcus mutans est un anaérobie facultatif , gram-positive coccus (ronde bactérie )trouve couramment dans l' humain de la cavité buccale et est un facteur important de la carie dentaire . Il fait partie des " streptocoques " (pluriel, minuscule non italique), un nom général informel pour toutes les espèces du genre Streptococcus . Le microbe a été décrit pour la première fois par James Kilian Clarke en 1924.
Cette bactérie, avec l'espèce étroitement apparentée Streptococcus sobrinus , peut cohabiter dans la bouche : les deux contribuent aux maladies bucco-dentaires, et le coût de les différencier dans les tests de laboratoire n'est souvent pas cliniquement nécessaire. Par conséquent, à des fins cliniques, ils sont souvent considérés ensemble comme un groupe, appelé streptocoques mutans (pluriel, non italique en raison de son nom de groupe informel). Ce regroupement de bactéries similaires avec un tropisme similaire peut également être observé chez les streptocoques viridans , un autre groupe d' espèces de Streptococcus .
Écologie
S. mutans est naturellement présent dans le microbiote oral humain, avec au moins 25 autres espèces de streptocoques oraux. La taxonomie de ces bactéries reste provisoire. Différentes zones de la cavité buccale présentent des niches écologiques différentes, et chaque espèce a des propriétés spécifiques pour coloniser différents sites buccaux. S. mutans est le plus répandu sur les fosses et les fissures , constituant 39% du total des streptocoques dans la cavité buccale. On trouve moins de bactéries S. mutans à la surface buccale (2 à 9 %).
La co-agrégation bactério-fongique peut aider à augmenter le potentiel cariogène de S.mutans . Une relation symbiotique avec S. mutans et Candida Albicans conduit à une production accrue de glucanes et à une formation accrue de biofilm. Ceci amplifie donc l'effet cariogène de S.mutans .
Les streptocoques oraux contiennent à la fois des bactéries inoffensives et nocives. Cependant, dans des conditions particulières, les streptocoques commensaux peuvent devenir des agents pathogènes opportunistes, initiant la maladie et endommageant l'hôte. Les déséquilibres dans le biote microbien peuvent déclencher des maladies bucco-dentaires.
Candida albicans est une levure pathogène opportuniste qui peut être trouvée dans la cavité buccale. Sa présence dans le biofilm favorise des niveaux plus élevés de Streptococcus mutans lors de l'examen des caries de la petite enfance. Il stimule la formation demicrocoloniesde S. mutans . Ceci est obtenu grâce à de faibles concentrations de métabolites inter-royaumes, tels que le farnesol , dérivés du biofilm . Il a été suggéré que lorsque les deux microbes sont présents, plus de matrice de biofilm est produite, avec une plus grande densité. Lorsque le farnesol est en forte concentration, il inhibe la croissance à la fois de S. mutans et de C. albicans . Cela diminue la pathogenèse du biofilm, et donc sonpotentiel de promotion des caries . Cela offre la possibilité d'utiliser un antifongique dans la prévention des caries dentaires .
Rôle dans la maladie
Carie
Les premiers colonisateurs de la surface dentaire sont principalement Neisseria spp. et les streptocoques , y compris S. mutans . Ils doivent résister aux forces de nettoyage bucco-dentaire (par exemple la salive et les mouvements de la langue) et adhérer suffisamment aux tissus durs dentaires. La croissance et le métabolisme de ces espèces pionnières modifient les conditions environnementales locales (par exemple, Eh, pH, coagrégation et disponibilité du substrat), permettant ainsi aux organismes plus exigeants de coloniser davantage après eux, formant la plaque dentaire . Avec S. sobrinus , S. mutans joue un rôle majeur dans la carie dentaire, en métabolisant le saccharose en acide lactique . L' environnement acide créé dans la bouche par ce processus est ce qui rend l' émail dentaire hautement minéralisé vulnérable à la carie. S. mutans est l'un des rares organismes spécialisés équipés de récepteurs qui améliorent l'adhérence à la surface des dents. S. mutans utilise l'enzyme glucansucrase pour convertir le saccharose en un polysaccharide collant, extracellulaire, à base de dextrane qui leur permet de se regrouper et de former une plaque. S. mutans produit du dextrane via l'enzyme dextrane- saccharase (une hexosyltransférase ) en utilisant le saccharose comme substrat dans la réaction suivante :
- n saccharose → (glucose) n + n fructose
Le saccharose est le seul sucre que les bactéries peuvent utiliser pour former ce polysaccharide collant.
Cependant, d'autres sucres - glucose , fructose , lactose - peuvent également être digérés par S. mutans , mais ils produisent de l'acide lactique comme produit final. La combinaison de plaque et d'acide conduit à la carie dentaire. En raison du rôle que joue S. mutans dans la carie dentaire, de nombreuses tentatives ont été faites pour créer un vaccin pour l'organisme. Jusqu'à présent, ces vaccins n'ont pas été efficaces chez l'homme. Récemment, il a été démontré que les protéines impliquées dans la colonisation des dents par S. mutans produisent des anticorps qui inhibent le processus cariogène . Une molécule récemment synthétisée à l'université de Yale et à l'université du Chili, appelée Keep 32 , serait capable de tuer S. mutans . Un autre candidat est un peptide appelé C16G2, synthétisé à l'UCLA.
On pense que Streptococcus mutans a acquis le gène qui lui permet de produire des biofilms par transfert horizontal de gènes avec d'autres espèces bactériennes lactiques, telles que Lactobacillus .
La vie dans la cavité buccale
Survivant dans la cavité buccale, S. mutans est le principal agent causal et l'espèce pathogène responsable des caries dentaires (carie dentaire ou caries) spécifiquement aux stades d'initiation et de développement.
La plaque dentaire , généralement le précurseur de la carie dentaire, contient plus de 600 micro-organismes différents, contribuant à l'environnement dynamique global de la cavité buccale qui subit fréquemment des changements rapides de pH, de disponibilité des nutriments et de tension d'oxygène. La plaque dentaire adhère aux dents et se compose de cellules bactériennes, tandis que la plaque est le biofilm à la surface des dents. La plaque dentaire et S. mutans sont fréquemment exposés à des « composés toxiques » provenant des produits de santé bucco-dentaire, des additifs alimentaires et du tabac.
Alors que S. mutans se développe dans le biofilm, les cellules maintiennent un équilibre métabolique qui implique la production et la détoxification. Le biofilm est un agrégat de micro-organismes dans lequel les cellules adhèrent les unes aux autres ou à une surface. Les bactéries de la communauté des biofilms peuvent en fait générer divers composés toxiques qui interfèrent avec la croissance d'autres bactéries concurrentes.
S. mutans a développé au fil du temps des stratégies pour coloniser avec succès et maintenir une présence dominante dans la cavité buccale. Le biofilm buccal est continuellement mis à l'épreuve par les changements des conditions environnementales. En réponse à de tels changements, la communauté bactérienne a évolué avec des membres individuels et leurs fonctions spécifiques pour survivre dans la cavité buccale. S. mutans a pu évoluer à partir de conditions nutritionnelles limitantes pour se protéger dans des conditions extrêmes. Les streptocoques représentent 20 % des bactéries buccales et déterminent effectivement le développement des biofilms. Bien que S. mutans puisse être contrarié par les colonisateurs pionniers, une fois qu'ils deviennent dominants dans les biofilms oraux, les caries dentaires peuvent se développer et prospérer.
Potentiel cariogène
L'agent causal de la carie dentaire est associé à sa capacité à métaboliser divers sucres, à former un biofilm robuste, à produire une quantité abondante d'acide lactique et à prospérer dans l'environnement acide qu'il génère. Une étude sur le pH de la plaque a indiqué que le pH critique pour une déminéralisation accrue des tissus dentaires durs (émail et dentine) est de 5,5. La courbe de Stephan illustre à quelle vitesse le pH de la plaque peut tomber en dessous de 5,5 après une collation ou un repas.
La carie dentaire est une maladie bucco-dentaire liée au biofilm dentaire associée à une consommation accrue de sucre alimentaire et de glucides fermentescibles. Lorsque les biofilms dentaires restent sur la surface des dents, en plus d'une exposition fréquente aux sucres, les bactéries acidogènes (membres des biofilms dentaires) métabolisent les sucres en acides organiques. La carie dentaire non traitée est la maladie la plus courante chez l'homme dans le monde . La persistance de cette condition acide favorise la prolifération des bactéries acidogènes et aciduriques en raison de leur capacité à survivre dans un environnement à faible pH. L'environnement à faible pH dans la matrice du biofilm érode la surface des dents et commence "l'initiation" de la carie dentaire. Streptococcus mutans est une bactérie qui est répandue dans l'environnement buccal et est considérée comme un micro-organisme vital qui contribue à cette initiation. S. mutans se développe dans des conditions acides, devenant la principale bactérie dans les cultures dont le pH est constamment réduit . Si l'adhérence de S. mutans à la surface des dents ou la capacité physiologique (acidogénicité et acidurité) de S. mutans dans les biofilms dentaires peut être réduite ou éliminée, le potentiel d'acidification des biofilms dentaires et des formations de cavités ultérieures peut être diminué.
Idéalement, nous pouvons arrêter le développement de diverses lésions précoces au-delà du stade des taches blanches. Une fois au-delà, la surface de l'émail est endommagée de manière irréversible et ne peut pas être réparée biologiquement. Chez les jeunes enfants, la douleur d'une lésion carieuse peut être assez pénible et un traitement réparateur peut provoquer une anxiété dentaire précoce. L'anxiété dentaire a des effets d'entraînement pour les professionnels dentaires et les patients. La planification du traitement et donc le succès du traitement peuvent être compromis. Le personnel dentaire peut devenir stressé et frustré lorsqu'il travaille avec des enfants anxieux. Cela peut compromettre leur relation avec l'enfant et ses parents. Des études ont montré l'existence d'un cycle, dans lequel les patients anxieux dentaires évitent de prendre soin de la santé de leurs tissus buccaux. Ils peuvent parfois éviter l'hygiène bucco-dentaire et essaieront d'éviter de demander des soins dentaires jusqu'à ce que la douleur soit insupportable.
La susceptibilité à la maladie varie selon les individus et des mécanismes immunologiques ont été proposés pour conférer une protection ou une susceptibilité à la maladie. Ces mécanismes doivent encore être complètement élucidés mais il semble que bien que les cellules présentatrices d'antigène soient activées par S. mutans in vitro , elles ne répondent pas in vivo . La tolérance immunologique à S. mutans à la surface de la muqueuse peut rendre les individus plus sujets à la colonisation par S. mutans et donc augmenter la sensibilité aux caries dentaires.
Chez les enfants
S. mutans est souvent acquis dans la cavité buccale à la suite d'une éruption dentaire, mais a également été détecté dans la cavité buccale d'enfants prédentés. Elle est généralement, mais pas exclusivement, transmise par transmission verticale de la personne qui s'occupe de l'enfant (généralement la mère) à l'enfant. Cela peut également se produire lorsque le parent met ses lèvres sur le biberon de l'enfant pour le goûter ou pour nettoyer la tétine de l'enfant, puis la met dans la bouche de l'enfant.
Maladie cardiovasculaire
S. mutans est impliqué dans la pathogenèse de certaines maladies cardiovasculaires et est l'espèce bactérienne la plus répandue détectée dans les tissus des valves cardiaques extirpés, ainsi que dans les plaques d' athérome , avec une incidence de 68,6 % et 74,1 %, respectivement. Il a été démontré que Streptococcus sanguinis , étroitement apparenté à S. mutans et également présent dans la cavité buccale, provoque une endocardite infectieuse.
Streptococcus mutans a été associé à une bactériémie et à une endocardite infectieuse (EI). IE est divisé en formes aiguës et subaiguës, et la bactérie est isolée dans les cas subaigus. Les symptômes courants sont : fièvre, frissons, sueurs, anorexie, perte de poids et malaise.
S. mutans a été classé en quatre sérotypes ; c, e, f et k. La classification des sérotypes est élaborée à partir de la composition chimique des polymères rhamnose-glucose spécifiques du sérotype. Par exemple, le sérotype k initialement trouvé dans les isolats sanguins présente une forte réduction des chaînes latérales de glucose attachées au squelette du rhamnose. S. mutans possède les antigènes protéiques de surface suivants : glucosyltransférases, antigène protéique et protéines de liaison au glucane. Si ces antigènes protéiques de surface ne sont pas présents, alors la bactérie est un mutant défectif en antigène protéique avec le moins de susceptibilité à la phagocytose, causant ainsi le moins de dommages aux cellules.
De plus, des expériences chez le rat ont montré que l'infection par de tels mutants de streptocoque défectueux ( souches de S. mutans sans glucosyltransférases isolées d'une valve cardiaque détruite d'un patient atteint d'endocardite infectieuse) entraînait une durée de bactériémie plus longue. Les résultats démontrent que la virulence de l'endocardite infectieuse causée par S. mutans est liée aux composants spécifiques de la surface cellulaire présents.
De plus, l' ADN de S. mutans a été trouvé dans des échantillons cardiovasculaires à un rapport plus élevé que d'autres bactéries parodontales. Cela met en évidence son implication possible dans divers types de maladies cardiovasculaires, et pas seulement dans les bactériémies et les endocardites infectieuses.
Prévention et traitement
La pratique d'une bonne hygiène bucco-dentaire comprenant le brossage quotidien, l'utilisation de la soie dentaire et l'utilisation d'un bain de bouche approprié peut réduire considérablement le nombre de bactéries buccales, y compris S. mutans et inhiber leur prolifération. S. mutans vit souvent dans la plaque dentaire , c'est pourquoi l'élimination mécanique de la plaque est un moyen efficace de s'en débarrasser. La meilleure technique de brossage des dents pour réduire l'accumulation de plaque dentaire, diminuant le risque de carie, est la technique de Bass modifiée. Un brossage deux fois par jour peut aider à réduire le risque de carie. Cependant, il existe certains remèdes utilisés dans le traitement des infections bactériennes buccales, en conjonction avec le nettoyage mécanique. Ceux-ci incluent le fluorure , qui a un effet inhibiteur direct sur l' enzyme énolase , ainsi que la chlorhexidine , qui agit vraisemblablement en interférant avec l'adhérence bactérienne.
De plus, les ions fluorure peuvent nuire au métabolisme des cellules bactériennes. Le fluorure inhibe directement les enzymes glycolytiques et les H+ATPases. Les ions fluorure abaissent également le pH du cytoplasme. Cela signifie qu'il y aura moins d'acide produit pendant la glycolyse bactérienne. Par conséquent, les bains de bouche, les dentifrices, les gels et les vernis fluorés peuvent aider à réduire la prévalence des caries. Cependant, les résultats d'enquêtes sur l'effet du vernis contenant du fluorure sur le niveau de Streptococcus mutans dans l'environnement buccal chez les enfants suggèrent que la réduction des caries ne peut pas être expliquée par une réduction du niveau de Streptococcus mutans dans la salive ou la plaque dentaire. Le traitement au vernis fluoré avec ou sans hygiène dentaire préalable n'a pas d'effet significatif sur la plaque et les niveaux salivaires de S. mutans .
S. mutans sécrète de la Glucosyltransférase sur sa paroi cellulaire, ce qui permet aux bactéries de produire des polysaccharides à partir de saccharose. Ces polysaccharides collants sont responsables de la capacité des bactéries à s'agréger entre elles et à adhérer à l'émail des dents, c'est-à-dire à former des biofilms . L'utilisation de l'immunoglobuline Y anti-glucosyltransférase associée aux cellules (Anti-CA-gtf) perturbe la capacité de S. mutans à adhérer à l'émail des dents, l'empêchant ainsi de se reproduire. Des études ont montré que l'IgY Anti-CA-gtf est capable de supprimer efficacement et spécifiquement S. mutans dans la cavité buccale.
D'autres mesures préventives courantes se concentrent sur la réduction de la consommation de sucre. Une façon de procéder consiste à utiliser des substituts de sucre tels que le xylitol ou l'érythritol qui ne peuvent pas être métabolisés en sucres qui améliorent normalement la croissance de S. mutans . La molécule xylitol, un sucre à 5 carbones, perturbe la production d'énergie de S.mutans en formant un intermédiaire toxique lors de la glycolyse. Divers autres remèdes naturels ont été suggérés ou étudiés dans une certaine mesure, notamment l' extrait de racine de réglisse déglycyrrhizinée , l' huile d'arbre à thé , le macelignan (présent dans la muscade ), les curcuminoïdes (les principaux composants du curcuma ) et l' eugénol (présent dans les feuilles de laurier, les feuilles de cannelle et clous de girofle). De plus, divers thés ont été testés pour leur activité contre S. mutans et d'autres avantages dentaires. Cependant, aucun de ces remèdes n'a fait l'objet d'essais cliniques ou n'est recommandé par les groupes de santé dentaire traditionnels pour traiter S. mutans .
L'ajout de billes de verre bioactives aux composites dentaires réduit la pénétration de Streptococcus mutans dans les espaces marginaux entre la dent et le composite. Ils ont des propriétés antimicrobiennes, réduisant la pénétration bactérienne. Cela diminue le risque de développer des caries secondaires, une cause fréquente d'échec des restaurations dentaires . Cela signifie que la longévité et l'efficacité des restaurations composites peuvent être améliorées.
Survie dans des conditions stressantes
Les conditions dans la cavité buccale sont diverses et complexes, changeant fréquemment d'un extrême à l'autre. Ainsi, pour survivre dans la cavité buccale, S. mutans doit tolérer rapidement des fluctuations environnementales sévères et une exposition à divers agents antimicrobiens pour survivre. La transformation est une adaptation bactérienne impliquant le transfert d'ADN d'une bactérie à une autre à travers le milieu environnant. La transformation est une forme primitive de reproduction sexuée . Pour qu'une bactérie puisse se lier, absorber et recombiner l'ADN exogène dans son chromosome, elle doit entrer dans un état physiologique spécial appelé « compétence » . Chez S. mutans , un système de signalisation à détection de quorum de phéromone peptidique contrôle la compétence génétique. Ce système fonctionne de manière optimale lorsque les cellules de S. mutans sont dans des biofilms surpeuplés. Les cellules de S. mutans qui poussent dans un biofilm sont transformées à un taux de 10 à 600 fois plus élevé que les cellules individuelles qui poussent dans des conditions non surpeuplées (cellules planctoniques). L'induction de la compétence semble être une adaptation pour réparer les dommages à l'ADN causés par des conditions de surpeuplement et de stress.
Connaître le quorum-sensing donne lieu au développement potentiel de médicaments et de thérapies. Les peptides à détection de quorum peuvent également être manipulés pour provoquer le suicide de la cible. De plus, l'extinction du quorum sensing peut conduire à la prévention de la résistance aux antibiotiques.
Évolution
Trois traits clés ont évolué chez S. mutans et ont augmenté sa virulence en améliorant son adaptabilité à la cavité buccale : une production accrue d'acides organiques, la capacité de former des biofilms sur les surfaces dures des dents et la capacité de survivre et de prospérer dans un pH bas. environnement.
Au cours de son évolution, S. mutans a acquis la capacité d'augmenter la quantité de glucides qu'il pouvait métaboliser et, par conséquent, davantage d'acide organique a été produit en tant que sous-produit. Ceci est important dans la formation de caries dentaires car une acidité accrue dans la cavité buccale amplifie le taux de déminéralisation de la dent, ce qui conduit à des lésions carieuses. On pense que le trait a évolué chez S. mutans par transfert latéral de gènes avec une autre espèce bactérienne présente dans la cavité buccale. Il existe plusieurs gènes, SMU.438 et SMU.1561, impliqués dans le métabolisme des glucides qui sont régulés à la hausse chez S. mutans . Ces gènes provenaient probablement de Lactococcus lactis et S. gallolyticus , respectivement.
Un autre exemple de transfert latéral de gènes est responsable de l' acquisition par S. mutans du gène de la glucosyltransférase (GTF). Les gènes GTF trouvés dans S. mutans sont très probablement dérivés d'autres bactéries anaérobies présentes dans la cavité buccale, telles que Lactobacillus ou Leuconostoc . De plus, les gènes GTF dans S. mutans présentent une homologie avec des gènes similaires trouvés dans Lactobacillus et Leuconostoc . On pense que le gène ancestral commun a été utilisé pour l'hydrolyse et la liaison des glucides.
Le troisième trait qui a évolué chez S. mutans est sa capacité non seulement à survivre, mais aussi à prospérer dans des conditions acides. Ce trait confère à S. mutans un avantage sélectif sur les autres membres du microbiote buccal. En conséquence, S. mutans pourrait supplanter d'autres espèces et occuper des régions supplémentaires de la bouche, telles que les plaques dentaires avancées , qui peuvent être aussi acides que pH 4,0. La sélection naturelle est très probablement le principal mécanisme évolutif responsable de ce trait.
En discutant de l'évolution de S. mutans , il est impératif d'inclure le rôle que les humains ont joué et la co-évolution qui s'est produite entre les deux espèces. Comme les humains ont évolué anthropologiquement, les bactéries ont évolué biologiquement. Il est largement admis que l'avènement de l'agriculture dans les premières populations humaines a fourni les conditions nécessaires à S. mutans pour évoluer en la bactérie virulente qu'elle est aujourd'hui. L'agriculture a introduit des aliments fermentés, ainsi que des aliments plus riches en glucides, dans le régime alimentaire des populations humaines historiques. Ces nouveaux aliments ont introduit de nouvelles bactéries dans la cavité buccale et créé de nouvelles conditions environnementales. Par exemple, Lactobacillus ou Leuconostoc se trouvent généralement dans des aliments tels que le yogourt et le vin. En outre, consommer plus de glucides a augmenté la quantité de sucres disponibles pour le métabolisme de S. mutans et a abaissé le pH de la cavité buccale. Ce nouvel habitat acide sélectionnerait les bactéries qui pourraient survivre et se reproduire à un pH inférieur.
Un autre changement important dans l'environnement oral s'est produit pendant la révolution industrielle . Un raffinage et une fabrication plus efficaces des denrées alimentaires ont augmenté la disponibilité et la quantité de saccharose consommée par les humains. Cela a fourni à S. mutans plus de ressources énergétiques et a ainsi exacerbé un taux déjà croissant de caries dentaires. Le sucre raffiné est du saccharose pur, le seul sucre qui peut être converti en glucanes collants, permettant aux bactéries de former une plaque épaisse et fortement adhérente.
