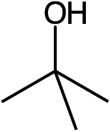
tert -Alcool butylique - tert-Butyl alcohol
|
|
|||

|
|||
| Noms | |||
|---|---|---|---|
|
Nom IUPAC préféré
2-Méthylpropane-2-ol |
|||
Autres noms
|
|||
| Identifiants | |||
|
Modèle 3D ( JSmol )
|
|||
| 906698 | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| Banque de médicaments | |||
| Carte d'information de l'ECHA |
100.000.809 |
||
| Numéro CE | |||
| 1833 | |||
| Engrener | tert-butyle+alcool | ||
|
CID PubChem
|
|||
| Numéro RTECS | |||
| UNII | |||
| Numéro ONU | 1120 | ||
|
Tableau de bord CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriétés | |||
| C 4 H 10 O | |||
| Masse molaire | 74,123 g·mol -1 | ||
| Apparence | Solide incolore | ||
| Odeur | Camphrée | ||
| Densité | 0,775 g/mL | ||
| Point de fusion | 25 à 26 °C ; 77 à 79 °F ; 298 à 299 K | ||
| Point d'ébullition | 82 à 83 °C ; 179 à 181 °F ; 355 à 356 K | ||
| miscible | |||
| log P | 0,584 | ||
| La pression de vapeur | 4,1 kPa (à 20 °C) | ||
| Acidité (p K a ) | 16,54 | ||
| 5,742 × 10 −5 cm 3 /mol | |||
|
Indice de réfraction ( n D )
|
1,387 | ||
| 1.31D | |||
| Thermochimie | |||
|
Capacité calorifique ( C )
|
215,37 J K -1 mol -1 | ||
|
Entropie molaire standard ( S |
189,5 JK -1 mol -1 | ||
|
Std enthalpie de
formation (Δ f H ⦵ 298 ) |
-360,04 à -358,36 kJ mol -1 | ||
|
Std enthalpie de
combustion (Δ c H ⦵ 298 ) |
−2.64479 à −2.64321 MJ mol −1 | ||
| Dangers | |||
| Fiche de données de sécurité | inchem.org | ||
| Pictogrammes SGH |
 
|
||
| Mention d'avertissement SGH | Danger | ||
| H225 , H319 , H332 , H335 | |||
| P210 , P261 , P305+351+338 | |||
| NFPA 704 (diamant de feu) | |||
| point de rupture | 11 °C (52 °F; 284 K) | ||
| 480 °C (896 °F; 753 K) | |||
| Limites d'explosivité | 2,4-8,0% | ||
| Dose ou concentration létale (LD, LC) : | |||
|
DL 50 ( dose médiane )
|
3559 mg/kg (lapin, oral) 3500 mg/kg (rat, oral) |
||
| NIOSH (limites d'exposition pour la santé aux États-Unis) : | |||
|
PEL (Autorisé)
|
TWA 100 ppm (300 mg/m 3 ) | ||
|
REL (recommandé)
|
TWA 100 ppm (300 mg/m 3 ) ST 150 ppm (450 mg/m 3 ) | ||
|
IDLH (Danger immédiat)
|
1600 ppm | ||
| Composés apparentés | |||
|
Butanols apparentés
|
2-Butanol |
||
|
Composés apparentés
|
2-Méthyl-2-butanol Triméthylsilanol |
||
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 °C [77 °F], 100 kPa). |
|||
|
|
|||
| Références de l'infobox | |||
L' alcool tert- butylique est l' alcool tertiaire le plus simple, avec une formule de (CH 3 ) 3 COH (parfois représenté par t -BuOH). C'est l'un des quatre isomères du butanol . L' alcool tert- butylique est un solide incolore qui fond près de la température ambiante etdégage une odeur de camphre . Il est miscible à l' eau , à l' éthanol et à l'éther diéthylique .
Occurrence naturelle
L' alcool tert- butylique a été identifié dans la bière et les pois chiches . On le trouve également dans le manioc , qui est utilisé comme ingrédient de fermentation dans certaines boissons alcoolisées .
Préparation
L' alcool tert- butylique est dérivé commercialement de l' isobutane en tant que coproduit de la production d' oxyde de propylène . Il peut également être produit par l' hydratation catalytique de l' isobutylène , ou par une réaction de Grignard entre l' acétone et le chlorure de méthylmagnésium .
La purification ne peut pas être effectuée par simple distillation en raison de la formation d'un azéotrope avec l'eau, bien que le séchage initial du solvant contenant de grandes quantités d'eau soit effectué en ajoutant du benzène pour former un azéotrope tertiaire et en distillant l'eau. De plus petites quantités d'eau sont éliminées par séchage avec de l'oxyde de calcium (CaO), du carbonate de potassium (K 2 CO 3 ), du sulfate de calcium (CaSO 4 ) ou du sulfate de magnésium (MgSO 4 ), suivi d'une distillation fractionnée. L' alcool tert- butylique anhydre est obtenu par reflux et distillation supplémentaires à partir de magnésium activé avec de l'iode ou des métaux alcalins tels que le sodium ou le potassium. D' autres méthodes comprennent l'utilisation de 4 Å tamis moléculaires , l' aluminium tert -butylate , l' hydrure de calcium (CaH 2 ), ou par cristallisation fractionnée sous atmosphère inerte.
Applications
L' alcool tert- butylique est utilisé comme solvant, dénaturant de l' éthanol , ingrédient de décapant pour peinture et amplificateur d' octane et oxygénant de l' essence . Il est un intermédiaire utilisé chimique pour produire un méthyle tert - butyle éther (MTBE) et éthyl tert - butyl éther (ETBE) par réaction avec le methanol et l' éthanol , respectivement, et tert - butyle hydroperoxyde (TBHP) par réaction avec le peroxyde d'hydrogène .
Réactions
En tant qu'alcool tertiaire, l'alcool tert- butylique est plus résistant à l'oxydation que les autres isomères du butanol.
L' alcool tert- butylique est déprotoné avec une base forte pour donner l' alcoxyde . Le tert- butoxyde de potassium est particulièrement courant , qui est préparé en traitant le tert- butanol avec du potassium métallique.
- K + t -BuOH → t -BuO − K + + 1/2 H 2
Le tert- butoxyde est une base forte non nucléophile en chimie organique. Il extrait facilement les protons acides des substrats, mais sa masse stérique empêche le groupe de participer à la substitution nucléophile , comme dans une synthèse d'éther de Williamson ou une réaction S N 2 .
L' alcool tert- butylique réagit avec le chlorure d'hydrogène pour former du chlorure de tert- butyle .
O-Chloration de l'alcool tert-butylique avec de l'acide hypochloreux pour donner l'hypochlorite de tert-butyle :
- (CH 3 ) 3 COH + HOCl → (CH 3 ) 3 COCl + H 2 O
Pharmacologie et toxicologie
Il existe des données limitées sur la pharmacologie et la toxicologie du tert-butanol chez l'homme et d'autres animaux. L'exposition humaine peut se produire en raison du métabolisme oxygéné du carburant. Le tert-butanol est faiblement absorbé par la peau mais rapidement absorbé en cas d'inhalation ou d'ingestion. Le tert-butanol est irritant pour la peau ou les yeux. La toxicité des doses uniques est généralement faible, mais des doses élevées peuvent produire un effet sédatif ou anesthésique.
Remarques
Les références
Liens externes
- Carte internationale de sécurité chimique 0114
- Guide de poche du NIOSH sur les risques chimiques. "#0078" . Institut national pour la sécurité et la santé au travail (NIOSH).
- Critères de santé environnementale IPCS 65 : Butanols : quatre isomères
- Guide de santé et de sécurité IPCS 7 : tert- butanol