Acide triflique - Triflic acid
|
|||
|
|
|||
| Des noms | |||
|---|---|---|---|
|
Nom IUPAC
Acide trifluorométhanesulfonique
|
|||
| Autres noms
Acide triflique
|
|||
| Identifiants | |||
|
Modèle 3D ( JSmol )
|
|||
| ChEBI | |||
| ChemSpider | |||
| Carte Info ECHA |
100.014.625 |
||
|
PubChem CID
|
|||
| UNII | |||
|
Tableau de bord CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriétés | |||
| CF 3 SO 3 H | |||
| Masse molaire | 150,07121 g / mol | ||
| Apparence | Liquide incolore | ||
| Densité | 1,696 g / mL | ||
| Point de fusion | −40 ° C (−40 ° F; 233 K) | ||
| Point d'ébullition | 162 ° C (324 ° F; 435 K) | ||
| Miscible | |||
| Acidité (p K a ) | -14,7 (± 2,0) | ||
| Base conjuguée | Anion triflate | ||
| Dangers | |||
| Principaux dangers | Provoque de graves brûlures acides | ||
| NFPA 704 (diamant de feu) | |||
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Références Infobox | |||
L' acide triflique , le nom abrégé de l' acide trifluorométhanesulfonique , TFMS , CELI , HOTf ou TfOH , est un acide sulfonique répondant à la formule chimique CF 3 SO 3 H. Il est l' un des plus puissants connus des acides . L'acide triflique est principalement utilisé dans la recherche comme catalyseur d' estérification . C'est un liquide hygroscopique , incolore, légèrement visqueux et soluble dans les solvants polaires .
La synthèse
L'acide trifluorométhanesulfonique est produit industriellement par fluoration électrochimique (ECF) d' acide méthanesulfonique :
- CH 3 SO 3 H + 4 HF → CF 3 SO 2 F + H 2 O + 3 H 2
Le CF résultant 3 SO 2 F est hydrolysée, et le sel de triflate obtenu est preprotonated. Alternativement, l'acide trifluorométhanesulfonique se produit par oxydation du chlorure de trifluorométhyl sulfényle :
- CF 3 SCl + 2 Cl 2 + 3 H 2 O → CF 3 SO 3 H + 5 HCl
L'acide triflique est purifié par distillation à partir de l'anhydride triflique .
Historique
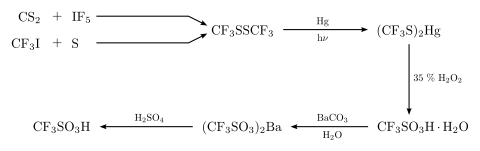
L'acide trifluorométhanesulfonique a été synthétisé pour la première fois en 1954 par Robert Haszeldine et Kidd par la réaction suivante:
Réactions
En tant qu'acide
En laboratoire, l'acide triflique est utile dans les protonations car la base conjuguée de l'acide triflique est non nucléophile. Il est également utilisé comme titrant acide dans le titrage acide-base non aqueux car il se comporte comme un acide fort dans de nombreux solvants ( acétonitrile , acide acétique , etc.) où les acides minéraux courants (tels que HCl ou H 2 SO 4 ) ne sont que modérément fort.
Avec a K a = 5 × 10 14 , p K a −14,7 ± 2,0, l'acide triflique est qualifié de superacide . Il doit nombre de ses propriétés utiles à sa grande stabilité thermique et chimique. L'acide et sa base conjuguée CF 3 SO -
3 , connu sous le nom de triflate , résiste aux réactions d' oxydation / réduction , alors que de nombreux acides forts sont oxydants, par exemple l'acide perchlorique ou nitrique . Recommandant en outre son utilisation, l'acide triflique ne sulfonate pas les substrats, ce qui peut être un problème avec l'acide sulfurique , l'acide fluorosulfurique et l'acide chlorosulfonique . Voici une sulfonation prototypique, que HOTf ne subit pas :
- C 6 H 6 + H 2 SO 4 → C 6 H 5 (SO 3 H) + H 2 O
L'acide triflique se dégage dans l'air humide et forme un monohydrate solide stable, CF 3 SO 3 H · H 2 O, point de fusion 34 ° C.
Sel et formation de complexes
Le ligand triflate est labile, reflétant sa faible basicité. L'acide trifluorométhanesulfonique réagit de manière exothermique avec les carbonates , hydroxydes et oxydes métalliques . La synthèse de Cu (OTf) 2 est illustrative .
- CuCO 3 + 2 CF 3 SO 3 H → Cu (O 3 SCF 3 ) 2 + H 2 O + CO 2
Les ligands chlorure peuvent être convertis en triflates correspondants:
- 3 CF 3 SO 3 H + [Co (NH 3 ) 5 Cl] Cl 2 → [Co (NH 3 ) 5 O 3 SCF 3 ] (O 3 SCF 3 ) 2 + 3 HCl
Cette conversion est effectuée dans du HOTf pur à 100 ° C, suivie d'une précipitation du sel lors de l'addition d'éther.
Chimie organique
L'acide triflique réagit avec les halogénures d'acyle pour donner des anhydrides triflates mixtes, qui sont des agents acylants puissants, par exemple dans les réactions de Friedel-Crafts .
- CH 3 C (O) Cl + CF 3 SO 3 H → CH 3 C (O) OSO 2 CF 3 + HCl
- CH 3 C (O) OSO 2 CF 3 + C 6 H 6 → CH 3 C (O) C 6 H 5 + CF 3 SO 3 H
L'acide triflique catalyse la réaction des composés aromatiques avec les chlorures de sulfonyle, probablement aussi par l'intermédiaire d'un anhydride mixte de l'acide sulfonique.
L'acide triflique favorise d'autres réactions de type Friedel – Crafts, notamment le craquage des alcanes et l'alkylation des alcènes, qui sont très importantes pour l'industrie pétrolière. Ces catalyseurs dérivés d'acide triflique sont très efficaces pour l'isomérisation d'hydrocarbures à chaîne droite ou légèrement ramifiés qui peuvent augmenter l' indice d'octane d'un carburant à base de pétrole particulier.
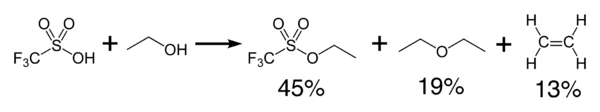
L'acide triflique réagit de manière exothermique avec les alcools pour produire des éthers et des oléfines.
La déshydratation donne l' anhydride d'acide , l'anhydride trifluorométhanesulfonique , (CF 3 SO 2 ) 2 O.
Sécurité
L'acide triflique est l'un des acides les plus forts. Le contact avec la peau provoque de graves brûlures avec une destruction des tissus retardée. Lors de l'inhalation, il provoque des spasmes mortels, une inflammation et un œdème .
Comme l'acide sulfurique, l'acide triflique doit être ajouté lentement aux solvants polaires pour éviter un emballement thermique .