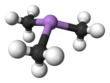
Triméthylarsine - Trimethylarsine
|
|
|||
| Noms | |||
|---|---|---|---|
|
Nom IUPAC préféré
Triméthylarsane |
|||
| Autres noms | |||
| Identifiants | |||
|
Modèle 3D ( JSmol )
|
|||
| 1730780 | |||
| ChEBI | |||
| ChemSpider | |||
| Carte d'information de l'ECHA |
100.008.925 |
||
| Numéro CE | |||
| 141657 | |||
| Engrener | Triméthylarsine | ||
|
CID PubChem
|
|||
| Numéro RTECS | |||
| UNII | |||
|
Tableau de bord CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriétés | |||
| C 3 H 9 Comme | |||
| Masse molaire | 120,027 g·mol -1 | ||
| Apparence | Liquide incolore | ||
| Densité | 1,124 g cm -3 | ||
| Point de fusion | −87,3 °C (−125,1 °F; 185,8 K) | ||
| Point d'ébullition | 56 °C (133 °F; 329 K) | ||
| Légèrement soluble | |||
| Solubilité dans d'autres solvants | solvants organiques | ||
| Structure | |||
| Pyramidale trigonale | |||
| 0,86 D | |||
| Dangers | |||
| Principaux dangers | Inflammable | ||
| Fiche de données de sécurité |
Voir : page de données FDS externe |
||
| Pictogrammes SGH |
 
|
||
| Mention d'avertissement SGH | Danger | ||
| H331 , H301 , H410 | |||
| point de rupture | −25 °C (−13 °F; 248 K) | ||
| Composés apparentés | |||
|
Composés apparentés
|
Acide cacodylique Triphénylarsine Pentaméthylarsenic Triméthylphosphine Triméthylamine |
||
| Page de données supplémentaires | |||
|
Indice de réfraction ( n ), Constante diélectrique (ε r ), etc. |
|||
|
Données thermodynamiques |
Comportement des phases solide-liquide-gaz |
||
| UV , IR , RMN , MS | |||
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 °C [77 °F], 100 kPa). |
|||
|
|
|||
| Références de l'infobox | |||
La triméthylarsine (en abrégé TMA ou TMA) est le composé chimique de formule (CH 3 ) 3 As, communément abrégé As Me 3 ou TMA. Ce dérivé organique de l' arsine a été utilisé comme source d' arsenic dans l' industrie microélectronique , élément constitutif d'autres composés organoarsenicaux et sert de ligand en chimie de coordination . Il a une odeur distincte "d' ail ". La triméthylarsine avait été découverte dès 1854.
Structure et préparation
AsMe 3 est une molécule pyramidale. Les distances As-C sont en moyenne de 1,519 et les angles C-As-C sont de 91,83°
La triméthylarsine peut être préparée par traitement de l'oxyde d'arsenic avec du triméthylaluminium :
- As 2 O 3 + 1,5 [AlMe 3 ] 2 → 2 AsMe 3 + 3/n (MeAl-O) n
Occurrence et réactions
La triméthylarsine est le sous-produit volatil de l'action microbienne sur les formes inorganiques de l'arsenic qui sont naturellement présentes dans les roches et les sols au niveau des parties par million. La triméthylarsine n'a été signalée qu'à des niveaux de traces (parties par milliard) dans les gaz d'enfouissement d'Allemagne, du Canada et des États-Unis, et est le principal composé contenant de l'arsenic dans le gaz.
La triméthylarsine est pyrophorique en raison de la nature exothermique de la réaction suivante, qui initie la combustion :
- AsMe 3 + 1/2 O 2 → OAsMe 3 (TMAO)
Histoire
On a supposé que les événements d'empoisonnement dus à un gaz produit par certains microbes étaient associés à l'arsenic dans la peinture. En 1893, le médecin italien Bartolomeo Gosio publia ses résultats sur le "gaz Gosio" qui s'avéra par la suite contenir de la triméthylarsine. Dans des conditions humides, la moisissure Scopulariopsis brevicaulis produit des quantités importantes de méthylarsine via la méthylation de pigments inorganiques contenant de l'arsenic , en particulier le vert de Paris et le vert de Scheele , qui étaient autrefois utilisés dans les papiers peints d'intérieur. Des études plus récentes montrent que la triméthylarsine a une faible toxicité et ne pourrait donc pas expliquer la mort et les graves problèmes de santé observés au 19ème siècle.
Sécurité
La triméthylarsine est potentiellement dangereuse, bien que sa toxicité soit souvent surestimée.