Oxyde de triphénylphosphine - Triphenylphosphine oxide

|
|

|
|

|
|
| Des noms | |
|---|---|
|
Nom IUPAC préféré
Triphényl-λ 5 -phosphanone |
|
| Autres noms
Oxyde de triphénylphosphine
|
|
| Identifiants | |
|
Modèle 3D ( JSmol )
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| Carte Info ECHA |
100.011.217 |
|
PubChem CID
|
|
| Numéro RTECS | |
| UNII | |
|
Tableau de bord CompTox ( EPA )
|
|
|
|
|
|
| Propriétés | |
| C 18 H 15 OP | |
| Masse molaire | 278,29 g / mol |
| Apparence | cristaux blancs |
| Densité | 1,212 g / cm ^ 3 |
| Point de fusion | 154 à 158 ° C (309 à 316 ° F; 427 à 431 K) |
| Point d'ébullition | 360 ° C (680 ° F; 633 K) |
| faible | |
| Solubilité dans d'autres solvants | solvants organiques polaires |
| Structure | |
| tétraédrique | |
| Dangers | |
| Principaux dangers | léger |
| Phrases R (obsolètes) | 22-36 / 37/38 |
| Phrases S (obsolètes) | 26 |
| Composés apparentés | |
|
Composés apparentés
|
P (C 6 H 5 ) 3 S ; |
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Références Infobox | |
L'oxyde de triphénylphosphine (souvent abrégé TPPO) est le composé organophosphoré de formule OP (C 6 H 5 ) 3 , également écrit Ph 3 PO ou PPh 3 O (Ph = C 6 H 5 ). Ce composé cristallin incolore est un déchet courant mais potentiellement utile dans les réactions impliquant la triphénylphosphine . C'est un réactif populaire pour induire la cristallisation de composés chimiques.
Structure et propriétés
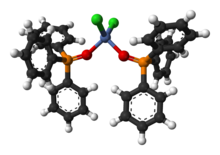
Ph 3 PO est une molécule tétraédrique liée à POCl 3 . Le centre d'oxygène est relativement basique. La rigidité du squelette et la basicité du centre de l'oxygène font de cette espèce un agent populaire pour cristalliser des molécules autrement difficiles à cristalliser. Cette astuce est applicable aux molécules qui ont des atomes d'hydrogène acides, par exemple les phénols .
Jusqu'à présent, plusieurs modifications de Ph 3 PO ont été trouvées: Par exemple, une forme monoclinique cristallise dans le groupe spatial P 2 1 / c avec Z = 4 et a = 15,066 (1) Å, b = 9,037 (2) Å , c = 11,296 (3) Â et ß = 98,47 (1) °. La modification orthorhombique cristallise dans le groupe spatial Pbca avec Z = 4 et 29,089 (3) Å, b = 9,1347 (9), c = 11,261 (1) Å.
En tant que sous-produit de la synthèse organique
Ph 3 PO est un sous-produit de nombreuses réactions utiles en synthèse organique, y compris les réactions de Wittig , Staudinger et Mitsunobu . Il se forme également lorsque PPh 3 Cl 2 est utilisé pour convertir des alcools en chlorures d'alkyle:
- Ph 3 PCl 2 + ROH → Ph 3 PO + HCl + RCl
La triphénylphosphine peut être régénérée à partir de l'oxyde par traitement avec une variété d'agents de désoxygénation, tels que le phosgène ou le trichlorosilane / triéthylamine:
- Ph 3 PO + SiHCl 3 → PPh 3 + 1 / n (OSiCl 2 ) n + HCl
L'oxyde de triphénylphosphine peut être difficile à éliminer des mélanges réactionnels au moyen de la chromatographie. Il est peu soluble dans l'hexane et l'éther diéthylique froid. La trituration ou la chromatographie des produits bruts avec ces solvants conduit souvent à une bonne séparation de l'oxyde de triphénylphosphine. Son élimination est facilitée par la conversion en son complexe Mg (II), qui est peu soluble dans le toluène ou le dichlorométhane et peut être filtré. Procédé de filtration alternative où ZnCl 2 (TPPO) 2 est formé lors de l' addition de ZnCl 2 peut être utilisé avec des solvants plus polaires tels que l' éthanol, l' acétate d' éthyle et le tétrahydrofuranne.
Chimie de coordination
Ph 3 PO est un ligand des centres métalliques « durs ». Un complexe représentatif est l'espèce tétraédrique NiCl 2 (OPPh 3 ) 2 .
Ph 3 PO est une impureté courante dans PPh 3 . L'oxydation du PPh 3 par l'oxygène, y compris l'air, est catalysée par de nombreux ions métalliques:
- 2 PPh 3 + O 2 → 2 Ph 3 PO