Citrate de calcium - Calcium citrate
 Structure 2D du citrate de calcium
|
|
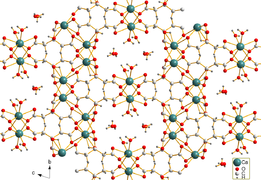 Citrate de calcium tétrahydraté
|
|
 Citrate de calcium tétrahydraté
|
|
| Noms | |
|---|---|
|
Nom IUPAC
Sel de calcium de l'acide 2-hydroxy-1,2,3-propane-tricarboxylique (2:3)
|
|
| Autres noms
E333, dicitrate tricalcique
|
|
| Identifiants | |
|
Modèle 3D ( JSmol )
|
|
| ChEMBL | |
| ChemSpider | |
| Banque de médicaments | |
| Carte d'information de l'ECHA |
100.011.265 |
| Numéro CE | |
| numéro E | E333 (antioxydants, ...) |
|
CID PubChem
|
|
| UNII | |
|
Tableau de bord CompTox ( EPA )
|
|
|
|
|
|
| Propriétés | |
| Ca 3 (C 6 H 5 O 7 ) 2 | |
| Masse molaire | 498,4334 g/mol (anhydre) 570,4945 g/mol (tétrahydraté) |
| Apparence | poudre blanche |
| Odeur | inodore |
| Densité | 1,63 g/cm 3 (anhydre) 2,00 g/cm 3 (tétrahydraté) |
| Point de fusion | Se décompose |
| Point d'ébullition | Se décompose |
| 0,85 g/L (18 °C) 0,95 g/L (25 °C) |
|
| Solubilité | insoluble dans l' alcool |
| Structure | |
| Triclinique (tétrahydraté) | |
| P 1 , n° 2 | |
|
a = 0,59466(4) nm, b = 1,02247(8) nm, c = 1,66496(13) nm
= 72,213(7)°, = 79,718(7)°, = 89,791(6)°
|
|
| Dangers | |
| Principaux dangers | Irritant |
| NFPA 704 (diamant de feu) | |
| Composés apparentés | |
|
Autres cations
|
Citrate de magnésium Citrate de strontium |
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Références de l'infobox | |
Le citrate de calcium est le sel de calcium de l'acide citrique . Il est couramment utilisé comme additif alimentaire ( E333 ), généralement comme conservateur , mais parfois pour la saveur . En ce sens, il est similaire au citrate de sodium . Le citrate de calcium se trouve également dans certains compléments alimentaires de calcium (par exemple Citracal). Le calcium représente 24,1 % du citrate de calcium (anhydre) et 21,1 % du citrate de calcium (tétrahydraté) en masse. Le tétrahydrate est présent dans la nature sous forme de minerai d' Earlandite .
Propriétés chimiques
Le citrate de calcium est peu soluble dans l'eau. Des cristaux en forme d'aiguille de dicitrate tricalcique tétrahydraté [Ca 3 (C 6 H 5 O 7 ) 2 (H 2 O) 2 ]·2H 2 O ont été obtenus par synthèse hydrothermale. La structure cristalline comprend un réseau tridimensionnel dans lequel des cations Ca 2+ coordinés huit fois sont liés par des anions citrate et des liaisons hydrogène entre deux molécules d'eau cristallines non coordonnantes et deux molécules d'eau coordonnantes.
Production
Le citrate de calcium est un intermédiaire dans l'isolement de l'acide citrique du processus de fermentation fongique par lequel l'acide citrique est produit industriellement. L'acide citrique dans la solution de bouillon est neutralisé par l' eau de chaux , précipitant le citrate de calcium insoluble. Celui-ci est ensuite filtré du reste du bouillon et lavé pour donner du citrate de calcium propre.
- 3 Ca(OH) 2(s) + 2 C 6 H 8 O 7(l) → Ca 3 (C 6 H 5 O 7 ) 2(s) + 6 H 2 O (l)
Le citrate de calcium ainsi produit peut être vendu tel quel, ou il peut être converti en acide citrique en utilisant de l'acide sulfurique dilué.
Rôle biologique
Chez de nombreux individus, la biodisponibilité du citrate de calcium est égale à celle du carbonate de calcium moins cher . Cependant, des altérations du tube digestif peuvent modifier la façon dont le calcium est digéré et absorbé. Contrairement au carbonate de calcium, qui est basique et neutralise l'acidité gastrique, le citrate de calcium n'a aucun effet sur l'acidité gastrique. Le carbonate de calcium est plus difficile à digérer que le citrate de calcium, et le carbonate de calcium comporte un risque de « rebond acide » (l'estomac surcompense en produisant plus d'acide), donc les personnes sensibles aux antiacides ou qui ont des difficultés à produire suffisamment d'acide gastrique peuvent choisir le citrate de calcium sur du carbonate de calcium pour la supplémentation. Selon des recherches récentes sur l'absorption du calcium après un pontage gastrique, le citrate de calcium pourrait avoir amélioré la biodisponibilité par rapport au carbonate de calcium chez les patients ayant un pontage gastrique Roux-en-Y qui prennent du citrate de calcium comme complément alimentaire après la chirurgie. Cela est principalement dû aux changements liés à l'endroit où se produit l'absorption du calcium dans le tube digestif de ces personnes.

