DCMU - DCMU
|
|

|
|
| Noms | |
|---|---|
|
Nom IUPAC préféré
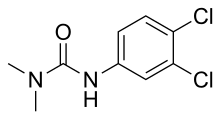
N ′-(3,4-Dichlorophényl) -N , N -diméthylurée |
|
| Autres noms
3-(3,4-Dichlorophényl)-1,1-diméthylurée, Karmex, Diuron, Direx
|
|
| Identifiants | |
|
Modèle 3D ( JSmol )
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| Carte d'information de l'ECHA |
100.005.778 |
| Numéro CE | |
| KEGG | |
|
CID PubChem
|
|
| Numéro RTECS | |
| UNII | |
| Numéro ONU | 3077, 2767 |
|
Tableau de bord CompTox ( EPA )
|
|
|
|
|
|
| Propriétés | |
| C 9 H 10 Cl 2 N 2 O | |
| Masse molaire | 233,09 g·mol -1 |
| Apparence | solide cristallin blanc |
| Densité | 1,48 g / cm 3 |
| Point de fusion | 158 °C (316 °F; 431 K) |
| Point d'ébullition | 180 °C (356 °F; 453 K) |
| 42 mg/L | |
| La pression de vapeur | 0,000000002 mmHg (20°C) |
| Dangers | |
| Pictogrammes SGH |
  
|
| Mention d'avertissement SGH | Avertissement |
| H302 , H351 , H373 , H400 , H410 | |
| P201 , P202 , P260 , P264 , P270 , P273 , P281 , P301 + 312 , P308 + 313 , P314 , P330 , P391 , P405 , P501 | |
| point de rupture | incombustible |
| NIOSH (limites d'exposition pour la santé aux États-Unis) : | |
|
PEL (Autorisé)
|
rien |
|
REL (recommandé)
|
TWA 10 mg/m 3 |
|
IDLH (Danger immédiat)
|
ND |
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 °C [77 °F], 100 kPa). |
|
| Références de l'infobox | |
DCMU ( 3- (3,4-dichlorophényl) -1,1-diméthylurée ) est un algicide et l' herbicide du groupe aryle urée classe qui inhibe la photosynthèse . Il a été introduit par Bayer en 1954 sous le nom commercial de Diuron .
Histoire
En 1952, les chimistes de l' EI du Pont de Nemours and Company ont breveté une série de dérivés d' aryl urée comme herbicides . Plusieurs composés couverts par ce brevet ont été commercialisés comme herbicides : le monuron (4-chlorophényle), le chlortoluron (3-chloro-4-méthylphényle) et le DCMU, l'exemple (3,4-dichlorophényle). Par la suite, plus de trente analogues de l' urée apparentés avec le même mécanisme d'action ont atteint le marché mondial.
Synthèse
Comme cela est décrit dans le brevet du Pont, le matériau de départ est un groupe aryle substitué amine , une aniline , qui est traitée avec du phosgene pour former son isocyanate dérivé. Celui-ci est ensuite mis à réagir avec de la diméthylamine pour donner le produit final.
- Aryl-NH 2 + COCl 2 → Aryl-NCO
- Aryl-NCO + NH(CH 3 ) 2 → Aryl-NHCON(CH 3 ) 2
Mécanisme d'action
DCMU est un inhibiteur très spécifique et sensible de la photosynthèse. Il bloque le site de liaison de la plastoquinone Q B du photosystème II , empêchant le flux d'électrons du photosystème II vers la plastoquinone. Cela interrompt la chaîne de transport d'électrons photosynthétique dans la photosynthèse et réduit ainsi la capacité de la plante à transformer l'énergie lumineuse en énergie chimique ( ATP et potentiel réducteur ).
DCMU ne bloque que le flux d'électrons du photosystème II, il n'a aucun effet sur le photosystème I ou d'autres réactions de la photosynthèse, telles que l'absorption de la lumière ou la fixation du carbone dans le cycle de Calvin .
Cependant, parce qu'elle empêche les électrons produits par l'oxydation de l'eau dans PS II d'entrer dans le pool de plastoquinone, la photosynthèse "linéaire" est effectivement arrêtée, car il n'y a pas d'électrons disponibles pour sortir du cycle de flux d'électrons photosynthétique pour la réduction de NADP + en NADPH. En fait, il a été découvert que la DCMU non seulement n'inhibe pas la voie photosynthétique cyclique , mais, dans certaines circonstances, la stimule réellement.
En raison de ces effets, DCMU est souvent utilisé pour étudier le flux d'énergie dans la photosynthèse .
