Aspartate de magnésium - Magnesium aspartate
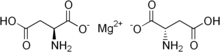 | |
| Donnée clinique | |
|---|---|
| AHFS / Drugs.com | Renseignements sur les médicaments destinés aux consommateurs |
| code ATC | |
| Identifiants | |
| |
| Numero CAS | |
| CID PubChem | |
| UNII | |
| Tableau de bord CompTox ( EPA ) | |
| Carte d'information de l'ECHA |
100.038.806 |
| Données chimiques et physiques | |
| Formule | C 8 H 12 Mg N 2 O 8 |
| Masse molaire | 288,495 g·mol -1 |
|
| |
L'aspartate de magnésium , le sel de magnésium chélaté de l'acide aspartique , est un complément minéral .
Action chimique
Cette forme de supplémentation en magnésium a une biodisponibilité accrue par rapport à l'oxyde et au citrate. Des essais cliniques prometteurs menés dans les années 1960 ont révélé qu'une combinaison d'aspartates de magnésium et de potassium avait un effet positif sur la fatigue et réduisait l'hyperexcitabilité musculaire. Dans son évaluation en 2005, le groupe scientifique AFC a conclu que chez l'homme, la biodisponibilité du magnésium à partir du L-aspartate de magnésium était similaire à celle d'autres sels de magnésium organiques et des sels de magnésium inorganiques plus solubles. Dans l'ensemble, il a été conclu que les sels organiques de magnésium ont la plus grande solubilité dans l'eau et démontrent une plus grande absorption orale et biodisponibilité par rapport aux préparations de magnésium moins solubles telles que l'oxyde de magnésium , l'hydroxyde de magnésium , le carbonate de magnésium et le sulfate de magnésium .
Dosage
| Âge | Homme | Femelle | Grossesse | Lactation |
|---|---|---|---|---|
| De la naissance à 6 mois | 30 mg* | 30 mg* | ||
| 7 à 12 mois | 75 mg* | 75 mg* | ||
| 1-3 ans | 80 mg | 80 mg | ||
| 4 à 8 ans | 130 mg | 130 mg | ||
| 9-13 ans | 240 mg | 240 mg | ||
| 14-18 ans | 410 mg | 360 mg | 400 mg | 360 mg |
| 19-30 ans | 400 mg | 310 mg | 350 mg | 310 mg |
| 31-50 ans | 420 mg | 320 mg | 360 mg | 320 mg |
| 51+ ans | 420 mg | 320 mg |
- Apport adéquat (IA)
Magnésium-L-aspartate 1230 mg (122 mg de magnésium) jusqu'à 3 fois/jour Ajustement posologique en cas d'insuffisance rénale : Les patients atteints d'insuffisance rénale sévère ne doivent pas recevoir de magnésium en raison de la toxicité due à l'accumulation.
Les suppléments de magnésium et autres produits contenant du magnésium, tels que les antiacides, peuvent se lier aux médicaments sur ordonnance, ce qui réduit leur efficacité.
Sécurité
En considérant les sources d'aspartate individuellement, les niveaux d'exposition estimés dans cet avis s'élèvent jusqu'à 6 g/jour pour l'aspartate de calcium (équivalent à 100 mg/kg pc/jour pour un individu de 60 kg), 5,8 g/jour pour l'aspartate de magnésium (équivalent à 97 mg/kg pc/jour), 4 g/jour pour l'aspartate de potassium (équivalent à 67 mg/kg pc/jour), 0,05 g/jour pour l'aspartate de zinc (0,8 mg/kg pc/jour) et 0,008 g/jour pour l'aspartate de cuivre (0,1 mg/kg pc/jour). Ces valeurs sont toutes inférieures à celles rapportées pour induire un déséquilibre des acides aminés dans les essais d'intervention (6,3 g d'aspartate/jour) et elles sont, respectivement, 7, 7,2, 10,5, 875 et 7000 fois inférieures à la NOAEL pour l'aspartate identifiée à partir d'une étude de 90 jours. étude sur le rat. Sur la base de ces marges de sécurité, le groupe scientifique conclut que l'utilisation d'aspartate de zinc et de cuivre, en tant que sources de zinc et de cuivre aux niveaux d'utilisation proposés, ne pose pas de problème de sécurité mais que l'utilisation d'aspartate de calcium, de magnésium et de potassium pourrait problème de sécurité car les marges de sécurité sont considérées comme trop faibles. Le groupe scientifique note que si toutes les sources étaient utilisées simultanément, l'exposition combinée serait de 16 g/jour (équivalant à 267 mg/kg de poids corporel/jour), ce qui est supérieur aux quantités signalées induisant un déséquilibre des acides aminés dans les essais d'intervention (6,3 g/jour ). De plus, cette valeur n'est que 3 fois inférieure à la NOAEL de l'étude sur le rat et, en raison de la faible marge de sécurité, le groupe scientifique considère qu'il s'agit d'un problème de sécurité. Le groupe scientifique estime que l'exposition à l'aspartate provenant de ces compléments alimentaires doit être ajoutée à l'exposition à l'aspartate résultant de l'alimentation.
Sur la base de données américaines, les estimations de l'exposition moyenne à l'acide aspartique provenant de l'alimentation sont de 4,1 g/jour (enfants de 1 à 3 ans) à 9,3 g/jour (hommes de 19 à 30 ans) et au 95e percentile de 6,6 g /jour (enfants 4-8 ans) à 12,9 g/jour (hommes 19-50 ans). Dans ces conditions, les estimations de l'exposition quotidienne maximale aux ions aspartate provenant de l'alimentation (13 g/jour) et des suppléments d'aspartate de calcium ou de magnésium seraient d'environ 19 g/jour6 et de l'aspartate de potassium seraient de 17 g/jour. Les estimations de l'exposition à l'aspartate provenant de la supplémentation en zinc ou en cuivre ne modifieraient pas de manière significative l'exposition à l'aspartate provenant de l'alimentation.
Pris individuellement, ces niveaux d'exposition sont inférieurs à ceux rapportés comme induisant un déséquilibre des acides aminés dans les essais d'intervention, lorsque l'exposition à l'aspartate par l'alimentation est également prise en compte (19,3 g/jour). Cependant, si l'on considère l'apport total potentiel d'ions aspartiques provenant de l'alimentation et d'une combinaison multi-minérale potentielle de tous les compléments alimentaires, l'exposition pourrait atteindre 29 g/jour. Conformément aux préoccupations du SCF, le groupe scientifique considère que l'utilisation d'acides aminés L dans les compléments alimentaires ne devrait pas donner lieu à un déséquilibre nutritionnel des acides aminés. Ainsi, le groupe scientifique conclut que, dans ces conditions, l'exposition aux ions aspartate provenant d'une combinaison multi-minérale de ce type pourrait constituer un problème de sécurité.
