Adsorption de polymère - Polymer adsorption
L'adsorption est l'adhésion d'ions ou de molécules sur la surface d'une autre phase. L'adsorption peut se produire par physisorption et chimisorption . Les ions et les molécules peuvent s'adsorber sur de nombreux types de surfaces, y compris les surfaces polymères. Un polymère est une grosse molécule composée de sous-unités répétitives liées entre elles par des liaisons covalentes . L'adsorption d'ions et de molécules sur les surfaces des polymères joue un rôle dans de nombreuses applications, notamment: biomédicales, structurelles, revêtements, environnementales et pétrolières.
Surfaces polymères ou non polymères
Les surfaces polymères diffèrent des surfaces non polymères en ce que les sous-unités qui composent la surface sont liées de manière covalente les unes aux autres. Les surfaces non polymères peuvent être liées par des liaisons ioniques , des liaisons métalliques ou des forces intermoléculaires (IMF) . Dans un système à deux composants, des surfaces non polymères se forment lorsqu'une quantité nette d'énergie positive est nécessaire pour rompre les auto-interactions et former des non-auto-interactions. Par conséquent, l'énergie de mélange (Δ mix G) est positive. Cette quantité d'énergie, telle que décrite par la tension interfaciale, varie pour différentes combinaisons de matériaux. Cependant, avec des surfaces de polymère, les sous-unités sont liées ensemble de manière covalente et la phase de masse de la surface solide ne permet pas de mesurer directement la tension superficielle. Les forces intermoléculaires entre les grosses molécules de polymère sont difficiles à calculer et ne peuvent pas être déterminées aussi facilement que les interactions moléculaires de surface non polymères. Les sous-unités liées de manière covalente forment une surface avec des propriétés différentes par rapport aux surfaces non polymères. Quelques exemples de surfaces polymères comprennent: le chlorure de polyvinyle (PVC) , le nylon , le polyéthylène (PE) et le polypropylène (PP) . Les surfaces de polymère ont été analysées à l'aide de diverses techniques, notamment: la microscopie électronique à balayage, la microscopie à effet tunnel et la spectroscopie infrarouge.
Isothermes d'adsorption
Le processus d'adsorption peut être caractérisé en déterminant quelle quantité d'ions ou de molécules est adsorbée sur la surface. Cette quantité peut être déterminée expérimentalement par la construction d'un isotherme d'adsorption. Un isotherme d'adsorption est un graphique de Γ (P, T) en fonction de la pression partielle de l'adsorbat (P / P 0 ) pour une température constante donnée, où Γ (P, T) est le nombre de molécules adsorbées par surface. Lorsque la pression partielle de l'adsorbat augmente, le nombre de molécules par zone augmente également.
Angle de contact et tension superficielle
L'angle de contact , l'angle auquel une gouttelette de liquide se rencontre sur une surface solide, est une autre façon de caractériser les surfaces de polymère. L'angle de contact (θ) est une mesure de la capacité de mouillage du liquide sur une surface solide. En général, en raison de la faible énergie de surface, les liquides ne mouillent pas les surfaces de polymère et l'angle de contact sera supérieur à 90 °. Les molécules liquides sont plus attirées par d'autres molécules liquides que la surface du polymère. Parce que les surfaces en polymère sont des surfaces solides, la tension superficielle ne peut pas être mesurée de manière traditionnelle telle que l'utilisation d'une plaque Wilhelmy . Au lieu de cela, les angles de contact peuvent être utilisés pour estimer indirectement la tension superficielle des surfaces de polymère. Ceci est accompli en mesurant les angles de contact d'une série de liquides sur une surface polymère. Un graphique de Fox et Zisman de cos θ en fonction des tensions superficielles des liquides (γ L ) donne une ligne droite qui peut être extrapolée pour déterminer la tension superficielle critique du solide (γ c ).
Où:
- est l'angle de contact
- est la tension superficielle du liquide
- est la tension superficielle critique du solide
La variable β a été précédemment déterminée comme étant d'environ 0,03 à 0,04. Bien que la tension superficielle réelle de la surface du polymère solide ne puisse pas être déterminée, le graphique de Fox et Zisman sert d'estimation. Cependant, cette estimation peut être biaisée s'il existe des forces intermoléculaires significatives entre la surface et le liquide. De plus, ce graphique n'est pas applicable pour les mélanges binaires de liquides déposés sur une surface de polymère. Certaines tensions superficielles estimées de différents polymères et les angles de contact de différents liquides sur des surfaces de polymère sont indiqués ci-dessous.
Polymère γ c (mN / m) Polystyrène (PS) 40,7 Polyvinylacétate (PVA) 36,5 Téflon 20 Acide polyméthylacrylique (PMAA) 41 Polypropylène 33 Silicone 24 Polyimide 40 Nylon 6/6 41 Polyacrylamide 56
Adsorption et relation de charge

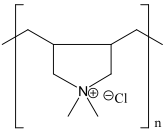
Différentes surfaces de polymère ont des chaînes latérales différentes sur leurs monomères qui peuvent se charger en raison de l'adsorption ou de la dissociation des adsorbats. Par exemple, le polystyrène sulfonate a des monomères contenant des chaînes latérales chargées négativement qui peuvent adsorber des adsorbats chargés positivement. Le polystyrène sulfonate adsorbera plus d'adsorbat chargé positivement que chargé négativement. Inversement, pour un polymère qui contient des chaînes latérales chargées positivement, comme le poly (chlorure de diallyldiméthylammonium) , les adsorbats chargés négativement seront fortement attirés.
Thermodynamique des surfaces polymères
Angle de contact
Parce que la capacité d'une surface à adsorber des molécules sur sa surface dépend des énergies d'interaction, la thermodynamique de l'adsorption peut être utilisée pour comprendre les forces motrices de l'adsorption. Pour mesurer la thermodynamique des surfaces polymères, les angles de contact sont souvent utilisés pour obtenir facilement des informations utiles. La description thermodynamique des angles de contact d'une goutte de liquide sur une surface solide est dérivée de l'équilibre formé entre les potentiels chimiques des interfaces solide-liquide, solide-vapeur et liquide-vapeur.
À l'équilibre, l'angle de contact d'une goutte de liquide sur une surface ne change pas. Par conséquent, l'énergie libre de Gibbs est égale à 0:
Les potentiels chimiques des trois interfaces doivent s'annuler, produisant l'équation de Young pour la relation entre les énergies de surface et les angles de contact:
où:
- est la tension superficielle du liquide
- est l'angle de contact du liquide
- est la tension superficielle de l'interface solide-vapeur
- est la tension superficielle de l'interface solide-liquide
- est la pression de vapeur du liquide à l'équilibre.
Cependant, cette équation ne peut pas être utilisée pour déterminer l' énergie de surface d'une surface solide par elle-même. Il peut être utilisé conjointement avec l'équation suivante pour déterminer la relation entre l'angle de contact et l'énergie de surface du solide, en tant que tension superficielle énergie de surface pour un solide:
où
- est l'énergie de surface du solide
- est la tension superficielle du liquide.
- et sont les composantes dispersives et polaires de l'énergie de surface du solide
En utilisant ces deux équations, l'énergie de surface d'un solide peut être déterminée simplement en mesurant l'angle de contact de deux liquides différents de tension superficielle connue sur la surface de ce solide.
Copolymères
Pour les surfaces hétérogènes (constituées de deux ou plusieurs types de matériaux différents), l'angle de contact d'une goutte de liquide en chaque point le long de la ligne de contact triphasée avec une surface solide est le résultat de la tension superficielle de la surface à ce point. Par exemple, si les régions hétérogènes de la surface forment de très grands domaines, et que la goutte existe entièrement dans un domaine homogène, alors elle aura un angle de contact correspondant à la tension superficielle de cette région homogène.
De même, une goutte qui chevauche deux domaines de tensions de surface différentes aura des angles de contact différents le long de la ligne de contact triphasée correspondant aux différentes tensions de surface en chaque point.
Cependant, avec des domaines suffisamment petits (comme dans ceux d'un copolymère bloc), l'énergie de surface observée de la surface se rapproche de la moyenne pondérée des énergies de surface de chacun des constituants de la surface:
où:
- est l'énergie de surface globale du polymère
- est la fraction du i ème composant de la surface du polymère
- est l'énergie de surface du i ème composant
Cela se produit parce que lorsque la taille des domaines homogènes devient très petite par rapport à la taille de la goutte, les différences d'angles de contact le long de différentes régions homogènes deviennent indiscernables de la moyenne des angles de contact.
L'angle de contact observé est donné par la formule suivante:
où:
- est la fraction du i ème composant
- est l'angle de contact i ème composante
Si le polymère est constitué de seulement deux monomères différents, il est possible d'utiliser l'équation ci-dessus pour déterminer la composition du polymère simplement en mesurant l'angle de contact d'une goutte de liquide placée dessus:
où:
- est l'angle de contact observé
- f est la fraction de surface d'un composant et la fraction de surface de l'autre.
- et sont les angles de contact des premier et second composants du polymère.
Couverture de surface
L'une des caractéristiques déterminantes des surfaces et des revêtements en polymère est la régularité chimique de la surface. Alors que de nombreux matériaux peuvent être des mélanges irréguliers de différents composants, les surfaces de polymère ont tendance à être chimiquement uniformes, avec la même distribution de différents groupes fonctionnels sur toutes les zones de la surface. Pour cette raison, l'adsorption de molécules sur des surfaces de polymère peut être facilement modélisée par les isothermes de Langmuir ou Frumkin. L'équation de Langmuir indique que pour l'adsorption d'une molécule d'adsorbat A sur un site de liaison de surface S , un seul site de liaison est utilisé, et chaque site de liaison libre est également susceptible d'accepter une molécule d'adsorbat:
où:
- A est l'adsorbat
- S est le site de liaison de surface
- est la paire adsorbat / site de liaison lié
La constante d'équilibre de cette réaction est alors définie comme:
La constante d'équilibre est liée à la couverture de surface d'équilibre θ , qui est donnée par:
où:
- ' θ est la couverture de surface (fraction, 0 est vide, 1 est entièrement couverte)
- est la constante d'équilibre d'adsorption
Énergie d'adsorption
Du fait que de nombreux polymères sont composés principalement de chaînes hydrocarbonées avec au plus des groupes fonctionnels légèrement polaires, ils ont tendance à avoir de faibles énergies de surface et donc à adsorber assez mal. Bien que cela puisse être avantageux pour certaines applications, la modification des surfaces de polymère est cruciale pour de nombreuses autres applications dans lesquelles l'adhérence d'un substrat à sa surface est vitale pour des performances optimales. Par exemple, de nombreuses applications utilisent des polymères comme composants structurels, mais qui se dégradent rapidement lorsqu'ils sont exposés aux intempéries ou à d'autres sources d'usure. Par conséquent, des revêtements doivent être utilisés pour protéger la couche structurelle contre les dommages. Cependant, les mauvaises propriétés adhésives des polymères non polaires rendent difficile l'adsorption du revêtement protecteur sur sa surface. Ces types de problèmes rendent la mesure et le contrôle des énergies de surface importants pour le développement de technologies utiles.
L'énergie d'adsorption de Gibbs,, peut être déterminée à partir de la constante d'équilibre d'adsorption:
Parce qu'il est négatif pour un processus spontané et positif pour un processus non spontané, il peut être utilisé pour comprendre la tendance des différents composés à s'adsorber sur une surface. De plus, il peut être divisé en une combinaison de deux composants:
qui sont les énergies de Gibbs de physisorption et de chimisorption , respectivement. De nombreuses applications de polymères, telles que celles qui utilisent du polytétrafluoroéthylène (PTFE ou Téflon) nécessitent l'utilisation d'une surface avec des propriétés de physisorption spécifiques vis-à-vis d'un type de matériau, tout en étant fermement adhérée en place à un type de matériau différent. Parce que l'énergie de physisorption est si faible pour ces types de matériaux, la chimisorption est utilisée pour former des liaisons covalentes entre le revêtement polymère et la surface de l'objet (comme une casserole) qui le maintient en place. Parce que les amplitudes relatives des processus de chimisorption sont généralement beaucoup plus importantes que les amplitudes des processus de physisorption, cela forme un lien fort entre le polymère et la surface à laquelle il adhère chimiquement, tout en permettant au polymère de conserver ses caractéristiques de physisorption vis-à-vis d'autres matériaux.
Expérimentalement, l'enthalpie et l'entropie d'adsorption sont souvent utilisées pour affiner les propriétés d'adsorption d'un matériau. L'enthalpie d'adsorption peut être déterminée à partir de la calorimétrie à pression constante:
où:
- est la chaleur échangée,
- est l'enthalpie molaire intégrale d'adsorption,
- est le nombre de moles adsorbées.
À partir de l'enthalpie d'adsorption, l'entropie d'adsorption peut être calculée:
où:
- est l'entropie molaire intégrale de l'adsorption,
- est la température en Kelvins .
Ensemble, ils sont utilisés pour comprendre les forces motrices des processus d'adsorption.
Applications
Revêtements d'implants
Revêtements résistants aux protéines
L'adsorption des protéines influence les interactions qui se produisent à l'interface tissu-implant. L'adsorption de protéines peut entraîner des caillots sanguins, la réponse d'un corps étranger et finalement la dégradation du dispositif. Afin de contrer les effets de l'adsorption des protéines, les implants sont souvent recouverts d'un revêtement polymère pour diminuer l'adsorption des protéines.
Il a été démontré que les revêtements en polyéthylène glycol (PEG) minimisent l'adsorption des protéines dans le corps. Le revêtement PEG est constitué de molécules hydrophiles qui répugnent à l'adsorption des protéines. Les protéines sont constituées de molécules hydrophobes et de sites de charge qui veulent se lier à d'autres molécules hydrophobes et à des sites de charge opposée. En appliquant une fine couche monocouche de PEG, l'adsorption des protéines est empêchée sur le site du dispositif. De plus, la résistance du dispositif à l'adsorption des protéines, à l'adhésion des fibroblastes et à l'adhésion des bactéries est augmentée.
Revêtements antithrombogènes
L'hémocompatibilité d'un dispositif médical dépend de la charge de surface, de l'énergie et de la topographie. Les dispositifs qui ne sont pas hémocompatibles courent le risque de former un thrombus, de proliférer et de compromettre le système immunitaire. Des revêtements polymères sont appliqués sur des dispositifs pour augmenter leur hémocompatibilité. Les cascades chimiques conduisent à la formation de caillots fibreux. En choisissant d'utiliser des revêtements polymères hydrophiles, l'adsorption des protéines diminue et le risque d'interactions négatives avec le sang diminue également. Un tel revêtement polymère qui augmente l'hémocompatibilité est l' héparine . L'héparine est un revêtement polymère qui interagit avec la thrombine pour empêcher la coagulation. Il a été démontré que l'héparine supprime l'adhésion plaquettaire, l'activation du complément et l'adsorption des protéines.
De construction
Composites polymères avancés
Les composites polymères avancés sont utilisés dans le renforcement et la réhabilitation d'anciennes structures. Ces composites avancés peuvent être fabriqués à l'aide de nombreuses méthodes différentes, notamment le préimprégné, la résine , l' infusion , l' enroulement de filament et la pultrusion . Les composites polymères avancés sont utilisés dans de nombreuses structures d'avion et leur plus grand marché est l'aérospatiale et la défense.
Polymères renforcés de fibres
Les polymères renforcés de fibres (PRF) sont couramment utilisés par les ingénieurs civils dans leurs structures. Les PRF répondent de manière linéaire-élastiquement aux contraintes axiales , ce qui en fait un excellent matériau pour supporter une charge. Les FRP sont généralement sous forme de stratifié , chaque lamelle ayant des fibres unidirectionnelles, typiquement du carbone ou du verre, noyées dans une couche de matériau de matrice polymère léger. Les PRF ont une grande résistance à l'exposition environnementale et une grande durabilité.
Polytétrafluoroéthylène
Le polytétrafluoroéthylène (PTFE) est un polymère utilisé dans de nombreuses applications, notamment les revêtements antiadhésifs, les produits de beauté et les lubrifiants. Le PTFE est une molécule hydrophobe composée de carbone et de fluor. Les liaisons carbone-fluor font que le PTFE est un matériau à faible frottement, propice aux environnements à haute température et résistant à la fissuration sous contrainte. Ces propriétés font que le PTFE n'est pas réactif et est utilisé dans un large éventail d'applications.
































![{\ displaystyle k_ {ad} = {\ frac {[AS]} {[A] [B]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/941d463dab97c11b33a6c444e10c3f3150ca659a)
![\ theta \ = \ frac {k_ {ad} [A]} {k_ {ad} [A] + 1}](https://wikimedia.org/api/rest_v1/media/math/render/svg/bc25aba277a64bf3e2c03b50f90cd0e0c35edbf2)










