Rifamycine - Rifamycin
 | |
 | |
| Donnée clinique | |
|---|---|
| Appellations commerciales | Aemcolo |
| AHFS / Drugs.com | Monographie |
| MedlinePlus | a619010 |
| Données de licence | |
| Voies d' administration |
Par la bouche |
| code ATC | |
| Statut légal | |
| Statut légal | |
| Identifiants | |
| Numero CAS | |
| CID PubChem | |
| Banque de médicaments | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| Données chimiques et physiques | |
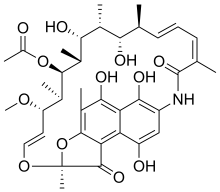
| Formule | C 37 H 47 N O 12 |
| Masse molaire | 697,778 g·mol -1 |
| Modèle 3D ( JSmol ) | |
| |
| |
Les rifamycines sont un groupe d' antibiotiques qui sont synthétisés soit naturellement par la bactérie Amycolatopsis rifamycinica, soit artificiellement. Ils sont une sous-classe de la grande famille des ansamycines . Les rifamycines sont particulièrement efficaces contre les mycobactéries et sont donc utilisées pour traiter les infections de la tuberculose , de la lèpre et du complexe mycobacterium avium (MAC).
Le groupe rifamycine comprend les médicaments "classiques" à base de rifamycine ainsi que les dérivés de la rifamycine rifampicine (ou rifampicine), rifabutine , rifapentine , rifalazil et rifaximine . La rifamycine, vendue sous le nom commercial Aemcolo, est approuvée aux États-Unis pour le traitement de la diarrhée du voyageur dans certaines circonstances.
Bactérie
Streptomyces mediterranei a été isolé pour la première fois en 1957 à partir d'un échantillon de sol collecté près de la ville balnéaire de St Raphael dans le sud de la France. Le nom a été donné à l'origine par deux microbiologistes travaillant avec la société pharmaceutique italienne Group Lepetit SpA à Milan , l'italienne Grazia Beretta et Pinhas Margalith d'Israël.
En 1969, la bactérie a été renommée Nocardia mediterranei lorsqu'un autre scientifique nommé Thiemann a découvert qu'elle possédait une paroi cellulaire typique de l'espèce Nocardia. Puis, en 1986, la bactérie a été rebaptisée Amycolatopsis mediterranei , en tant que première espèce d'un nouveau genre, car un scientifique nommé Lechevalier a découvert que la paroi cellulaire manque d'acide mycolique et ne peut pas être infectée par les phages Nocardia et Rhodococcus. Sur la base de séquences d'ARN ribosomique 16S , Bala et al. rebaptisé l'espèce en 2004 Amycolatopsis rifamycinica .
Premiers médicaments
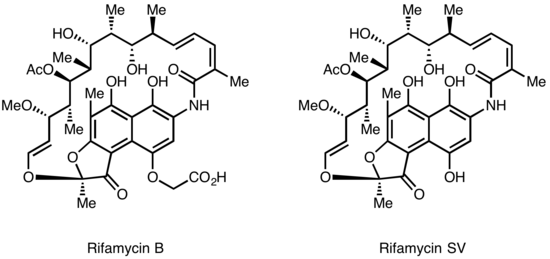
Les rifamycines ont été isolées pour la première fois en 1957 à partir d'une culture de fermentation de Streptomyces mediterranei au laboratoire de Gruppo Lepetit SpA à Milan par deux scientifiques nommés Piero Sensi et Maria Teresa Timbal, en collaboration avec le scientifique israélien Pinhas Margalith. Initialement, une famille d'antibiotiques étroitement apparentés a été découverte sous le nom de Rifamycine A, B, C, D, E. Le seul composant de ce mélange suffisamment stable pour être isolé sous une forme pure était la Rifamycine B, qui était malheureusement peu active. Cependant, d'autres études ont montré que si la rifamycine B était essentiellement inactive, elle était spontanément oxydée et hydrolysée dans des solutions aqueuses pour donner la rifamycine S hautement active. Une simple réduction de la rifamycine S a donné la forme hydroquinone appelée rifamycine SV, qui est devenue le premier membre de ce classe pour entrer dans l'utilisation clinique comme antibiotique intraveineux. Une modification chimique supplémentaire de la rifamycine SV a donné un analogue amélioré, le rifamide, qui a également été introduit dans la pratique clinique, mais qui était également limité à une utilisation intraveineuse. Après un vaste programme de modification, la Rifampine a finalement été produite, qui est disponible par voie orale et est devenue un pilier du traitement de la tuberculose.
Lepetit a déposé une demande de protection par brevet de la rifamycine B au Royaume-Uni en août 1958 et aux États-Unis en mars 1959. Le brevet britannique GB921045 a été accordé en mars 1963 et le brevet américain 3 150 046 a été accordé en septembre 1964. Le médicament est largement considéré comme ayant aidé à vaincre le problème de la tuberculose pharmacorésistante dans les années 1960.
Essais cliniques
Les rifamycines ont été utilisées pour le traitement de nombreuses maladies, la plus importante étant la tuberculose liée au VIH. Une revue systématique des essais cliniques sur des schémas thérapeutiques alternatifs pour la prévention de la tuberculose active chez les individus séronégatifs atteints de TB latente a révélé qu'un schéma thérapeutique hebdomadaire, directement observé de rifapentine avec de l' isoniazide pendant trois mois était aussi efficace qu'un schéma posologique quotidien auto-administré d'isoniazide. pendant neuf mois. Mais le régime rifapentine-isoniazide avait des taux d'achèvement du traitement plus élevés et des taux d' hépatotoxicité plus faibles . Cependant, le taux d'événements indésirables limitant le traitement était plus élevé dans le schéma rifapentine-isoniazide.
Les rifamycines ont un mécanisme d'action unique, inhibant sélectivement l' ARN polymérase ADN-dépendante bactérienne , et ne présentent aucune résistance croisée avec d'autres antibiotiques en usage clinique. Cependant, malgré leur activité contre les bactéries résistantes aux autres antibiotiques , les rifamycines elles-mêmes souffrent d'une fréquence de résistance assez élevée. Pour cette raison, la rifampicine et d'autres rifamycines sont généralement utilisées en association avec d'autres médicaments antibactériens. Ceci est pratiqué de manière routinière dans le traitement de la tuberculose et sert à empêcher la formation de mutants résistants à l'un des médicaments de la combinaison. La rifampine tue rapidement les souches de bacilles à division rapide ainsi que les cellules « persistantes », qui restent biologiquement inactives pendant de longues périodes leur permettant d'échapper à l'activité antibiotique. De plus, la rifabutine et la rifapentine ont toutes deux été utilisées contre la tuberculose acquise chez les patients séropositifs. Bien que le traitement de la tuberculose reste l'utilisation la plus importante de la rifampicine, un problème croissant d'infections bactériennes multirésistantes graves a conduit à l'utilisation d'associations d'antibiotiques contenant de la rifampicine pour les traiter.
Mécanisme d'action
L'activité antibactérienne des rifamycines repose sur l'inhibition de la synthèse d'ARN dépendante de l'ADN bactérien. Ceci est dû à la forte affinité des rifamycines pour l' ARN polymérase procaryote . La sélectivité des rifamycines dépend du fait qu'elles ont une très faible affinité pour l'enzyme analogue de mammifère. Les données de structure cristalline de l'antibiotique lié à l'ARN polymérase indiquent que la rifamycine bloque la synthèse en provoquant de forts conflits stériques avec l'oligonucléotide en croissance (mécanisme d'« occlusion stérique »). Si la rifamycine se lie à la polymérase après le démarrage du processus d'extension de chaîne, aucune inhibition n'est observée sur la biosynthèse, ce qui correspond à un mécanisme d'occlusion stérique. Une résistance élevée de niveau unique aux rifamycines se produit à la suite d'un seul changement d'acide aminé dans l'ARN polymérase dépendante de l'ADN bactérien.
Biosynthèse
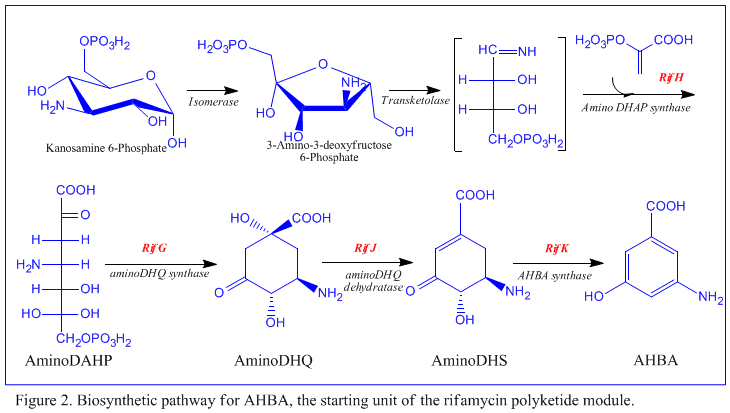
Les premières informations sur la biosynthèse des rifamycines sont venues d'études utilisant l'isotope stable Carbon-13 et la spectroscopie RMN pour établir l'origine du squelette carboné. Ces études ont montré que la chaîne ansa était dérivée de l' acétate et du propionate , en commun avec d'autres antibiotiques polycétides . Il a été montré que le chromophore naphtalénique dérive d'une unité propionate couplée à une fraction amino à sept atomes de carbone d'origine inconnue. Le schéma général de la biosynthèse commence par l'unité de départ peu courante, l'acide 3-amino-5-hydroxybenzoïque ( AHBA ), via la voie des polycétides de type I ( PKS I ) dans laquelle l'extension de chaîne est réalisée à l'aide de 2 unités acétate et 8 unités propionate. On pense que l'AHBA provient de la voie Shikimate , mais cela n'a pas été incorporé dans le mécanisme de biosynthèse. Ceci est dû à l'observation que 3 analogues d'acides aminés se sont convertis en AHBA dans des extraits acellulaires d' A . mediterranei .
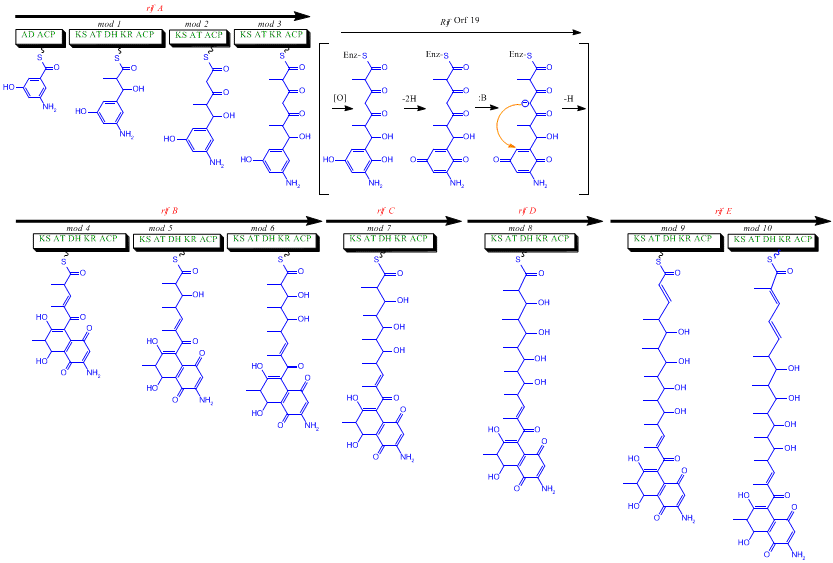
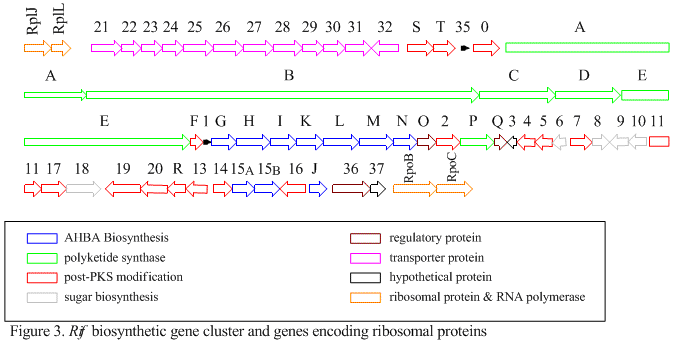
Le cluster rif est responsable de la biosynthèse des rifamycines. Il contient les gènes rifG à rifN , qui se sont avérés biosynthétiser l'AHBA.[10] On pense que RifK , rifL , rifM et rifN agissent comme des transaminases afin de former le précurseur de l'AHBA, la kanosamine. "RifH" code pour l'aminoDAHP synthase qui catalyse la condensation entre le 1-désoxy-1-imino-d-érythrose 4-phosphate et le phosphoénolpyruvate . RifA à rifE codent pour un module de polykétide synthase de type I, le module de chargement étant une peptide synthétase non ribosomique . Dans l'ensemble, rifA-E assemble un undecaketide linéaire et est suivi par rifF , qui code pour une amide synthase et provoque la libération de l'undecaketide et la formation d'une structure macrolactame. De plus, le cluster rif contient diverses protéines régulatrices et gènes de glycosylation qui semblent être silencieux. D'autres types de gènes semblent effectuer des modifications post-synthase du polykétide d'origine.
Dérivés
Lepetit a introduit la rifampicine, une rifamycine active par voie orale, vers 1966. La rifabutine, un dérivé de la rifamycine S, a été inventée vers 1975 et est arrivée sur le marché américain en 1993. Hoechst Marion Roussel (qui fait maintenant partie d' Aventis ) a introduit la rifapentine en 1999.
La rifaximine est une rifamycine orale commercialisée aux États-Unis par Salix Pharmaceuticals qui est mal absorbée par l'intestin. Il a été utilisé pour traiter l'encéphalopathie hépatique et la diarrhée du voyageur .
Rifamycines actuellement disponibles
- Rifampicine ou Rifampine
- Rifabutine
- Rifapentine
- Rifaximine
Les références
Bibliographie
- Sensi. et al. , Farmaco éd. Sci. (1959) 14, 146-147 - l'article annonçant la découverte des rifamycines.
- Thieman et al. Cambre. Microbiole. (1969), 67 147-151 - l'article qui a renommé Streptomyces mediterranei en Nocardia mediterranei .
- Lechevalier et al. , Int. J. Syst. Bactériol. (1986), 36, 29) - l'article qui a renommé Nocardia mediterranei en Amycolatopsis mediterranei .
- Bala S (2004). "Reclassement de "Amycolatopsis mediterranei" DSM 46095 en "Amycolatopsis rifamycinica" sp. nov" . Journal international de microbiologie systématique et évolutive . 54 (4) : 1145-1149. doi : 10.1099/ijs.0.02901-0 . PMID 15280283 . - le papier avec le dernier changement de nom
Liens externes
- "Rifamycine" . Portail d'information sur les médicaments . Bibliothèque nationale de médecine des États-Unis.