Tétrafluoroborate de triéthyloxonium - Triethyloxonium tetrafluoroborate
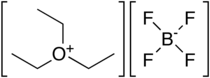
|
|
|
|
| Noms | |
|---|---|
|
Nom IUPAC
Tétrafluoroborate de triéthyloxonium
|
|
| Identifiants | |
|
Modèle 3D ( JSmol )
|
|
| 3598090 | |
| ChemSpider | |
| Carte d'information de l'ECHA |
100.006.096 |
|
CID PubChem
|
|
| UNII | |
| Numéro ONU | 3261 |
|
Tableau de bord CompTox ( EPA )
|
|
|
|
|
|
| Propriétés | |
| C 6 H 15 B F 4 O | |
| Masse molaire | 189,99 g·mol -1 |
| Point de fusion | 91 à 92 °C (196 à 198 °F ; 364 à 365 K) |
| Réagit | |
| Dangers | |
|
Classification UE (DSD) (obsolète)
|
|
| Phrases R (obsolètes) | R14 , R34 |
| Phrases S (obsolètes) | S22 , S26 , S36/37/39 |
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Références de l'infobox | |
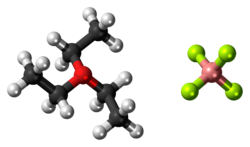
Le tétrafluoroborate de triéthyloxonium est le composé organique d' oxonium de formule [(CH 3 CH 2 ) 3 O]BF 4 . Il est souvent appelé réactif de Meerwein ou sel de Meerwein d' après son découvreur Hans Meerwein . Le tétrafluoroborate de triméthyloxonium apparenté est également bien connu et disponible dans le commerce . Les composés sont des solides blancs qui se dissolvent dans des solvants organiques polaires. Ce sont des agents alkylants puissants . A part le BF−
4 sel, de nombreux dérivés apparentés sont disponibles.
Synthèse et réactivité
Le tétrafluoroborate de triéthyloxonium est préparé à partir de trifluorure de bore , d' éther diéthylique et d' épichlorhydrine :
- 4 Et 2 O·BF 3 + 2 Et 2 O + 3 C 2 H 3 (O)CH 2 Cl → 3 Et 3 O + BF−
4+ B[(OCH(CH 2 Cl)CH 2 OEt] 3
Le sel de triméthyloxonium est disponible à partir de l'éther diméthylique par une voie analogue. Ces sels n'ont pas une longue durée de conservation à température ambiante. Ils se dégradent par hydrolyse :
- [(CH 3 CH 2 ) 3 O] + BF−
4+ H 2 O → (CH 3 CH 2 ) 2 O + CH 3 CH 2 OH + HBF 4
La propension des sels de trialkyloxonium à l'échange d'alkyle peut être avantageuse. Par exemple, le tétrafluoroborate de triméthyloxonium, qui réagit lentement en raison de sa faible solubilité dans la plupart des solvants compatibles, peut être converti in situ en alkyle supérieur/oxoniums plus solubles, accélérant ainsi les réactions d'alkylation.
Structure
La structure du tétrafluoroborate de triéthyloxonium n'a pas été caractérisée par cristallographie aux rayons X , mais la structure de l' hexafluorophosphate de triéthyloxonium a été examinée. Les mesures confirment que le cation est pyramidal avec des angles COC compris entre 109,4° et 115,5°. La distance C–O moyenne est de 1,49 Å.
Sécurité
Le tétrafluoroborate de triéthyloxonium est un agent alkylant puissant, bien que les risques soient réduits car il n'est pas volatil. Il libère un acide fort au contact de l'eau. Les propriétés du dérivé méthyle sont similaires.
Les références
- ^ H. Meerwein; G. Hinz ; P. Hofmann ; E. Kroning & E. Pfeil (1937). "Über Tertiäre Oxoniumsalze, I". Journal für Praktische Chemie . 147 (10-12) : 257. doi : 10.1002/prac.19371471001 .
- ^ H. Meerwein; E. Bettenberg ; H. Or ; E. Pfeil & G. Willfang (1940). "Über Tertiäre Oxoniumsalze, II". Journal für Praktische Chemie . 154 (3–5) : 83. doi : 10.1002/prac.19391540305 .
- ^ Hartwig Prest, Dave G. Seapy "Triethyloxonium Tetrafluoroborate" dans Encyclopédie des réactifs pour la synthèse organique John Wiley & Sons, New York, 2008. doi : 10.1002/047084289X.rt223.pub2 . Date de mise en ligne de l'article : 14 mars 2008
- ^ H. Meerwein (1973). "Fluoroborate de triéthyloxonium" . Synthèses organiques .; Volume collectif , 5 , p. 1080
- ^ TJ Curphey (1988). "Tétrafluoroborate de triméthyloxonium" . Synthèses organiques .; Volume collectif , 6 , p. 1019
- ^ Vartak AP & Crooks PA (2009). « Une synthèse énantiosélective évolutive de l'agoniste alpha2-adrénergique, Lofexidine ». Org. Processus Rés. Dév. 13 (3) : 415-419. doi : 10.1021/op8002689 .
- ^ Watkins, Michael I.; IP, Wai Man; Olah, George A.; Bau, Robert (1982). « Structure des ions oxonium : une étude cristallographique aux rayons X de l'hexafluorophosphate de triéthyloxonium et du tétraphénylborate de triphényloxonium ». Journal de l'American Chemical Society . 104 (9) : 2365–2372. doi : 10.1021/ja00373a006 .
