11β-hydroxystéroïde déshydrogénase de type 1 - 11β-Hydroxysteroid dehydrogenase type 1
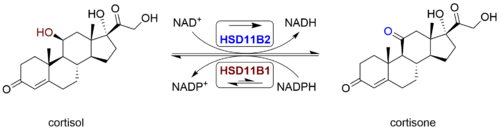
La 11β-hydroxystéroïde déshydrogénase de type 1 , également connue sous le nom de cortisone réductase , est une enzyme dépendante du NADPH fortement exprimée dans les principaux tissus métaboliques, notamment le foie , le tissu adipeux et le système nerveux central . Dans ces tissus, HSD11B1 réduit la cortisone en l'hormone active cortisol qui active les récepteurs des glucocorticoïdes . Elle appartient à la famille des déshydrogénases à chaîne courte .
Une fonction
La protéine codée par ce gène est une enzyme microsomale qui catalyse la conversion de l'hormone du stress cortisol en métabolite inactif cortisone . De plus, la protéine codée peut catalyser la réaction inverse, la conversion de la cortisone en cortisol. Trop de cortisol peut entraîner une obésité centrale , et une variation particulière de ce gène a été associée à l'obésité et à la résistance à l' insuline chez les enfants. Deux variants de transcription codant pour la même protéine ont été trouvés pour ce gène.
Signification clinique
La 11β-HSD1 est inhibée par la carbénoxolone , un médicament généralement utilisé dans le traitement des ulcères gastroduodénaux . De plus, l'acide 18alpha- glycyrrhizique de la racine de glycyrrhiza glabra a été découvert comme inhibiteur.
Le salicylate régule négativement l'expression de la 11β-HSD1 dans le tissu adipeux chez les souris obèses et peut donc expliquer pourquoi l'aspirine améliore le contrôle glycémique dans le diabète de type 2. Le gallate d' épigallocatéchine du thé vert peut également inhiber puissamment cette enzyme; Le thé vert est un mélange complexe de divers composés phénoliques dont le contenu varie selon la production et la transformation, et certains des composés phénoliques sont des inhibiteurs connus de HDAC qui modifient l'expression génétique. L'EGCG tel qu'il est habituellement consommé dans le thé vert est mal absorbé dans la circulation sanguine. Des recherches supplémentaires sont nécessaires pour parvenir à des conclusions définitives.
Voir également
Les références
Liens externes
- Emplacement du génome humain HSD11B1 et page de détails du gène HSD11B1 dans le navigateur de génome de l' UCSC .
Lectures complémentaires
- White PC, Mune T, Agarwal AK (février 1997). "11 bêta-hydroxystéroïde déshydrogénase et syndrome d'excès apparent de minéralocorticoïde". Examens endocriniens . 18 (1) : 135-56. doi : 10.1210/er.18.1.135 . PMID 9034789 .
- Agarwal AK (novembre 2003). « Métabolisme du cortisol et obésité viscérale : rôle de l'enzyme 11bêta-hydroxystéroïde déshydrogénase de type I et du cofacteur réduit NADPH ». Recherche endocrinienne . 29 (4) : 411-8. doi : 10.1081/ERC-120026947 . PMID 14682470 . S2CID 32163545 .
- Tomlinson JW, Walker EA, Bujalska IJ, Draper N, Lavery GG, Cooper MS, Hewison M, Stewart PM (octobre 2004). « 11beta-hydroxystéroïde déshydrogénase de type 1 : un régulateur tissu-spécifique de la réponse aux glucocorticoïdes » . Examens endocriniens . 25 (5) : 831–66. doi : 10.1210/er.2003-0031 . PMID 15466942 .
- Wake DJ, Walker BR (février 2006). « Inhibition de la 11beta-hydroxystéroïde déshydrogénase de type 1 dans l'obésité ». Endocrinien . 29 (1) : 101-8. doi : 10.1385/ENDO:29:1:101 . PMID 16622297 . S2CID 8906021 .
- Tannin GM, Agarwal AK, Monder C, New MI, White PC (septembre 1991). "Le gène humain de la 11 bêta-hydroxystéroïde déshydrogénase. Structure, distribution tissulaire et localisation chromosomique" . Le Journal de Chimie Biologique . 266 (25) : 16653-8. doi : 10.1016/S0021-9258 (18) 55351-5 . PMID 1885595 .
- Graham DL, Oram JF (juin 1987). "Identification et caractérisation d'une protéine de liaison aux lipoprotéines de haute densité dans les membranes cellulaires par transfert de ligand" . Le Journal de Chimie Biologique . 262 (16) : 7439-42. doi : 10.1016/S0021-9258 (18) 47584-9 . PMID 3034894 .
- Whorwood CB, Mason JI, Ricketts ML, Howie AJ, Stewart PM (avril 1995). « Détection des isoformes de la déshydrogénase bêta-hydroxystéroïde 11 humaine à l'aide de la réaction en chaîne de la transcriptase inverse-polymérase et localisation de l'isoforme de type 2 dans les canaux collecteurs rénaux ». Endocrinologie moléculaire et cellulaire . 110 (1–2) : R7–12. doi : 10.1016/0303-7207(95)03546-J . PMID 7545619 . S2CID 25070635 .
- Mune T, Rogerson FM, Nikkilä H, Agarwal AK, White PC (août 1995). « L'hypertension humaine causée par des mutations dans l'isoenzyme rénale de la 11 bêta-hydroxystéroïde déshydrogénase ». Génétique de la nature . 10 (4) : 394-9. doi : 10.1038/ng0895-394 . PMID 7670488 . S2CID 30848352 .
- Ricketts ML, Verhaeg JM, Bujalska I, Howie AJ, Rainey WE, Stewart PM (avril 1998). « Localisation immunohistochimique de type 1 11beta-hydroxystéroïde déshydrogénase dans les tissus humains ». Le Journal d'endocrinologie clinique et du métabolisme . 83 (4) : 1325-1335. doi : 10.1210/jc.83.4.1325 . PMID 9543163 .
- Calvo D, Gómez-Coronado D, Suárez Y, Lasunción MA, Vega MA (avril 1998). "Le CD36 humain est un récepteur de haute affinité pour les lipoprotéines natives HDL, LDL et VLDL" . Journal de recherche sur les lipides . 39 (4) : 777-88. doi : 10.1016/S0022-2275(20)32566-9 . PMID 9555943 .
- Odermatt A, Arnold P, Stauffer A, Frey BM, Frey FJ (octobre 1999). "Les séquences d'ancrage N-terminales des déshydrogénases 11bêta-hydroxystéroïdes déterminent leur orientation dans la membrane du réticulum endoplasmique" . Le Journal de Chimie Biologique . 274 (40) : 28762-70. doi : 10.1074/jbc.274.40.28762 . PMID 10497248 .
- Sriskanda V, Schwer B, Ho CK, Shuman S (octobre 1999). "L'analyse mutationnelle de l'ADN ligase d'Escherichia coli identifie les acides aminés requis pour la nick-ligation in vitro et pour la complémentation in vivo de la croissance des cellules de levure supprimées pour CDC9 et LIG4" . Recherche sur les acides nucléiques . 27 (20) : 3953-63. doi : 10.1093/nar/27.20.3953 . PMC 148661 . PMID 10497258 .
- Schutte BC, Bjork BC, Coppage KB, Malik MI, Gregory SG, Scott DJ, Brentzell LM, Watanabe Y, Dixon MJ, Murray JC (janvier 2000). "Une carte génétique préliminaire pour la région critique du syndrome de Van der Woude dérivée de 900 kb de séquence génomique à 1q32-q41" . Recherche sur le génome . 10 (1) : 81-94. doi : 10.1101/gr.10.1.81 (inactif le 31 mai 2021). PMC 310500 . PMID 10645953 .Maint CS1: DOI inactif à partir de mai 2021 ( lien )
- Cooper MS, Walker EA, Bland R, Fraser WD, Hewison M, Stewart PM (septembre 2000). « Expression et conséquences fonctionnelles de l'activité 11beta-hydroxystéroïde déshydrogénase dans l'os humain ». Os . 27 (3) : 375-81. doi : 10.1016/S8756-3282(00)00344-6 . PMID 10962348 .
- Reddy ST, Wadleigh DJ, Grijalva V, Ng C, Hama S, Gangopadhyay A, Shih DM, Lusis AJ, Navab M, Fogelman AM (avril 2001). "La paraoxonase-3 humaine est une enzyme associée aux HDL avec une activité biologique similaire à la protéine paraoxonase-1 mais n'est pas régulée par les lipides oxydés" . Artériosclérose, thrombose et biologie vasculaire . 21 (4) : 542-7. doi : 10.1161/01.ATV.21.4.542 . PMID 11304470 .
- Pácha J, Lisa V, Miksík I (février 2002). "Effet de la différenciation cellulaire sur l'activité 11beta-hydroxystéroïde déshydrogénase dans l'intestin". Stéroïdes . 67 (2) : 119–26. doi : 10.1016/S0039-128X(01)00143-X . PMID 11755176 . S2CID 568790 .
- Albertin G, Tortorella C, Malendowicz LK, Aragona F, Neri G, Nussdorfer GG (mai 2002). « Le cortex surrénalien humain et les adénomes sécrétant l'aldostérone expriment à la fois les gènes 11beta-hydroxystéroïde déshydrogénase de type 1 et de type 2 ». Journal international de médecine moléculaire . 9 (5) : 495-8. doi : 10.3892/ijmm.9.5.495 . PMID 11956655 .
- Mazzocchi G, Malendowicz LK, Aragona F, Tortorella C, Gottardo L, Nussdorfer GG (juillet 2002). "Les types 1 et 2 de déshydrogénase 11beta-hydroxystéroïde sont régulés à la hausse et à la baisse dans les adénomes surrénaliens sécrétant du cortisol". Journal de médecine d'investigation . 50 (4) : 288-92. doi : 10.2310/6650.2002.33012 . PMID 12109593 .