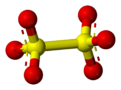
Dithionate - Dithionate
|
|
|||
| Noms | |||
|---|---|---|---|
|
Nom IUPAC
Dithionate
|
|||
|
Nom IUPAC systématique
Bis(trioxydosulfate)( S — S )(2−) |
|||
| Identifiants | |||
|
Modèle 3D ( JSmol )
|
|||
| ChEBI | |||
| ChemSpider | |||
|
CID PubChem
|
|||
|
Tableau de bord CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriétés | |||
|
S 2O2− 6 |
|||
| Masse molaire | 160,126 g mol -1 | ||
| Acide conjugué | Acide dithionique | ||
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 °C [77 °F], 100 kPa). |
|||
| Références de l'infobox | |||
L' anion dithionate (ou métabisulfate ) , S
2O2−
6, est un oxoanion de soufre dérivé de l' acide dithionique , H 2 S 2 O 6 . Sa formule chimique est parfois écrite dans un format semi-structural, comme [O 3 SSO 3 ] 2− .
Les atomes de soufre de l'ion dithionate sont à l' état d'oxydation +5 en raison de la présence de la liaison S-S. En général, les dithionates forment des composés stables qui ne sont pas facilement oxydés ou réduits. Les oxydants forts les oxydent en sulfates et les agents réducteurs forts les réduisent en sulfites et dithionites . Les solutions aqueuses de dithionates sont assez stables et peuvent être bouillies sans décomposition.
L' irradiation des dithionates cristallins produit du SO•−
3 ions radicaux . L'électron non apparié dans le SO•−
3peut être détecté par résonance paramagnétique électronique et le dithionate de baryum a été proposé comme base pour un dosimètre de rayonnement .
L'ion dithionate peut agir comme un ligand bidenté .
La structure de l'ion dithionate à l'état solide est décalée dans Na 2 S 2 O 6 ·2H 2 O, alors que dans le sel de potassium anhydre, elle est presque éclipsée .
Composés
Les composés contenant l'ion dithionate comprennent :
- dithionate de sodium , Na 2 S 2 O 6
- dithionite de potassium , K 2 S 2 O 6
- dithionate de baryum , BaS 2 O 6
Les références
Liens externes
![]() Médias liés à l' ion dithionate sur Wikimedia Commons
Médias liés à l' ion dithionate sur Wikimedia Commons