Altrétamine - Altretamine
 | |
 | |
| Donnée clinique | |
|---|---|
| Appellations commerciales | Hexalen |
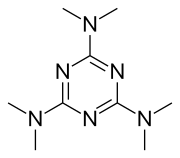
| Autres noms | 2,4,6-Tris (diméthylamino) -1,3,5-triazine |
| AHFS / Drugs.com | Monographie |
| MedlinePlus | a601200 |
| Données de licence | |
Catégorie de grossesse |
|
| Voies d' administration |
Orale ( capsules ) |
| Code ATC | |
| Statut légal | |
| Statut légal | |
| Données pharmacocinétiques | |
| Liaison protéique | 94% |
| Métabolisme | Foie extensif |
| Métabolites | Pentaméthylmélamine, tétraméthylmélamine |
| Demi-vie d' élimination | 4,7 à 10,2 heures |
| Identifiants | |
| |
| Numero CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| Tableau de bord CompTox ( EPA ) | |
| Carte Info ECHA |
100.010.391 |
| Données chimiques et physiques | |
| Formule | C 9 H 18 N 6 |
| Masse molaire | 210,285 g · mol −1 |
| Modèle 3D ( JSmol ) | |
| |
| |
| (Vérifier) | |
L'altrétamine (nom commercial Hexalen ) est un agent antinéoplasique . Il a été approuvé par la FDA américaine en 1990.
Les usages
Il est indiqué pour une utilisation en monothérapie dans le traitement palliatif des patientes atteintes d' un cancer de l'ovaire persistant ou récidivant après un traitement de première intention avec une association à base de cisplatine et / ou d'agent alkylant .
Il n'est pas considéré comme un traitement de première intention, mais il peut être utile comme thérapie de sauvetage . Il présente également l'avantage d'être moins toxique que les autres médicaments utilisés pour traiter le cancer de l'ovaire réfractaire.
Mécanisme
Le mécanisme précis par lequel l'altrétamine exerce son effet anticancéreux est inconnu mais il est classé par le MeSH comme un agent antinéoplasique alkylant .
On pense que cette structure unique endommage les cellules tumorales par la production du formaldéhyde , une espèce faiblement alkylante , un produit de la N- déméthylation médiée par CYP450 . Administrée par voie orale, l'altrétamine est largement métabolisée au premier passage, produisant principalement des métabolites mono- et didéméthylés. Des réactions de déméthylation supplémentaires se produisent dans les cellules tumorales, libérant du formaldéhyde in situ avant que le médicament ne soit excrété dans l'urine. Les intermédiaires carbinolamine (méthylol) du métabolisme médié par le CYP450 peuvent également générer des espèces iminium électrophiles capables de réagir de manière covalente avec des résidus d'ADN guanine et cytosine ainsi qu'avec des protéines. La réticulation d'ADN médiée par l'iminium et la réticulation interstrand ADN-protéine, médiée à la fois par l'intermédiaire iminium et le formaldéhyde, ont été démontrées, bien que l'importance de la réticulation de l'ADN sur l'activité antitumorale de l'altrétamine soit incertaine.
Effets secondaires
Les effets secondaires comprennent les nausées , les vomissements , l' anémie et la neuropathie sensorielle périphérique .
Les interactions
L'association avec la pyridoxine (vitamine B 6 ) diminue la neurotoxicité mais s'est avérée réduire l'efficacité d'un régime d'altrétamine / cisplatine . Un inhibiteur de la MAO peut provoquer une hypotension orthostatique sévère lorsqu'il est associé à l'altrétamine; et la cimétidine peut augmenter sa demi-vie d'élimination et sa toxicité.
Voir également
Références
