Stéarate de magnésium - Magnesium stearate
|
|
| Des noms | |
|---|---|
|
Nom IUPAC
Octadécanoate de magnésium
|
|
| Identifiants | |
|
Modèle 3D ( JSmol )
|
|
| ChEBI | |
| ChemSpider | |
| Carte d'information de l'ECHA |
100.08.320 |
| numéro E | E572 (régulateurs d'acidité, ...) |
|
CID PubChem
|
|
| UNII | |
|
Tableau de bord CompTox ( EPA )
|
|
|
|
|
|
| Propriétés | |
|
Mg( C 18H 35O 2) 2 |
|
| Masse molaire | 591,27 g/mol |
| Apparence | poudre blanche claire |
| Odeur | léger |
| Densité | 1,026 g / cm 3 |
| Point de fusion | 88,5 °C (191,3 °F; 361,6 K) |
| 0,003 g/100 ml (15 °C) 0,004 g/100 ml (25 °C) 0,008 g/100 ml (50 °C) |
|
| Solubilité | négligeable dans l' éther et l' alcool légèrement soluble dans le benzène |
| Dangers | |
| Fiche de données de sécurité | FDS externe |
| NFPA 704 (diamant de feu) | |
| point de rupture | 250 °C (482 °F; 523 K) |
| Dose ou concentration létale (LD, LC) : | |
|
DL 50 ( dose médiane )
|
> 1000 mg/kg (orale, rat) |
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Références de l'infobox | |
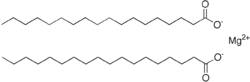
Le stéarate de magnésium est le composé chimique de formule Mg( C
18H
35O
2)
2. C'est un savon composé de sel contenant deux équivalents de stéarate (l'anion de l'acide stéarique ) et un cation magnésium (Mg 2+ ). Le stéarate de magnésium est une poudre blanche insoluble dans l'eau. Ses applications exploitent sa douceur, son insolubilité dans de nombreux solvants et sa faible toxicité. Il est utilisé comme agent de démoulage et comme composant ou lubrifiant dans la production de produits pharmaceutiques et cosmétiques.
Fabrication
Le stéarate de magnésium est produit par la réaction du stéarate de sodium avec des sels de magnésium ou par traitement de l'oxyde de magnésium avec de l'acide stéarique. Certains compléments nutritionnels précisent que le stéarate de sodium utilisé dans la fabrication du stéarate de magnésium est produit à partir d'acide stéarique d'origine végétale.
Les usages
Le stéarate de magnésium est souvent utilisé comme anti-adhérent dans la fabrication de comprimés, gélules et poudres médicaux. À cet égard, la substance est également utile car elle possède des propriétés lubrifiantes , empêchant les ingrédients de coller aux équipements de fabrication lors de la compression de poudres chimiques en comprimés solides ; Le stéarate de magnésium est le lubrifiant le plus couramment utilisé pour les comprimés. Cependant, cela peut entraîner une mouillabilité plus faible et une désintégration plus lente des comprimés et une dissolution plus lente et encore plus faible du médicament.
Le stéarate de magnésium peut également être utilisé efficacement dans les procédés de revêtement à sec.
Dans la création de bonbons pressés, le stéarate de magnésium agit comme agent de démoulage et il est utilisé pour lier le sucre dans les bonbons durs tels que les menthes.
Le stéarate de magnésium est un ingrédient courant dans les préparations pour bébés.
Dans l' UE et l' AELE, il est répertorié comme additif alimentaire E470b .
Occurrence
Le stéarate de magnésium est un composant majeur des anneaux de baignoire. Lorsqu'ils sont produits par du savon et de l' eau dure , le stéarate de magnésium et le stéarate de calcium forment tous deux un solide blanc insoluble dans l'eau et sont collectivement connus sous le nom d' écume de savon .
Sécurité
Le stéarate de magnésium est généralement considéré comme sûr pour la consommation humaine à des niveaux inférieurs à 2500 mg/kg par jour et est classé aux États-Unis comme généralement reconnu comme sûr (GRAS). En 1979, le sous-comité de la FDA sur les substances GRAS (SCOGS) a rapporté : « Il n'y a aucune preuve dans les informations disponibles sur... le stéarate de magnésium... qui démontre, ou suggère des motifs raisonnables de suspecter, un danger pour le public lorsqu'ils sont utilisés à des niveaux qui sont actuellement actuels et de la manière actuellement pratiquée, ou qui pourraient raisonnablement être attendus à l'avenir. »
Les références
- ^ un b Angelo Nora, Alfred Szczepanek, Gunther Koenen, "Savons métalliques" dans l'Encyclopédie d'Ullmann de chimie industrielle 2005 Wiley-VCH, Weinheim. doi : 10.1002/14356007.a16_361
- ^ "Résultats de recherche rapide du DSLD" . Base de données d'étiquettes de compléments alimentaires . Instituts nationaux de la santé . Consulté le 27 décembre 2015 .
- ^ Ritter, Steve (2008). "Qu'est-ce que c'est ? Excipients : Les ingrédients inactifs des médicaments remplissent plusieurs fonctions dans l'administration des médicaments" . Nouvelles de la chimie et de l'ingénierie . 86 (1) : 25. doi : 10.1021/cen-v086n001.p025 .
- ^ Sworbrick, James; Boylan, James C. (1990). Encyclopédie de la technologie pharmaceutique . p. 2274. ISBN 9780824728243.
- ^ Weiner, Myra L.; Kotkoskie, Lois A. (1999). Toxicité et sécurité des excipients . p. 10 . ISBN 9780824782108.
- ^ Demuth; et al. (2017). "Enquête sur la dissolution détériorée de l'itraconazole amorphe : description de l'incompatibilité avec le stéarate de magnésium et solutions possibles" . Pharmaceutique Moléculaire . 14 (11) : 3927-3934. doi : 10.1021/acs.molpharmaceut.7b00629 . PMID 28972782 .
- ^ Ouabbas Y, Dodds J., Galet L., Chamayou A., Baron M. (2009). « Revêtement particule-particule dans un mélangeur à impact cyclomix » (PDF) . Technologie des poudres . 189 (2) : 245-252. doi : 10.1016/j.powtec.2008.04.031 .CS1 maint : plusieurs noms : liste des auteurs ( lien )
- ^ Thomas G., Ouabbas Y., Grosseau P., Baron M., Chamayou A., Galet L. (2009). "Modélisation des principales forces d'interaction entre particules de poudre. Application aux mélanges gel de silice-stéarate de magnésium". Sciences appliquées des surfaces . 255 (17) : 7500–7507. Bibcode : 2009ApSS..255.7500T . CiteSeerX 10.1.1.591.1899 . doi : 10.1016/j.apsusc.2009.03.099 .CS1 maint : plusieurs noms : liste des auteurs ( lien )
- ^ Sato A., Serris E., Grosseau P., Thomas G., Galet L., Chamayou A., Baron M. (2013). "Expérience et simulation de revêtement de particules sèches" (PDF) . Chem. Ing. Sciences . 86 : 164-172. doi : 10.1016/j.ces.2012.07.037 .CS1 maint : plusieurs noms : liste des auteurs ( lien )
- ^ https://www.ctahr.hawaii.edu/oc/freepubs/pdf/FST-9.pdf
- ^ Erich Lück et Gert-Wolfhard von Rymon Lipinski (2002). "Aliments, 3. Additifs alimentaires". Encyclopédie de chimie industrielle d'Ullmann . Weinheim : Wiley-VCH. doi : 10.1002/14356007.a11_561 . ISBN 978-3527306732.
- ^ Sondergaarda, D.; Meyera, O.; Würtzena, G. (1980). "Stéarate de magnésium donné peroprally à des rats. Une étude à court terme". Toxicologie . 17 (1) : 51-55. doi : 10.1016/0300-483X(80)90026-8 . PMID 7434368 .
- ^ Base de données SCOGS de la FDA ; Rapport n° 60 ; Code d'identification : 557-04-0 ; Année : 1979

