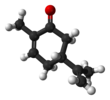
Carvone - Carvone

|
|||
|
|
|||
| Noms | |||
|---|---|---|---|
|
Nom IUPAC préféré
2-méthyl-5- (prop-1-én-2-yl) cyclohex-2-én-1-one |
|||
| Autres noms
2-méthyl-5- (prop-1-én-2-yl) cyclohex-2-énone
2-méthyl-5- (1-méthyléthényl) -2-cyclohexénone Δ 6: 8 (9) - p -Menthadien-2 -one 1-méthyl-4-isopropényl-Δ 6 -cyclohexen-2-one Carvol (obsolète) |
|||
| Identifiants | |||
|
Modèle 3D ( JSmol )
|
|||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| Carte Info ECHA |
100,002,508 |
||
| KEGG | |||
|
PubChem CID
|
|||
| Numéro RTECS | |||
| UNII | |||
|
Tableau de bord CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriétés | |||
| C 10 H 14 O | |||
| Masse molaire | 150,22 g / mol | ||
| Apparence | Liquide clair et incolore | ||
| Densité | 0,96 g / cm 3 | ||
| Point de fusion | 25,2 ° C (77,4 ° F; 298,3 K) | ||
| Point d'ébullition | 231 ° C (448 ° F; 504 K) (91 ° C à 5 mmHg) | ||
| Insoluble (froid) Légèrement soluble (chaud) / soluble à l'état de traces |
|||
| Solubilité dans l' éthanol | Soluble | ||
| Solubilité dans l'éther diéthylique | Soluble | ||
| Solubilité dans le chloroforme | Soluble | ||
|
Rotation chirale ([α] D )
|
−61 ° ( R ) -Carvone 61 ° ( S ) -Carvone |
||
| −92,2 × 10 −6 cm 3 / mol | |||
| Dangers | |||
| Principaux dangers | Inflammable | ||
| Fiche de données de sécurité | MSDS externe | ||
| Pictogrammes SGH |
  
|
||
| Mot de signalisation SGH | Danger | ||
| H304 , H315 , H317 , H411 | |||
| P261 , P264 , P270 , P272 , P273 , P280 , P301 + 310 , P301 + 312 , P302 + 352 , P321 , P330 , P331 , P332 + 313 , P333 + 313 , P362 , P363 , P391 , P405 , P501 | |||
| NFPA 704 (diamant de feu) | |||
| Composés apparentés | |||
|
Cétone associée
|
menthone dihydrocarvone carvomenthone |
||
|
Composés apparentés
|
limonène , menthol , p -cymène , carvéol |
||
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Références Infobox | |||
Carvone fait partie d'une famille de produits chimiques appelés terpénoïdes . La carvone se trouve naturellement dans de nombreuses huiles essentielles , mais elle est plus abondante dans les huiles de graines de carvi ( Carum carvi ), de menthe verte ( Mentha spicata ) et d' aneth .
Les usages
Les deux carvones sont utilisés dans l'industrie alimentaire et aromatique. R - (-) - Carvone est également utilisé pour les produits de rafraîchissement de l'air et, comme de nombreuses huiles essentielles , les huiles contenant des carvones sont utilisées en aromathérapie et en médecine alternative . S - (+) - Carvone a montré un effet suppresseur contre le gain de poids induit par un régime riche en graisses chez la souris.
Applications alimentaires
En tant que composé le plus responsable de la saveur du carvi, de l'aneth et de la menthe verte, la carvone est utilisée depuis des millénaires dans les aliments. La gomme à la menthe verte Wrigley et les Life Savers aromatisés à la menthe verte sont les principaux utilisateurs de l'huile de menthe verte naturelle de Mentha spicata . La graine de carvi est extraite avec de l'alcool pour faire la boisson européenne Kümmel .
Agriculture
S - (+) - Carvone est également utilisé pour empêcher la germination prématurée des pommes de terre pendant le stockage, étant commercialisé aux Pays-Bas à cette fin sous le nom de Talent .
Contrôle des insectes
( R ) - (-) - Carvone a été approuvé par l' Agence américaine de protection de l'environnement pour une utilisation comme répulsif contre les moustiques .
Synthèse organique
Carvone est disponible à peu de frais dans les deux formes énantiomériquement pures, ce qui en fait un matériau de départ attrayant pour la synthèse totale asymétrique de produits naturels . Par exemple, ( S ) - (+) - carvone a été utilisé pour commencer une synthèse de 1998 du terpénoïde quassin :
Stéréoisomérie et odeur
Carvone forme deux formes d'image miroir ou énantiomères : R - (-) - carvone, ou L -carvone, a une odeur de menthe sucrée, comme les feuilles de menthe verte . Son image miroir, S - (+) - carvone, ou D-carvone, a un arôme épicé avec des notes de seigle, comme les graines de carvi . Le fait que les deux énantiomères soient perçus comme ayant une odeur différente est la preuve que les récepteurs olfactifs doivent contenir des groupes chiraux , leur permettant de répondre plus fortement à un énantiomère qu'à l'autre. Tous les énantiomères n'ont pas des odeurs distinctes. On a également constaté que les singes-écureuils étaient capables de faire la distinction entre les énantiomères de la carvone.
Les deux formes sont également désignées par les noms plus anciens de laevo (L) faisant référence à R - (-) -carvone et dextro (D) faisant référence à S - (+) -carvone.
Occurrence
S - (+) - Carvone est le principal constituant (60–70%) de l'huile de graines de carvi ( Carum carvi ), qui est produite à une échelle d'environ 10 tonnes par an. Il se produit également à hauteur d'environ 40 à 60% dans l'huile de graines d' aneth (d' Anethum graveolens ), ainsi que dans l' huile de zeste de mandarine . R - (-) - Carvone est également le composé le plus abondant dans l'huile essentielle de plusieurs espèces de menthe, en particulier l'huile de menthe verte ( Mentha spicata ), qui est composée de 50 à 80% de R - (-) - carvone. La menthe verte est une source majeure de R - (-) - carvone naturellement produite . Cependant, la majorité du R - (-) - carvone utilisé dans les applications commerciales est synthétisé à partir du R - (+) - limonène. L' isomère R - (-) - carvone se trouve également dans l' huile de kuromoji . Certaines huiles, comme l' huile de gingembre , contiennent un mélange des deux énantiomères. De nombreuses autres huiles naturelles, par exemple l' huile de menthe poivrée , contiennent des traces de carvones.
L'histoire
Le carvi était utilisé à des fins médicinales par les anciens Romains, mais le carvone n'a probablement pas été isolé en tant que composé pur jusqu'à ce que Franz Varrentrapp (1815–1877) l'obtienne en 1849. Il était à l'origine appelé carvol par Schweizer. Goldschmidt et Zürrer l'ont identifié comme une cétone liée au limonène , et la structure a finalement été élucidée par Georg Wagner (1849-1903) en 1894.
Préparation
La forme dextro, S - (+) - carvone est obtenue pratiquement pure par distillation fractionnée d' huile de carvi . La forme levo obtenue à partir des huiles qui la contiennent nécessite généralement un traitement supplémentaire pour produire du R - (-) - carvone de haute pureté . Ceci peut être réalisé par la formation d'un composé d'addition avec du sulfure d'hydrogène , à partir duquel la carvone peut être régénérée par traitement avec de l'hydroxyde de potassium dans l' éthanol puis distillation du produit dans un courant de vapeur. La carvone peut être préparée synthétiquement à partir de limonène via du nitrosochlorure de limonène qui peut être formé par traitement du limonène avec du nitrite d'isoamyle dans de l'acide acétique glacial . Ce composé est ensuite converti en carvoxime, ce qui peut être obtenu par reflux avec du DMF dans l' isopropanol . Le reflux de la carvoxime avec de l'acide oxalique à 5% donne de la carvone. Cette procédure permet d'obtenir du R - (-) - carvone à partir du R - (+) - limonène. Le d-limonène est principalement utilisé comme précurseur de la S - (+) - carvone. La disponibilité à grande échelle d'écorces d'orange, un sous-produit de la production de jus d'orange, a rendu le limonène disponible à bon marché et la carvone synthétique préparée à peu de frais.
La biosynthèse de la carvone se fait par oxydation du limonène .
Propriétés chimiques
Réduction
Il y a trois doubles liaisons dans la carvone capables de réduction; le produit de la réduction dépend des réactifs et des conditions utilisés. L'hydrogénation catalytique de la carvone ( 1 ) peut donner soit du carvomenthol ( 2 ) soit de la carvomenthone ( 3 ). Le zinc et l'acide acétique réduisent la carvone en dihydrocarvone ( 4 ). La réduction du MPV en utilisant le propane-2-ol et l'isopropoxyde d'aluminium pour la réduction du groupe carbonyle uniquement pour fournir du carvéol ( 5 ); une combinaison de borohydrure de sodium et de CeCl 3 ( réduction de Luche ) est également efficace. L'hydrazine et l'hydroxyde de potassium donnent du limonène ( 6 ) via une réduction de Wolff-Kishner .
Oxydation
L'oxydation de la carvone peut également conduire à une variété de produits. En présence d'un alcali tel que Ba (OH) 2 , la carvone est oxydée par l' air ou l' oxygène pour donner la dicétone 7 . Avec le peroxyde d'hydrogène, l' époxyde 8 est formé. La carvone peut être clivée à l'aide d' ozone puis de vapeur, donnant la di lactone 9 , tandis que KMnO 4 donne 10 .
Ajouts conjugués
En tant que cétone α, β; -insaturée , la carvone subit des ajouts conjugués de nucléophiles. Par exemple, la carvone réagit avec le diméthylcuprate de lithium pour placer un groupe méthyle trans sur le groupe isopropényle avec une bonne stéréosélectivité . L' énolate résultant peut ensuite être allylé en utilisant du bromure d'allyle pour donner la cétone 11 .
Métabolisme
Dans le corps, in vivo Des études indiquent que les deux énantiomères de la carvone sont principalement métabolisés en acide dihydrocarvonic , l' acide carvonic et uroterpenolone . (-) - Carveol est également formé en tant que produit mineur par réduction par NADPH . (+) - Carvone est également converti en (+) - carveol. Cela se produit principalement dans le foie et implique la cytochrome P450 oxydase et la (+) - trans-carvéol déshydrogénase .
Les références
Liens externes
- Carvone au tableau périodique des vidéos (Université de Nottingham)