Cyclobutanone - Cyclobutanone

|
|
| Noms | |
|---|---|
|
Nom IUPAC préféré
Cyclobutanone |
|
| Identifiants | |
|
Modèle 3D ( JSmol )
|
|
| ChemSpider | |
| Carte Info ECHA |
100.013.405 |
|
PubChem CID
|
|
| UNII | |
|
Tableau de bord CompTox ( EPA )
|
|
|
|
|
|
| Propriétés | |
| C 4 H 6 O | |
| Masse molaire | 70,091 g · mol −1 |
| Apparence | Liquide incolore |
| Densité | 0,9547 g / cm 3 (0 ° C) |
| Point de fusion | −50,9 ° C (−59,6 ° F; 222,2 K) |
| Point d'ébullition | 99,75 ° C (211,55 ° F; 372,90 K) |
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 ° C [77 ° F], 100 kPa). |
|
| Références Infobox | |
La cyclobutanone est un composé organique de formule moléculaire (CH 2 ) 3 CO. Il s'agit d'une cétone cyclique à quatre chaînons (cycloalcanone). C'est un liquide volatil incolore à température ambiante. Étant donné que la cyclopropanone est très sensible, la cyclobutanone est la plus petite cétone cyclique facile à manipuler.
Préparation
Le chimiste russe Nikolai Kischner a préparé la cyclobutanone pour la première fois en 1905. Il a synthétisé la cyclobutanone avec un faible rendement à partir de l' acide cyclobutanecarboxylique en plusieurs étapes de réaction. Ce processus est lourd et inefficace selon les normes actuelles.
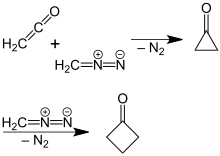
Des synthèses plus efficaces et à haut rendement ont depuis été développées. Une stratégie implique la dégradation des éléments constitutifs à cinq carbones. Par exemple, la décarboxylation oxydative de l'acide cyclobutanecarboxylique a été améliorée par l'utilisation d'autres réactifs et méthodes. Une préparation plus récente et plus efficace de cyclobutanone a été trouvée par P. Lipp et R. Köster dans laquelle une solution de diazométhane dans l'éther diéthylique est mise à réagir avec du cétène . Cette réaction est basée sur une expansion cyclique de l' intermédiaire cyclopropanone initialement formé, dans laquelle l'azote moléculaire est séparé. Le mécanisme de la réaction a été confirmée par une réaction utilisant 14 diazométhane C-marqué.
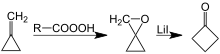
Une autre synthèse de cyclobutanone implique un réarrangement catalysé par le lithium de l'oxaspiropentane, qui est formé par époxydation du méthylènecyclopropane facilement accessible .
La cyclobutanone peut également être préparée en deux étapes par dialkylation du 1,3-dithiane avec du 1-bromo-3-chloropropane suivie d'une déprotection de la cétone avec du chlorure mercurique (HgCl 2 ) et du carbonate de cadmium (CdCO 3 ).
Réactions
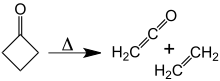
À environ 350 ° C, la cyclobutanone se décompose en éthylène et cétène . L' énergie d'activation pour cette [2 + 2] cycloréversion est de 52 kcal / mol. La réaction de réversion, la [2 + 2] cycloaddition de cétène et d'éthylène, n'a jamais été observée.
Voir également
Autres cétones cycliques: