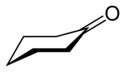
Cyclohexanone - Cyclohexanone
|
|
|||
|
|
|||
| Des noms | |||
|---|---|---|---|
|
Nom IUPAC préféré
Cyclohexanone |
|||
| Autres noms
oxocyclohexane, cétone pimélique, cétohexaméthylène, cyclohexyl cétone, cétocyclohexane, hexanon, Hydrol-O, Sextone, K, Anone
|
|||
| Identifiants | |||
|
Modèle 3D ( JSmol )
|
|||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| Banque de médicaments | |||
| Carte d'information de l'ECHA |
100.003.302 |
||
| Numéro CE | |||
| KEGG | |||
|
CID PubChem
|
|||
| UNII | |||
|
Tableau de bord CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriétés | |||
| C 6 H 10 O | |||
| Masse molaire | 98,15 g/mol | ||
| Apparence | Liquide incolore | ||
| Odeur | menthe poivrée ou de l' acétone -comme | ||
| Densité | 0,9478 g/mL, liquide | ||
| Point de fusion | −47 °C (−53 °F; 226 K) | ||
| Point d'ébullition | 155,65 °C (312,17 °F; 428,80 K) | ||
| 8,6 g/100 ml (20 °C) | |||
| Solubilité dans tous les solvants organiques | Miscible | ||
| La pression de vapeur | 5 mmHg (20°C) | ||
| -62,04·10 −6 cm 3 /mol | |||
|
Indice de réfraction ( n D )
|
1.447 | ||
| Viscosité | 2,02 cP à 25 °C | ||
| Thermochimie | |||
|
Entropie molaire standard ( S |
+229,03 JK -1 .mol -1 | ||
|
Std enthalpie de
formation (Δ f H ⦵ 298 ) |
−270,7 kJmol −1 | ||
|
Std enthalpie de
combustion (Δ c H ⦵ 298 ) |
−3519,3 kJmol −1 | ||
| Dangers | |||
| Pictogrammes SGH |
  
|
||
| Mention d'avertissement SGH | Danger | ||
| H226 , H302 , H312 , H332 , H315 , H318 | |||
| P280 , P305+351+338 | |||
| NFPA 704 (diamant de feu) | |||
| point de rupture | 44 °C (111 °F; 317 K) | ||
| 420 °C (788 °F; 693 K) | |||
| Limites d'explosivité | 1,1-9,4% | ||
| Dose ou concentration létale (LD, LC) : | |||
|
CL 50 ( concentration médiane )
|
8000 ppm (rat, 4 heures) | ||
|
LC Lo (le plus bas publié )
|
4706 ppm (souris, 1,5 h) | ||
| NIOSH (limites d'exposition pour la santé aux États-Unis) : | |||
|
PEL (Autorisé)
|
TWA 50 ppm (200 mg/m 3 ) | ||
|
REL (recommandé)
|
TWA 25 ppm (100 mg/m 3 ) [peau] | ||
|
IDLH (Danger immédiat)
|
700 ppm | ||
| Composés apparentés | |||
|
Cétones associées
|
Cyclopentanone , cycloheptanone | ||
|
Composés apparentés
|
Cyclohexanol | ||
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 °C [77 °F], 100 kPa). |
|||
|
|
|||
| Références de l'infobox | |||
La cyclohexanone est le composé organique de formule (CH 2 ) 5 CO. La molécule est constituée d'une molécule cyclique à six atomes de carbone avec un groupe fonctionnel cétone . Cette huile incolore a une odeur rappelant celle de l' acétone . Au fil du temps, les échantillons de cyclohexanone prennent une couleur jaune. La cyclohexanone est légèrement soluble dans l'eau et miscible avec les solvants organiques courants. Des milliards de kilogrammes sont produits chaque année, principalement en tant que précurseur du nylon .
Production
La cyclohexanone est produite par l'oxydation du cyclohexane dans l'air, généralement à l'aide de catalyseurs au cobalt :
- C 6 H 12 + O 2 → (CH 2 ) 5 CO + H 2 O
Ce procédé co-forme le cyclohexanol , et ce mélange, appelé « KA Oil » pour huile cétone-alcoolique, est la principale charge d'alimentation pour la production d' acide adipique . L'oxydation fait intervenir des radicaux et l'intermédiation de l' hydroperoxyde C 6 H 11 O 2 H. Dans certains cas, le cyclohexanol purifié, obtenu par hydratation du cyclohexène , est le précurseur. Alternativement, la cyclohexanone peut être produite par hydrogénation partielle du phénol :
- C 6 H 5 OH + 2 H 2 → (CH 2 ) 5 CO
Ce procédé peut également être ajusté pour favoriser la formation de cyclohexanol.
ExxonMobil a développé un procédé dans lequel le benzène est hydroalkylé en cyclohexylbenzène . Ce dernier produit est oxydé en un hydroperoxyde puis clivé en phénol et cyclohexanone. Par conséquent, ce nouveau procédé sans produire le sous-produit d'acétone semble attrayant et est similaire au procédé Cumène car un hydroperoxyde est formé puis décomposé pour donner deux produits clés.
Méthodes de laboratoire
La cyclohexanone peut être préparée à partir de cyclohexanol par oxydation avec du trioxyde de chrome ( oxydation de Jones ). Une autre méthode utilise l' hypochlorite de sodium oxydant plus sûr et plus facilement disponible .
Les usages
La grande majorité de la cyclohexanone est consommée dans la production de précurseurs du Nylon 6,6 et du Nylon 6 . Environ la moitié de l'approvisionnement mondial est convertie en acide adipique , l'un des deux précurseurs du nylon 6,6 . Pour cette application, l'huile KA (voir ci-dessus) est oxydée avec de l'acide nitrique . L'autre moitié de l'offre de cyclohexanone est convertie en cyclohexanone oxime . En présence de catalyseur acide sulfurique , l' oxime se réarrange en caprolactame , un précurseur du nylon 6 :
Réactions de laboratoire
En plus des réactions à grande échelle conduites au service de l'industrie des polymères, de nombreuses réactions ont été développées pour la cyclohexanone. En présence de lumière, il subit une alpha-chloration pour donner la 2-chlorocyclohexanone. Il forme un éther de triméthylsilylénol lors d'un traitement avec du chlorure de triméthylsilyle en présence d'une base. Il forme également une énamine avec la pyrolidine.
Utilisation illicite
La cyclohexanone a été utilisée dans la production illicite de phencyclidine et de ses analogues et, en tant que telle, est souvent soumise à des contrôles supplémentaires avant achat.
Sécurité
Comme le cyclohexanol , la cyclohexanone n'est pas cancérigène et est modérément toxique, avec une VLE de 25 ppm pour la vapeur. C'est un irritant.
Les références
- ^ Carte internationale de sécurité chimique 0425
- ^ Guide de poche NIOSH sur les risques chimiques
- ^ A b c d NIOSH Pocket Guide de dangers des produits chimiques. "#0166" . Institut national pour la sécurité et la santé au travail (NIOSH).
- ^ Extrait de données de Landolt-Börnstein IV/25: Viscosity of Pure Organic Liquids and Binary Liquid Mixtures
- ^ Sigma-Aldrich - Cyclohexanone
- ^ A b c Sigma-Aldrich Co. , cyclohexanone . Consulté le 2017-11-20.
- ^ un b "Cyclohexanone" . Concentrations de danger immédiat pour la vie ou la santé (IDLH) . Institut national pour la sécurité et la santé au travail (NIOSH).
- ^ A b c d e Michael T. Musser "cyclohexanol et Cyclohexanone" dans l' Encyclopédie Ullmann de chimie industrielle, Wiley-VCH, Weinheim, 2005. doi : 10.1002 / 14356007.a08_217
- ^ Plotkin, Jeffrey S. (2016-03-21). "Quoi de neuf dans la production de phénol ?" . Société chimique américaine. Archivé de l'original le 2019-10-27 . Récupéré le 2019-10-27 .
- ^ "Phénol - L'industrie chimique essentielle en ligne" . 2017-01-11 . Récupéré le 2019-10-27 .
- ^ "Copie archivée" . Archivé de l'original le 2012-04-26 . Récupéré le 09/07/2012 .CS1 maint: copie archivée comme titre ( lien )
- ^ MS Newman, MD Farbman, H. Hipsher (1945). « 2-chlorocyclohexanone ». Org. Synthé . 25 : 22. doi : 10.15227/orgsyn.025.0022 .CS1 maint : utilise le paramètre auteurs ( lien )
- ^ Valsamma Varghese, Manasi Saha, Kenneth M. Nicholas (1989). « Alkylations utilisant des sels d'hexacarbonyl (Propargylium) dicobalt : 2-(1-méthyl-2-propynyl) cyclohexanone ». Org. Synthé . 67 : 141. doi : 10.15227/orgsyn.067.0141 .CS1 maint : utilise le paramètre auteurs ( lien )
- ^ RB Woodward , IJ Pachter, ML Scheinbaum (1974). "2,2-(Triméthylènedithio)cyclohexanone". Org. Synthé . 54 : 39. doi : 10.15227/orgsyn.054.0039 .CS1 maint : utilise le paramètre auteurs ( lien )
- ^ Shulgin, AT; MacLean, DE (25 septembre 2008). "Synthèse illicite de Phencyclidine (PCP) et plusieurs de ses analogues". Toxicologie Clinique . 9 (4) : 553-560. doi : 10.3109/15563657608988157 .