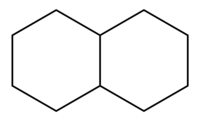
Décaline - Decalin
|
|
| Des noms | |
|---|---|
|
Nom IUPAC préféré
Décahydronaphtalène |
|
| Autres noms
Bicyclo[4.4.0]décane
Décaline |
|
| Identifiants | |
|
Modèle 3D ( JSmol )
|
|
| 878165 | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| Carte d'information de l'ECHA |
100.001.861 |
| Numéro CE | |
| 185147 | |
|
CID PubChem
|
|
| Numéro RTECS | |
| UNII | |
| Numéro ONU | 1147 |
|
Tableau de bord CompTox ( EPA )
|
|
|
|
|
|
| Propriétés | |
| C 10 H 18 | |
| Masse molaire | 138,25 g/mol |
| Apparence | liquide incolore |
| Densité | 0,896 g / cm 3 |
| Point de fusion | trans : −30,4 °C (−22,7 °F, 242,7 K) cis : −42,9 °C (−45,2 °F, 230,3 K) |
| Point d'ébullition | trans : 187 °C (369 °F) cis : 196 °C (384 °F) |
| Insoluble | |
|
Indice de réfraction ( n D )
|
1.481 |
| Dangers | |
| Fiche de données de sécurité | Décaline FDS |
| Pictogrammes SGH |
     
|
| Mention d'avertissement SGH | Danger |
| H226 , H302 , H305 , H314 , H318 , H331 , H332 , H400 , H410 , H411 | |
| P210 , P233 , P240 , P241 , P242 , P243 , P260 , P261 , P264 , P271 , P273 , P280 , P301+310 , P301+330+331 , P303+361+353 , P304+312 , P304+340 , P305+ 351+338 , P310 , P311 , P312 , P321 , P331 , P363 , P370+378 | |
| point de rupture | 57 °C (135 °F; 330 K) |
| 250 °C (482 °F; 523 K) | |
| Composés apparentés | |
|
Composés apparentés
|
Naphtalène ; Tétraline |
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Références de l'infobox | |
La décaline ( décahydronaphtalène , également appelée bicyclo[4.4.0]décane et parfois décaline ), un composé organique bicyclique , est un solvant industriel . Liquide incolore à odeur aromatique, il est utilisé comme solvant pour de nombreuses résines ou additifs pour carburants. C'est l'analogue saturé du naphtalène et peut être préparé à partir de celui-ci par hydrogénation en présence d'un catalyseur . La décaline forme facilement des peroxydes organiques explosifs lors du stockage en présence d'air.
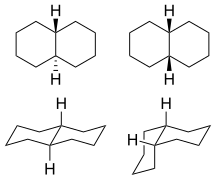
Isomères
Le décahydronaphtalène se présente sous les formes cis et trans . La forme trans est énergétiquement plus stable en raison de moins d' interactions stériques . cis -Decalin est une molécule chirale sans centre chiral ; il a un axe de symétrie de rotation double, mais pas de symétrie réfléchissante. Cependant, la chiralité est annulée par un processus de retournement de chaise qui transforme la molécule en son image miroir.
- 2:
modèle à bille et bâton de cis- décaline
trans- décaline
La seule façon possible de joindre les deux cycles à six chaînons en position trans signifie que le deuxième cycle doit partir de deux liaisons équatoriales (bleues) du premier cycle. Un cycle à six chaînons n'offre pas suffisamment d'espace pour partir d'une position axiale (vers le haut), et atteindre la position axiale de l'atome de carbone voisin, qui sera alors sur la face inférieure de la molécule (voir le modèle du cyclohexane dans figure 5). La structure est gelée conformationnellement, plutôt que d'avoir la capacité de subir le retournement de chaise comme dans l' isomère cis . En biologie, cette fixation est largement utilisée dans le squelette stéroïdien pour construire des molécules (comme la figure 6) qui jouent un rôle clé dans la signalisation entre des cellules distantes.
Réactions
L'oxygénation de la décaline donne l' hydroperoxyde tertiaire , qui se réarrange en cyclodécénone, précurseur de l'acide sébacique .