Oripavine - Oripavine

|
|
| Des noms | |
|---|---|
|
Nom IUPAC
6,7,8,14-Tétradéhydro-4,5α-époxy-6-méthoxy-17-méthylmorphinane-3-ol
|
|
| Autres noms
3-O-desméthylthébaïne
|
|
| Identifiants | |
|
Modèle 3D ( JSmol )
|
|
| ChEMBL | |
| ChemSpider | |
| Carte d'information de l'ECHA |
100.006.715 |
| Numéro CE | |
| KEGG | |
| Engrener | Oripavine |
|
CID PubChem
|
|
| UNII | |
|
Tableau de bord CompTox ( EPA )
|
|
|
|
|
|
| Propriétés | |
| C 18 H 19 N O 3 | |
| Masse molaire | 297,348 g/mol |
| Pharmacologie | |
| N02A ( OMS ) | |
| SC | |
| Statut légal | |
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Références de l'infobox | |
L'oripavine est un opioïde et le principal métabolite de la thébaïne . C'est le composé parent à partir duquel une série d' opioïdes semi-synthétiques sont dérivés, qui comprend les composés étorphine et buprénorphine . Bien que sa puissance analgésique soit comparable à celle de la morphine , elle n'est pas utilisée en clinique en raison de sa toxicité grave et de son faible indice thérapeutique . En raison de son utilisation dans la fabrication d'opioïdes puissants, l'oripavine est une substance contrôlée dans certaines juridictions.
Propriétés pharmacologiques
L'oripavine possède une puissance analgésique comparable à la morphine; cependant, il n'est pas cliniquement utile en raison de sa toxicité grave et de son faible indice thérapeutique . Chez la souris et le rat , des doses toxiques ont provoqué des crises tonico-cloniques suivies de la mort , similaires à celles de la thébaïne . L'oripavine a un potentiel de dépendance significativement supérieur à celui de la thébaïne mais légèrement inférieur à celui de la morphine .
Dérivés pontés
Les propriétés des orvinols, une grande famille de dérivés semi-synthétiques de l'oripavine classiquement synthétisés par la réaction de Diels-Alder de la thébaïne avec un diénophile approprié suivie d'une 3- O- déméthylation en l'oripavine pontée correspondante, sont beaucoup plus pertinentes . Ces composés ont été développés par le groupe dirigé par KW Bentley dans les années 1960, et ces composés Bentley représentent la première série d' agonistes -opioïdes "super puissants" , certains composés de la série étant plus de 10 000 fois la puissance de la morphine en tant que médicament analgésique. Le composé parent d'oripavine ponté simple 6,14-Endoethenotetrahydrooripavine est déjà 40 fois plus puissant que la morphine, mais l'ajout d'un substituant alcool tertiaire ramifié sur la position C7 donne lieu à une large gamme de composés très puissants.
| Nom du médicament | R | Puissance analgésique (Morphine = 1) |
|---|---|---|
| isobutyle | dix | |
| phényle | 34 | |
| n-hexyle | 58 | |
| méthyle | 63 | |
| cyclopentyle | 70 | |
| éthyle | 330 | |
| phénéthyle | 2200 | |
| Etorphine | n-propyle | 3200 |
| cyclohexyle | 3400 | |
| n-pentyle | 4500 | |
| n-butyle | 5200 | |
| isopentyle | 9200 |
D'autres dérivés notables résultent ensuite d'une nouvelle modification de ce modèle, avec la saturation de la double liaison 7,8 de l'étorphine résultant en la dihydroétorphine encore plus puissante (jusqu'à 12 000 fois la puissance de la morphine) et l'acétylation du groupe 3-hydroxy de l'étorphine résultant en acétorphine (8700 × morphine) - bien que l'homologue isopentyle de l'étorphine soit presque trois fois plus puissant, ses dérivés 7,8-dihydro et 3-acétyle sont moins puissants que les dérivés correspondants de l'étorphine à 11 000 × et 1300 × morphine respectivement. Le remplacement du groupe N-méthyle par du cyclopropylméthyle entraîne des antagonistes des opioïdes tels que la diprénorphine (M5050, qui est utilisé comme antidote pour inverser les effets de l'étorphine, M99) et des agonistes partiels tels que la buprénorphine , qui est largement utilisé dans le traitement des opioïdes dépendance .
Statut légal
En raison de la facilité relative de la modification synthétique de l'oripavine pour produire d'autres stupéfiants (par des voies directes ou indirectes via la thébaïne ), le Comité d'experts sur la pharmacodépendance de l' Organisation mondiale de la santé a recommandé en 2003 que l'oripavine soit contrôlée en vertu de l'annexe I de la loi unique de 1961 . Convention sur les stupéfiants . Le 14 mars 2007, la Commission des stupéfiants des Nations Unies a formellement décidé d'accepter ces recommandations et a inscrit l'oripavine à l'annexe I.
Jusqu'à récemment, l'oripavine était un médicament de l' annexe II aux États-Unis par défaut en tant que dérivé de la thébaïne , bien qu'elle ne soit pas explicitement répertoriée. Cependant, en tant qu'État membre en vertu de la Convention unique sur les stupéfiants de 1961 , les États-Unis ont été obligés de contrôler spécifiquement la substance en vertu de la Loi sur les substances contrôlées à la suite de son contrôle international par la Commission des Nations Unies sur les stupéfiants. Le 24 septembre 2007, la Drug Enforcement Administration a officiellement ajouté l'oripavine à l'annexe II.
En vertu du Controlled Substances Act 1970, l'oripavine a un ACSCN de 9330 et un quota de fabrication 2013 de 22 750 kg (50 160 lb).
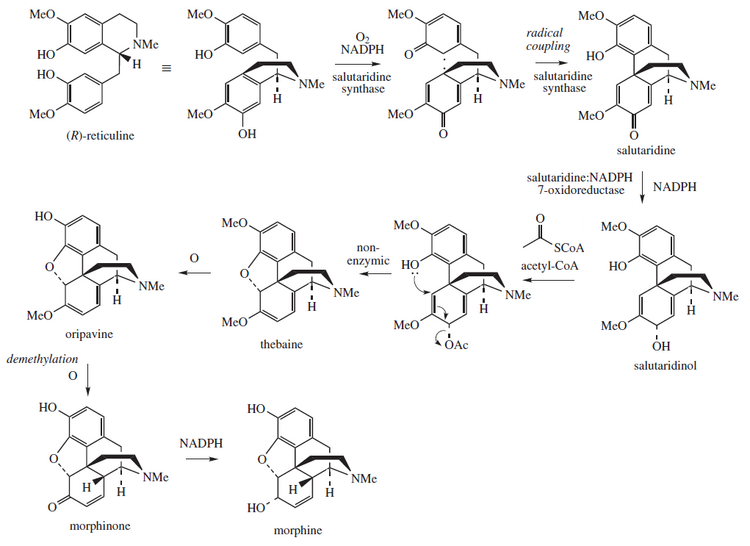
Biosynthèse
Cette molécule est biosynthétiquement liée au métabolisme des dérivés de la morphinane , où la thébaïne et la morphine sont impliquées.