Acide périodique - Periodic acid
|
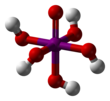
Acide orthopériodique
|
|||
|
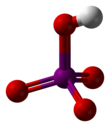
Acide métapériodique
|
|||
 HIO 4 . 2H 2 O
|
|||
| Noms | |||
|---|---|---|---|
| Autres noms | |||
| Identifiants | |||
|
Modèle 3D ( JSmol )
|
|||
| ChemSpider | |||
| Carte d'information de l'ECHA |
100.030.839 |
||
|
CID PubChem
|
|||
| UNII | |||
|
Tableau de bord CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriétés | |||
| HIO 4 (métapériodique) H 5 IO 6 (orthopériodique) |
|||
| Masse molaire | 227,941 g/mol (H 5 IO 6 ) 190,91 g/mol (HIO 4 ) |
||
| Apparence | Cristaux incolores | ||
| Point de fusion | 128,5 °C (263,3 °F; 401,6 K) | ||
| Solubilité | soluble dans l'eau, les alcools | ||
| Base conjuguée | Périodate | ||
| Dangers | |||
| Fiche de données de sécurité | FDS externe | ||
|
Classification UE (DSD) (obsolète)
|
Oxydant ( O ), Toxique ( T ), Corrosif ( C ) | ||
| Phrases R (obsolètes) | R23 R24 R25 R34 R41 | ||
| NFPA 704 (diamant de feu) | |||
| Composés apparentés | |||
|
Autres anions
|
|||
|
Autres cations
|
|||
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 °C [77 °F], 100 kPa). |
|||
|
|
|||
| Références de l'infobox | |||
L' acide périodique ( / ˌ p ɜːr aɪ ɒ d ɪ k / per-oculaire OD ik ) est la plus haute oxoacide de l' iode , dans lequel l'iode existe dans l' état d'oxydation +7. Comme tous les périodates, il peut exister sous deux formes : l'acide orthopériodique, de formule chimique H 5 I O 6 et l'acide métapériodique, qui a pour formule HIO 4 .
L'acide périodique a été découvert par Heinrich Gustav Magnus et CF Ammermüller en 1833.
Synthèse
La production à l'échelle industrielle moderne implique l' oxydation d'une solution d' iodate de sodium dans des conditions alcalines, soit par voie électrochimique sur une anode de PbO 2 , soit par traitement au chlore :
-
OI−
3+ 6 HO−
− 2 e − → IO5−
6+ 3 H 2 O ( contre-ions omis pour plus de clarté) E ° = -1,6 V -
OI−
3+ 6 HO−
+ Cl 2 → IO5−
6+ 2 Cl − + 3 H 2 O
L'acide orthopériodique peut être déshydraté pour donner de l'acide métapériodique par chauffage à 100 °C sous pression réduite.
- H 5 IO 6 HIO 4 + 2 H 2 O
Un chauffage supplémentaire à environ 150 °C donne du pentoxyde d'iode (I 2 O 5 ) plutôt que l' anhydride diiode heptoxyde attendu (I 2 O 7 ). L'acide métapériodique peut également être préparé à partir de divers orthopériodates par traitement avec de l'acide nitrique dilué .
- H 5 IO 6 → HIO 4 + 2 H 2 O
Propriétés
L'acide orthopériodique a un certain nombre de constantes de dissociation acide . Le pKa de l'acide métapériodique n'a pas été déterminé.
- H 5 IO 6 ⇌ H
4OI−
6+ H + , p K a = 3,29
-
H
4OI−
6⇌ H
3OI2−
6+ H + , p K a = 8,31
-
H
3OI2−
6⇌ H
2OI3−
6+ H + , p K a = 11,60
Étant donné qu'il existe deux formes d'acide périodique, il s'ensuit que deux types de sels de periodate sont formés. Par exemple, le métapériodate de sodium , NaIO 4 , peut être synthétisé à partir de HIO 4 tandis que l'orthoperiodate de sodium , Na 5 IO 6 peut être synthétisé à partir de H 5 IO 6 .
Structure
L'acide orthopériodique forme des cristaux monocliniques ( groupe spatial P2 1 / n ) constitués d'un octaèdre IO 6 légèrement déformé relié par des hydrogènes pontants. Cinq distances de liaison I–O sont comprises entre 1,87 et 1,91 et une liaison I–O est de 1,78 . La structure de l'acide métapériodique comprend également des octaèdres IO 6 , mais ceux-ci sont connectés via un partage de bord cis avec des oxygènes de pontage pour former des chaînes infinies unidimensionnelles.
Réactions
Comme tous les periodates, l' acide périodique peut être utilisé pour cliver divers composés 1,2-difonctionnels. Plus particulièrement, l'acide périodique clive les diols vicinaux en deux fragments d' aldéhyde ou de cétone ( réaction de Malaprade ).
Cela peut être utile pour déterminer la structure des glucides car l'acide périodique peut être utilisé pour ouvrir les cycles saccharidiques. Ce procédé est souvent utilisé pour marquer les saccharides avec des molécules fluorescentes ou d'autres marqueurs tels que la biotine . Parce que le processus nécessite des diols vicinaux, l'oxydation au périodate est souvent utilisée pour marquer sélectivement les terminaisons 3' de l' ARN (le ribose a des diols vicinaux ) au lieu de l' ADN car le désoxyribose n'a pas de diols vicinaux.
L'acide périodique est également utilisé comme agent oxydant de force modérée, comme illustré dans l' oxydation de Babler d' alcools allyliques secondaires qui sont oxydés en énones par des quantités stoechiométriques d'acide orthopériodique avec le catalyseur PCC .
Autres oxyacides
Le periodate fait partie d'une série d' oxyacides dans lesquels l'iode peut prendre des états d'oxydation de -1, +1, +3, +5 ou +7. Un certain nombre d' oxydes d'iode neutres sont également connus.
| État d'oxydation de l'iode | -1 | +1 | +3 | +5 | +7 |
|---|---|---|---|---|---|
| Nom | Iodure d'hydrogène | Acide hypoiode | Acide iodé | Acide iodique | Acide périodique |
| Formule | SALUT | HIO | HIO 2 | HIO 3 | HIO 4 ou H 5 IO 6 |
Voir également
Composés de structure similaire :
- Acide perchlorique , acide perbromique et acide perastatique , les acides perhalogéniques apparentés
- Acide tellurique et acide perxénique , les oxoacides isoélectroniques du tellure et du xénon
Composés avec une chimie similaire :