Silencieux (génétique) - Silencer (genetics)
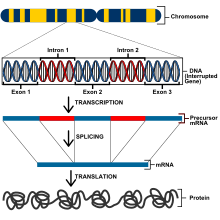
En génétique , un silencieux est une séquence d' ADN capable de se lier à des facteurs de régulation de la transcription , appelés répresseurs . L'ADN contient des gènes et fournit la matrice pour produire l'ARN messager (ARNm). Cet ARNm est ensuite traduit en protéines. Lorsqu'une protéine répresseur se lie à la région du silencieux de l'ADN, l' ARN polymérase est empêchée de transcrire la séquence d'ADN en ARN. Avec la transcription bloquée, la traduction de l'ARN en protéines est impossible. Ainsi, les silencieux empêchent les gènes d'être exprimés sous forme de protéines.
L'ARN polymérase, une enzyme dépendante de l'ADN, transcrit les séquences d'ADN, appelées nucléotides , dans la direction 3 'vers 5' tandis que l'ARN complémentaire est synthétisé dans la direction 5 'vers 3'. L'ARN est similaire à l'ADN, sauf que l'ARN contient de l'uracile, au lieu de la thymine, qui forme une paire de bases avec l'adénine. Une région importante pour l'activité de répression et d'expression génique trouvée dans l'ARN est la région non traduite 3 ' . Il s'agit d'une région à l'extrémité 3 'de l'ARN qui ne sera pas traduite en protéine mais comprend de nombreuses régions régulatrices.
On ne sait pas encore grand chose sur les silencieux, mais les scientifiques continuent d'étudier dans l'espoir de classer davantage de types, d'emplacements dans le génome et de maladies associées aux silencieux.
Fonctionnalité
Emplacements dans le génome
Un silencieux est un élément spécifique à une séquence qui induit un effet négatif sur la transcription de son gène particulier. Il existe de nombreuses positions dans lesquelles un élément silencieux peut être situé dans l'ADN. La position la plus courante se trouve en amont du gène cible où elle peut aider à réprimer la transcription du gène. Cette distance peut varier considérablement entre environ -20 pb et -2 000 pb en amont d'un gène. Certains silencieux peuvent être trouvés en aval d'un promoteur situé dans l'intron ou l'exon du gène lui-même. Des silenceurs ont également été trouvés dans la région non traduite 3 prime (3 'UTR) de l'ARNm.
Les types
Actuellement, il existe deux principaux types de silencieux dans l'ADN, qui sont l'élément silencieux classique et l' élément régulateur négatif non classique (NRE). Dans les silencieux classiques, le gène est activement réprimé par l'élément silencieux, principalement en interférant avec l' assemblage du facteur de transcription général (GTF). Les NRE répriment passivement le gène, généralement en inhibant d'autres éléments situés en amont du gène. Parmi les NRE, il existe certains silencieux qui dépendent de l'orientation, ce qui signifie que le facteur de liaison se lie dans une direction particulière par rapport à d'autres séquences. Les silencieux dépendant du promoteur sont considérés comme des éléments de silencieux car ils dépendent de la position et de l'orientation, mais doivent également utiliser un facteur spécifique au promoteur. Il y a eu une découverte récente des éléments de réponse du groupe polycomb (PRE), qui peuvent permettre et inhiber la répression en fonction de la protéine qui y est liée, et de la présence d'une transcription non codante.
Mécanismes
Pour les silencieux classiques, la voie de signalisation est relativement simple. La répression étant active, les éléments silencieux ciblent l'assemblage des GTF, nécessaires à la transcription du gène. Ces éléments silencieux sont pour la plupart situés en amont du gène et peuvent varier entre des distances courtes et longues. Pour les silencieux à longue portée, il a été observé que l'ADN formera une boucle afin de rapprocher le silencieux du promoteur et de boucler l'ADN interférant. Les silencieux ciblent également les sites d' hélicase dans l'ADN qui sont riches en adénine et en thymine (AT) et enclins à dérouler l'ADN, ce qui laisse de la place pour initier la transcription. L'activité hélicase inhibée conduit à l'inhibition de la transcription. Ceci est couramment observé dans le promoteur du gène de la thyrotropine-ß humaine . Les NRE peuvent induire une courbure dans la région du promoteur pour bloquer les interactions, comme on le voit quand un NRE se lie à Yin-Yang 1 ( YY1 ), et flanquer également des signaux de régulation ou des régions de promoteur. Lorsque la région du silencieux est située dans un intron, il peut y avoir deux types de répressions. Premièrement, il peut y avoir un blocage physique d'un site d'épissure. Deuxièmement, il peut y avoir une courbure dans l'ADN qui inhibera le traitement de l'ARN.
Lorsqu'il est situé dans l'exon ou la région non traduite, le silencieux sera principalement classique ou dépendant de la position. Cependant, ces silencieux peuvent exercer leur activité avant la transcription. La plupart des silencieux sont exprimés de manière constitutive dans les organismes, ne permettant l'activation d'un gène qu'en inhibant le silencieux ou en activant une région activatrice. Le meilleur exemple de ceci est le facteur de silence neuronal restrictif (NRSF) qui est produit par le gène REST . Le gène REST produit du NRSF afin de réprimer la transcription des gènes neuronaux essentiels à la localisation du tissu neuronal. Lorsqu'un silencieux réprime REST , le NRSF est également inhibé, ce qui permet la transcription des gènes neuronaux.
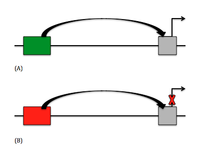
Similitudes avec les exhausteurs
Un autre élément régulateur situé en amont du gène est un activateur . Les amplificateurs fonctionnent comme un interrupteur "d'activation" dans l'expression génique et activeront la région promotrice d'un gène particulier tandis que les silencieux agissent comme un interrupteur "d'arrêt". Bien que ces deux éléments régulateurs agissent l'un contre l'autre, les deux types de séquences affectent la région promotrice de manière très similaire. Parce que les silencieux n'ont pas été complètement identifiés et analysés, les recherches approfondies sur les amplificateurs ont aidé les biologistes à comprendre la mécanique du silencieux. Les amplificateurs peuvent être trouvés dans plusieurs des mêmes domaines que les silencieux sont trouvés, comme en amont du promoteur par de nombreuses paires de kilobases, ou même en aval dans l'intron du gène. La boucle d'ADN est également une fonction modèle utilisée par les amplificateurs afin de raccourcir la proximité du promoteur par rapport à l'amplificateur. Les amplificateurs fonctionnent également avec des facteurs de transcription afin d'initier l'expression, tout comme les silencieux peuvent le faire avec des répresseurs.
Chez les procaryotes et les eucaryotes
Procaryotes

Il existe plusieurs différences dans la régulation du contrôle métabolique chez les eucaryotes et chez les procaryotes. Les procaryotes font varier le nombre d'enzymes spécifiques fabriquées dans leurs cellules afin de réguler l'expression génique, qui est un contrôle métabolique lent, et régulent également les voies enzymatiques par des mécanismes tels que la rétro-inhibition et la régulation allostérique , qui est un contrôle métabolique rapide. Les gènes des procaryotes sont regroupés en fonction de fonctions similaires en unités appelées opérons qui se composent d'un promoteur et d'un opérateur . L'opérateur est le site de liaison du répresseur et a donc une fonction équivalente à la région du silencieux dans l'ADN eucaryote. Lorsqu'une protéine répresseur est liée à l'opérateur, l'ARN polymérase ne peut pas se lier au promoteur pour initier la transcription de l'opéron.
Répression de l' opéron lac
L' opéron lac dans le procaryote E. coli est constitué de gènes qui produisent des enzymes pour décomposer le lactose. Son opéron est un exemple de silencieux procaryote. Les trois gènes fonctionnels de cet opéron sont lacZ, lacY et lacA. Le gène répresseur, lacI, produira la protéine répresseur LacI qui est sous régulation allostérique. Ces gènes sont activés par la présence de lactose dans la cellule qui agit comme une molécule effectrice qui se lie à LacI. Lorsque le répresseur est lié au lactose, il ne se liera pas à l'opérateur, ce qui permet à l'ARN polymérase de se lier au promoteur pour initier la transcription de l'opéron. Lorsque le site allostérique du répresseur n'est pas lié au lactose, son site actif se liera à l'opérateur pour empêcher l'ARN polymérase de transcrire les gènes de l' opéron lac .
Eucaryotes
Les eucaryotes ont un génome beaucoup plus grand et ont donc des méthodes de régulation génique différentes de celles des procaryotes. Toutes les cellules d'un organisme eucaryote ont le même ADN mais sont spécifiées par l'expression génique différentielle, un phénomène connu sous le nom de totipotence génétique . Cependant, pour qu'une cellule exprime les gènes pour un bon fonctionnement, les gènes doivent être étroitement régulés pour exprimer les propriétés correctes. Les gènes chez les eucaryotes sont contrôlés aux niveaux transcriptionnel , post-transcriptionnel , traductionnel et post-traductionnel . Au niveau transcriptionnel, l'expression génique est régulée en modifiant les taux de transcription. Les gènes qui codent pour des protéines comprennent des exons qui coderont pour les polypeptides, des introns qui sont retirés de l'ARNm avant la traduction des protéines, un site de départ transcriptionnel dans lequel l'ARN polymérase se lie et un promoteur.
Répression de la boîte TATA
Les gènes eucaryotes contiennent un promoteur en amont et un promoteur de noyau également appelé promoteur basal. Un promoteur basal commun est la séquence TATAAAAAA connue sous le nom de boîte TATA . La boîte TATA est un complexe avec plusieurs protéines différentes, y compris le facteur de transcription II D (TFIID) qui comprend la protéine de liaison TATA (TBP) qui se lie à la boîte TATA avec 13 autres protéines qui se lient au TBP. Les protéines de liaison à la boîte TATA comprennent également le facteur de transcription II B (TFIIB) qui se lie à la fois à l'ADN et à l'ARN polymérases.
Les silenceurs chez les eucaryotes contrôlent l'expression des gènes à un niveau transcriptionnel dans lequel l'ARNm n'est pas transcrit. Ces séquences d'ADN peuvent agir comme des silencieux ou des amplificateurs basés sur le facteur de transcription qui se lie à la séquence et la liaison de cette séquence empêchera des promoteurs tels que la boîte TATA de se lier à l'ARN polymérase. Une protéine répresseur peut avoir des régions qui se lient à la séquence d'ADN ainsi que des régions qui se lient aux facteurs de transcription assemblés au niveau du promoteur du gène, ce qui créerait un mécanisme de boucle chromosomique. La boucle amène les silencieux à proximité des promoteurs pour garantir que les groupes de protéines nécessaires à une expression génique optimale fonctionneront ensemble.
Silencieux mutés, maladies héréditaires et leurs effets
Des mutations génétiques se produisent lorsque les séquences nucléotidiques d'un organisme sont modifiées. Ces mutations conduisent non seulement à des influences phénotypiques observables chez un individu, mais également à des altérations phénotypiquement indétectables. Les sources de ces mutations peuvent être des erreurs de réplication, des mutations spontanées et des mutagènes chimiques et physiques ( UV et rayonnements ionisants , chaleur). Les silencieux, étant codés dans le génome, sont sensibles à de telles altérations qui, dans de nombreux cas, peuvent conduire à de graves anomalies phénotypiques et fonctionnelles. D'une manière générale, des mutations dans des éléments ou des régions du silencieux pourraient conduire soit à l'inhibition de l'action du silencieux, soit à la répression persistante d'un gène nécessaire. Cela peut alors conduire à l'expression ou à la suppression d'un phénotype indésirable qui peut affecter la fonctionnalité normale de certains systèmes dans l'organisme. Parmi les nombreux éléments et protéines du silencieux, REST / NSRF est un facteur de silencieux important qui a une variété d'impacts, pas seulement dans les aspects neuronaux du développement. En fait, dans de nombreux cas, REST / NSRF agit en conjonction avec RE-1 / NRSE pour réprimer et influencer les cellules non neuronales. Ses effets vont des grenouilles ( Xenopus laevis ) aux humains, avec d'innombrables effets sur le phénotype et aussi sur le développement. Chez Xenopus laevis , un dysfonctionnement ou des lésions REST / NRSF ont été associés à une configuration ectodermique anormale au cours du développement et à des conséquences importantes sur le tube neural, les ganglions crâniens et le développement des yeux. Chez l'homme, une carence en élément silencieux REST / NSRF a été corrélée à la maladie de Huntington en raison de la diminution de la transcription du BDNF .
En outre, des études en cours indiquent que la NRSE est impliquée dans la régulation du gène ANP, qui, lorsqu'il est surexprimé, peut conduire à une hypertrophie ventriculaire . Les mutations dans les complexes du groupe Polycomb (PcG) ont également présenté des modifications significatives dans les systèmes physiologiques des organismes. Par conséquent, la modification des éléments et des séquences du silencieux peut entraîner des changements dévastateurs ou imperceptibles.
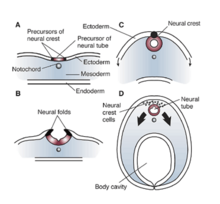
REST / NRSF à Xenopus laevis
Les effets et les influences de RE1 / NRSE et REST / NRSF sont significatifs dans les cellules non neuronales qui nécessitent la répression ou le silence des gènes neuronaux. Ces éléments silencieux régulent également l'expression de gènes qui n'induisent pas de protéines spécifiques aux neurones et des études ont montré l'impact considérable de ces facteurs sur les processus cellulaires. Chez Xenopus laevis, un dysfonctionnement ou une mutation RE1 / NRSE et REST / NRSF a démontré un impact significatif sur le tube neural , les ganglions crâniens et le développement des yeux. Toutes ces altérations peuvent être attribuées à une mauvaise configuration de l' ectoderme pendant le développement de Xenopus. Ainsi, une mutation ou une altération de la région de silence RE1 / NRSE ou du facteur silencieux REST / NRSF peut perturber la différenciation et la spécification appropriées du domaine neuroépithélial et également entraver la formation de peau ou d'ectoderme. L'absence de ces facteurs entraîne une diminution de la production de protéine morphogénétique osseuse (BMP), qui se traduit par un développement déficient de la crête neurale . Par conséquent, les effets de NRSE et NRSF sont d'une importance fondamentale pour la neurogenèse de l'embryon en développement, et également dans les premiers stades de la structuration ectodermique. En fin de compte, un fonctionnement inadéquat de ces facteurs peut entraîner un tube neural aberrant, des ganglions crâniens et un développement oculaire chez Xenopus .
REST / NSRF et maladie de Huntington
La maladie de Huntington (MH) est une maladie neurodégénérative héréditaire, avec des symptômes apparaissant au milieu de l'âge adulte. Les symptômes les plus visibles de cette maladie progressive sont les troubles cognitifs et moteurs, ainsi que les altérations du comportement. Ces déficiences peuvent évoluer vers la démence , la chorée et éventuellement la mort. Au niveau moléculaire, la HD résulte d'une mutation de la protéine huntingtine (Htt). Plus spécifiquement, il existe une répétition anormale d'une séquence CAG vers l'extrémité 5 'du gène, ce qui conduit alors au développement d'un étirement polyglutamine (polyQ) toxique dans la protéine. La protéine Htt mutée affecte les fonctions neuronales propres d'un individu en inhibant l'action de REST / NRSF.
REST / NRSF est un élément silencieux important qui se lie aux régions régulatrices pour contrôler l'expression de certaines protéines impliquées dans les fonctions neurales. Les actions mécanistes de la huntingtine ne sont pas encore entièrement comprises, mais une corrélation entre Htt et REST / NRSF existe dans le développement de la MH. En se fixant au REST / NRSF, la protéine huntingtine mutée inhibe l'action de l'élément silencieux et la retient dans le cytosol. Ainsi, REST / NRSF ne peut pas entrer dans le noyau et se lier à l'élément régulateur RE-1 / NRSE à 21 paires de bases. Une répression adéquate de gènes cibles spécifiques est d'une importance fondamentale, car beaucoup sont impliqués dans le bon développement des récepteurs neuronaux, des neurotransmetteurs , des protéines des vésicules synaptiques et des protéines des canaux. Une carence dans le bon développement de ces protéines peut provoquer les dysfonctionnements neuronaux observés dans la maladie de Huntington. En plus de l'absence de répression due au REST / NRSF inactif, la protéine huntingtine mutée peut également diminuer la transcription du gène du facteur neurotrope dérivé du cerveau (BDNF). Le BDNF influence la survie et le développement des neurones du système nerveux central ainsi que du système nerveux périphérique. Cette répression anormale se produit lorsque la région RE1 / NRSE au sein de la région promotrice BDNF est activée par la liaison de REST / NRSF, ce qui conduit à l'absence de transcription du gène BDNF. Par conséquent, la répression anormale de la protéine BDNF suggère un impact significatif dans la maladie de Huntington.
Recherche actuelle sur REST / NRSF et l'hypertrophie ventriculaire chez les mammifères
REST / NRSF en conjonction avec RE1 / NRSE agit également en dehors du système nerveux en tant que régulateurs et répresseurs. La recherche actuelle a lié l'activité RE1 / NRSE à la régulation de l'expression du gène du peptide natriurétique auriculaire ( ANP ). Une région de régulation NRSE est présente dans la région non traduite 3 'du gène ANP et agit comme un médiateur pour son expression appropriée. La protéine codée par le gène ANP est importante au cours du développement embryonnaire pour la maturation et le développement des myocytes cardiaques . Cependant, pendant la petite enfance et tout au long de l'âge adulte, l'expression de l'ANP est supprimée ou maintenue au minimum dans le ventricule. Ainsi, une induction anormale du gène ANP peut entraîner une hypertrophie ventriculaire et des conséquences cardiaques sévères. Afin de maintenir la répression du gène, NRSF (neuron-restrictive silencer factor) ou REST se lie à la région NRSE dans la région non traduite en 3 'du gène ANP . De plus, le complexe NRSF-NRSE recrute un corépresseur transcriptionnel appelé mSin3. Cela conduit à l'activité de l' histone désacétylase dans la région et à la répression du gène. Par conséquent, des études ont révélé la corrélation entre REST / NRSF et RE1 / NRSE dans la régulation de l' expression du gène ANP dans les myocytes ventriculaires. Une mutation du NRSF ou du NRSE peut conduire à un développement indésirable de myocytes ventriculaires, en raison d'un manque de répression, ce qui peut alors provoquer une hypertrophie ventriculaire. L'hypertrophie ventriculaire gauche, par exemple, augmente le risque de mort subite d'un individu en raison d'une arythmie ventriculaire résultant de l'augmentation de la masse ventriculaire. En plus de l'influence sur le gène ANP , la séquence NRSE régule d'autres gènes embryonnaires cardiaques, tels que le peptide natriurétique cérébral BNP, l'α-actine squelettique et la sous-unité Na, K-ATPase α3. Par conséquent, l'activité régulatrice de la NRSE et du NRSF chez les mammifères empêche non seulement les dysfonctionnements neuronaux, mais également les anomalies physiologiques et phénotypiques dans d'autres régions non neuronales du corps.
Mutations dans les éléments de réponse du groupe polycomb (PRE)
Les complexes régulateurs du groupe Polycomb (PcG) sont connus pour leur influence sur la régulation épigénétique des cellules souches, en particulier dans les cellules souches hématopoïétiques . Le Polycomb Repressive Complex 1 (PRC 1) est directement impliqué dans le processus d'hématopoïèse et fonctionne conjointement avec, par exemple, le gène PcG « Bmi1 ». Des études chez la souris indiquent que les organismes avec «Bmi1» muté démontrent un fonctionnement mitochondrial déficient et ont également entravé la capacité des cellules hématopoïétiques à s'auto-renouveler. De même, des mutations dans les gènes PRC2 étaient liées à des conditions hématologiques telles que la leucémie lymphoblastique aiguë (LAL), qui est une forme de leucémie. Par conséquent, les gènes et les protéines du groupe Polycomb sont impliqués dans le bon maintien de l'hématopoïèse dans le corps.
Références
Liens externes
- Silencer + Elements à la US National Library of Medicine Medical Subject Headings (MeSH)