Organocatalyse de la thiourée - Thiourea organocatalysis
Dans le domaine de l' organocatalyse , la (thio) urée organocatalyse décrit l'utilisation d' urée et de thiourée pour accélérer et altérer stéréochimiquement les transformations organiques. Les effets proviennent d' interactions de liaison hydrogène entre le substrat et la (thio) urée. Contrairement aux catalyseurs classiques, ces organocatalyseurs interagissent par des interactions non covalentes, en particulier des liaisons hydrogène (« protonation partielle »). La portée de ces donneurs de liaisons H à petites molécules appelés organocatalyse (thio) urée couvre à la fois les applications non stéréosélectives et stéréosélectives.
L'histoire
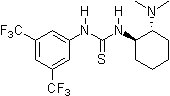
Des contributions pionnières ont été apportées par Kelly, Etter, Jorgensen, Hine, Curran, Göbel et De Mendoza (voir les articles de synthèse cités ci-dessous) sur les interactions de liaison hydrogène de petits composés sans métal avec des sites de liaison riches en électrons. Peter R. Schreiner et ses collègues ont identifié et introduit des dérivés de thiourée pauvres en électrons comme organocatalyseurs de liaison hydrogène. La thiourée de Schreiner, N, N ' -bis [[3,5-bis (trifluorméthyl) phényl thiourée, combine toutes les caractéristiques structurelles pour l'organocatalyse médiée par une double liaison H:
- pauvre en électrons
- structure rigide
- substituants attracteurs d'électrons non coordinants en position 3,4 et / ou 5 d'un cycle phényle
- le groupe 3,5-bis (trifluorométhyl) phényle est le substituant préféré
Interactions catalyseur-substrat
La liaison hydrogène entre les dérivés de la thiourée et les substrats carbonyle implique deux liaisons hydrogène fournies par des substituants amino coplanaires dans la (thio) urée.
Les squaramides s'engagent dans des interactions de double liaison H et sont souvent supérieurs aux thiourées.
Avantages des organocatalyseurs de thiourée
Les thio) urées sont des catalyseurs verts et durables . Lorsqu'elles sont efficaces, elles peuvent offrir ces avantages:
- absence d'inhibition du produit en raison d'une faible liaison enthalpique , mais liaison spécifique - «reconnaissance»
- faible charge de catalyseur (jusqu'à 0,001 mol%)
- Valeurs élevées de TOF (Turn-Over-Frequency) (jusqu'à 5700 h -1 )
- synthèse simple et peu coûteuse à partir d'isothiocyanates et de matières premières fonctionnalisées par amine primaire (pool chiral)
- facile à moduler et à manipuler (stable au banc), aucune atmosphère de gaz inerte requise
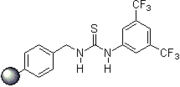
- immobilisation sur une phase solide (organocatalyseurs liés aux polymères), récupération du catalyseur et réutilisabilité
- catalyse dans des conditions presque neutres (pk a thiourea 21,0) et des conditions douces, les substrats sensibles aux acides sont tolérés
- sans métal, non toxique (comparez les catalyseurs traditionnels à l'acide de Lewis contenant des métaux)
- tolérante à l'eau, même catalytiquement efficace dans l'eau ou les milieux aqueux.
Les substrats
Les substrats acceptant les liaisons H comprennent les composés carbonylés , les imines , les nitroalcènes . La réaction Diels-Alder est un processus qui peut bénéficier des catalyseurs (thio) urée.
Catalyseurs
Une grande variété d'organocatalyseurs chiraux à double liaison hydrogène (thio) urée monofonctionnels et bifonctionnels (concept de bifonctionnalité) ont été développés pour accélérer diverses transformations organiques synthétiquement utiles.
1998 : dérivé de la thiourée à base de Schiff chiral (lié au polymère) de Jacobsen pour les réactions de Strecker asymétriques .
2004 : Organocatalyseur chiral bis-thiourée de Nagasawa, catalyse des réactions asymétriques de Baylis-Hillman .
2005 : La thiourée bifonctionnelle de Nagasawa a fonctionnalisé la guanidine, catalyse asymétrique des réactions de Henry (Nitroaldol) .
2005 : Dérivé de thiourée chirale de Ricci avec alkylation énantiosélective de Friedel-Crafts à groupes hydroxy supplémentaires d' indols avec des nitroalcènes.
2005 : Dérivé bifonctionnel de la binaphtyl-thiourée de Wei Wang, catalyse asymétrique des réactions Morita-Baylis-Hillman .
2005 : La thiourée bifonctionnelle de Soos, Connon et Dobson a fonctionnalisé un alcaloïde de Cinchona , des ajouts asymétriques de nitroalcanes aux chalcones ainsi que des malonates aux nitroalcènes
2006 : Pyrrolidine-thiourée bifonctionnelle chirale de Yong Tang, ajouts énantiosélectifs de Michael de cyclohexanone aux nitrooléfines.
2006 : Thiourée chirale liée au PEG de Takemoto, catalyse asymétrique des réactions (tandem-) de Michael du trans -β-nitrostyrène , réactions aza-Henry.
2007 : Wanka / Schreiner, thiourée peptidique chirale à base d' adamantane , catalyse des réactions Morita-Baylis-Hillman.
2007 : Hydroxy- thiourée bifonctionnelle chélatante de Takemoto pour la réaction énantiosélective de type pétasis des quinoléines .
Lectures complémentaires
- Christian M. Kleiner, Peter R. Schreiner (2006). "L'amplification hydrophobe d'organocatalyse non covalente". Chem. Commun. : 4315–4017.
- Z. Zhang et PR Schreiner (2007). "Hydrogénation de transfert catalysée par la thiourée des aldimines". Synlett . 2007 (9): 1455-1457. doi : 10.1055 / s-2007-980349 .
- Wanka, Lukas; Chiara Cabrele; Maksims Vanejews; Peter R. Schreiner (2007). "Acides γ-aminoadamantanecarboxyliques par des amidations directes de liaison C – H". Journal européen de chimie organique . 2007 (9): 1474–1490. doi : 10.1002 / ejoc.200600975 . ISSN 1434-193X .